试剂盒使用说明Word格式.docx
《试剂盒使用说明Word格式.docx》由会员分享,可在线阅读,更多相关《试剂盒使用说明Word格式.docx(23页珍藏版)》请在冰豆网上搜索。
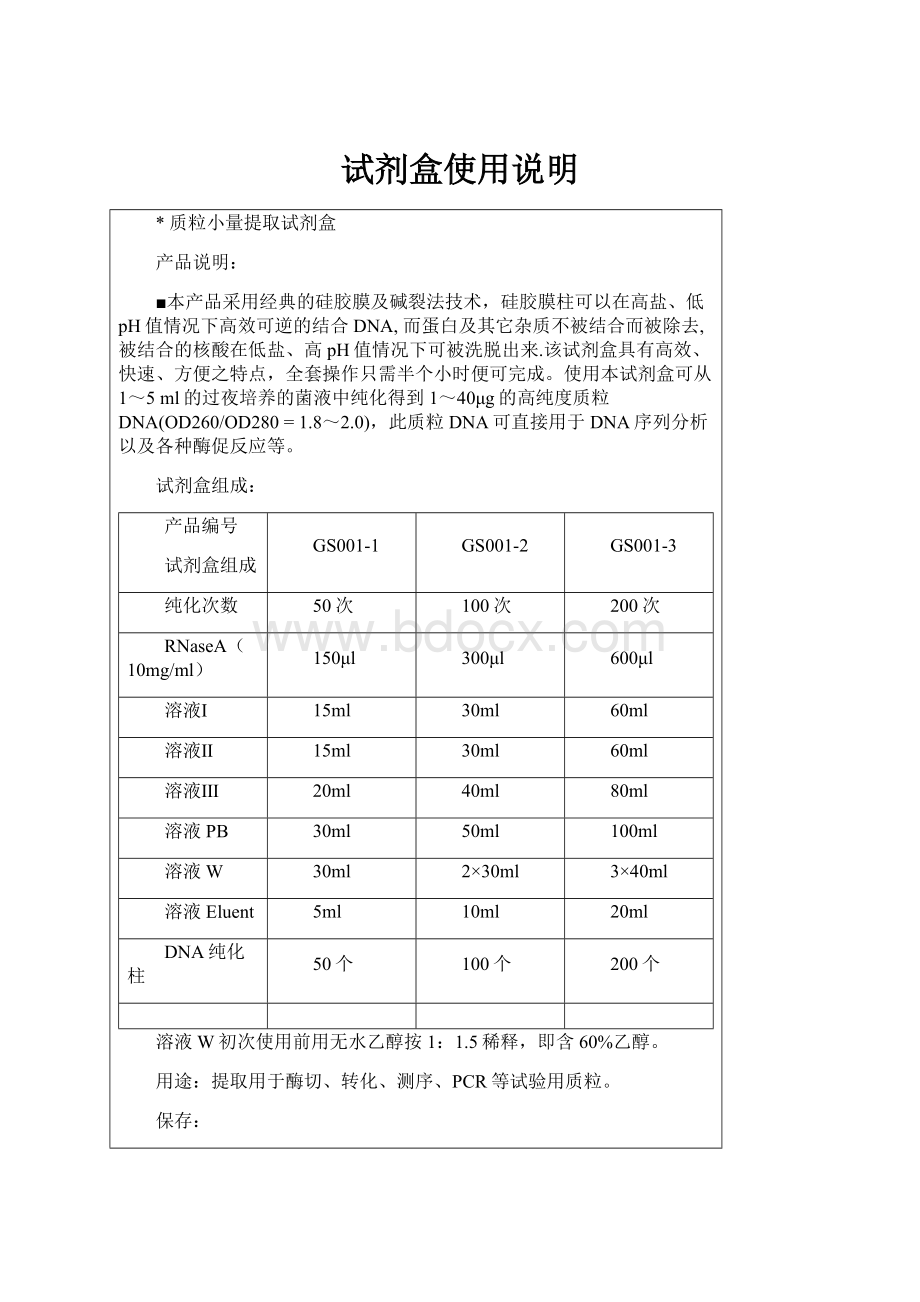
200个
溶液W初次使用前用无水乙醇按1:
1.5稀释,即含60%乙醇。
用途:
提取用于酶切、转化、测序、PCR等试验用质粒。
保存:
初次使用本试剂盒时,请将RNaseA全部加入到溶液Ⅰ中,均匀混合后4℃保存。
溶液Ⅱ:
室温保存,若出现沉淀,请于37℃保温溶解,待恢复至室温后使用。
其他试剂:
室温保存。
操作步骤:
1.
用1.5ml离心管收集1.5-5ml菌液,12000rpm离心60秒,弃上清。
(应根据所培养的菌液的浓度确定收集的菌液量)
2.
加入250µ
l溶液Ⅰ/RNaseA混合液,漩涡振荡使菌液完全重新悬浮。
(菌液重新悬浮对于获得高产量是非常重要的,为使RNA被RNaseA充分降解,让悬浮菌液静置1-2分钟
3.
250µ
l溶液Ⅱ,温和反复颠倒混匀4-10次,室温放置1-2分钟,以获得澄清的裂解液。
(不可剧烈混和,否则会使染色体DNA断裂.)
4.
加入350µ
l溶液Ⅲ,反复颠倒混匀4-6次,12000rpm离心10分钟。
5.
将上清置于DNA纯化柱中,静置1-2分钟。
6.
12000rpm离心60秒,弃虑液。
(注:
此时DNA被吸附于DNA纯化柱中的硅胶膜上。
)
7.
加入500µ
l溶液PB,12000rpm离心60秒,弃虑液。
注:
目的是将硅胶膜上吸附的蛋白、盐等杂质洗脱,得到高质量的DNA。
如果所需的DNA质量要求不是很高此步可以省去.
8.
l溶液W,12000rpm离心60秒,弃虑液。
9.
可选做步骤:
重复步骤8,再用500ul溶液W洗涤柱子一次.
10.12000rpm再次离心60秒,甩干剩余液体。
主要是去除残余酒精,以利于DNA溶解。
11.
将DNA纯化柱置于新的离心管中,加入适量(50-100µ
l)Eluent(≥60℃预热)室温放置2分钟
12000rpm离心60秒,管底即为质粒DNA。
注:
溶液Eluent可用无菌双蒸水代替,但其pH需为8.0-8.5,加入体积视质粒拷贝数多少、
用户对质粒浓度要求而定。
60℃预热,目的是提高产量,温度不需很准,50℃-65℃均可。
*DNA凝胶回收试剂盒
本试剂盒所带DNA纯化柱,具有在高盐、低pH值情况下吸附DNA,低盐、高pH值情况下释放DNA的性质.该试剂盒能从各个等级的琼脂糖凝胶中很好的回收50bp-40kb的DNA带,回收率高达85%.目的DNA带从凝胶上切下来后,经特定的溶液BD处理,可将含目的带的琼脂糖溶解完全,然后转移到一个DNA回收纯化柱上,经过溶液PE快速的洗涤步骤后,DNA便可用去离子水(或低盐缓冲液)洗脱出来,回收产物可用于PCR、连接、测序、限制性酶切等应用。
该试剂盒还适用于PCR产物纯化、酶切产物回收及基因组DNA纯化。
产品编号
GS002-1
GS002-2
GS002-3
溶液BD
溶液PE
2.5ml
5.0ml
溶液PE初次使用前用无水乙醇按1:
4稀释,即含80%乙醇。
保存条件:
室温保存大于24个月。
产品特点:
快速――15min内从凝胶中回收DNA
可靠――最适宜的缓冲液系统保证了高纯度的DNA
安全――无有机溶液抽提
质量――纯净的DNA适用于多种下游应用
可以高效的回收小片段DNA.
通过把切取含DNA片段的琼脂糖凝胶装在1.5ml小离心管中,称其重量近似地确定其体积,每100mg琼脂
糖凝胶相当于100µ
l体积,称量每次切取含DNA片段的琼脂糖凝胶加入等体积的溶液BD。
PCR产物纯化、酶切产物回收及基因组DNA则加入等体积的溶液BD混匀,进入步骤3.
55℃-65℃水浴7-10分钟,直至胶完全融化,期间振荡3次,琼脂糖必须完全融化。
如果体积大于500µ
l,可适当增加融胶时间,若此时溶液变红,可加10µ
l3MNaAC(pH5.0)。
将溶液置于DNA纯化柱中,静置2分钟,12,000rpm离心60秒,若一次加不完,可分两次离心,弃虑液。
加入500µ
l溶液PE(初次使用前用无水乙醇按1:
4稀释)于离心柱中12,000rpm,离心60秒,弃虑液.
用溶液PE(初次使用前用无水乙醇按1:
4稀释)500µ
l再洗一遍,12,000rpm离心60秒。
12,000rpm再次离心2分钟,以甩干剩余液体。
此步对获得较好的DNA产量十分重要)
将离心柱置于新的离心管中,加入60℃预热的溶液Eluent25-35µ
l于纯化柱中(硅胶膜中央),
静置2分钟,12,000rpm离心60秒,管底即为回收的DNA。
将DNA贮存于-20℃。
*PCR产物及DNA片段纯化试剂盒
本试剂盒所带DNA纯化柱,具有在高盐、低pH值情况下吸附DNA,低盐、高pH值情况下释放DNA的性质。
该试剂盒能很好的回收50bp-40kb的DNA片段,回收率高达85%.PCR产物或酶切产物经特定的BD溶液处理,然后转移到一个DNA回收纯化柱上,经过离心吸附,然后经溶液PE快速的洗涤步骤后,DNA便可用去离子水(或低盐缓冲液)洗脱出来,回收产物可用于PCR、连接、测序、限制性酶切等应用。
该试剂盒可从PCR扩增体系、酶切和其它水溶液体系中快速回收纯化DNA,有效去除PCR反应体系中的dNTPs、引物和聚合酶.该试剂盒可以高效的回收小片段DNA(50bp、100bp).该试剂盒还可以用于从琼脂糖凝胶中回收DNA片段。
GS010-1
GS010-2
GS010-3
说明书
1
·
快速――10min内从PCR产物中回收DNA
可以高效的回收小片段DNA(50bp).
注意事项:
溶液PE初次使用前请用无水乙醇按1:
溶液Eluent(10mMTris/HCl,pH8.5)可用无菌双蒸水代替,但其pH需为8.0-8.5,加入体积视回收DNA量
的多少及用户对浓度要求而定。
60℃预热,目的是提高产量,温度不需很准,50℃-65℃均可。
确定PCR反应产物体积,将PCR产物转移至一个1.5ml离心管中,加入等体积的BD溶液,旋涡混匀,
然后进入步骤2.(如果用于从琼脂糖凝胶中回收DNA片段则先进行步骤a和步骤b再进入步骤2)
a.
通过把切取含DNA片段的琼脂糖凝胶装在1.5ml小离心管中,称其重量近似地确定其体积,每100mg琼脂糖凝胶相当于100µ
b.
如果体积大于500µ
将溶液置于DNA纯化柱中,静置2分钟,12,000rpm离心60秒.
将离心柱置于一新的离心管中,加入60℃预热的30-100µ
l溶液Eluent于纯化柱中(硅胶膜中央),
静置2分钟,12,000rpm离心60秒,管底即为回收的DNA。
效果图
*GzolReagent(RNA提取试剂)
CatNo.GS004-150ml;
CatNo.GS004-2100ml
产品说明
■TRIzol是目前最常用的RNA提取试剂.采用异硫氰酸胍一步法提取总RNA原理,在短时间内提取高质量的总RNA。
■方便从人、动物、植物和细菌组织提取总RNA,可同时处理大量样本,提取的RNA没有DNA和蛋白的污染,可用于RT-PCR、NorthernBlot、Dotblot、Nucleaseprotectionassays、cDNA合成等下游应用。
保存
室温下可稳定保存1年,为保证试剂质量,建议保存在2-8℃的环境下。
实验所需试剂但未提供的物品
★氯仿★异丙醇
★75%乙醇(用DEPC处理过的水配制)
★无RNA酶的水或0.5%SDS溶液[调配无RNA酶的水,将水加入无RNA酶的玻璃瓶中,加入DEPC至0.1%(v/v)。
放置过夜并高压灭菌。
SDS溶液必须用DEPC处理过并经高压灭菌的水配制。
预防RNA酶污染:
在抽提RNA过程中任一环节的不正确操作都可能导致RNA酶的污染。
由于RNA酶的活性很难完全抑制,预防其污染是十分必要的。
在实际的操作中应遵循以下指南:
*全程佩戴一次性手套。
皮肤经常带有细菌和霉菌,可能污染RNA的抽提并成为RNA酶的来源。
培养良好的微生物实验操作习惯预防微生物污染。
*使用灭菌的,一次性的塑料器皿和自动吸管抽提RNA,避免使用公共仪器所导致的RNA酶交叉污染。
例如,使用RNA探针的实验室可能用RNA酶A或T1来降低滤纸上的背景,因而某些非一次性的物品(如自动吸管)可能富含RNA酶。
*在TRIzol中,RNA是隔离在RNA酶污染之外的。
而对样品的后续操作会要求用无RNA酶的非一次性的玻璃器皿或塑料器皿。
玻璃器皿可以在150°
C的烘箱中烘烤4小时。
塑料器皿可以在0.5MNaOH中浸泡10分钟,用水彻底漂洗干净后高压灭菌备用。
RNA抽提操作步骤
注意:
用TRIzol抽提RNA时要戴手套和护眼罩。
避免接触皮肤和衣服。
在化学通风橱
完成操作。
避免呼吸道吸入。
如无例外,所有的操作应该在在15~30°
C的条件下。
实验所需试剂但未提供的物品:
*氯仿*异丙醇
*75%乙醇(用DEPC处理过的水配制)
*无RNA酶的水或0.5%SDS溶液[调配无RNA酶的水,将水加入无RNA酶的玻璃瓶中,加入DEPC至0.1%(v/v)。
匀浆化作用
a.组织
用glass或强力匀浆器搅匀组织样品,每50~100mg组织加1ml的TRIzol。
匀浆化时组织样品容积不能超过TRIzol容积的10%。
b.单层生长的细胞
直接往直径3.5cm的培养板中加入1ml的TRIzol溶解细胞,通过移液管分次移出细胞裂解物。
依据培养板的面积而不是依据细胞的数量来决定所需的TRIzol量(每10cm2加1ml)。
当TRIzol量不足时可导致抽提的RNA中污染有DNA。
c.悬浮生长的细胞
通过离心来沉淀细胞。
在TRIzol试剂中用移液管反复吹打来裂解细胞。
每5~10×
106的动
物细胞,植物或酵母菌细胞或每1×
107细菌加1ml的TRIzol。
在加入TRIzol前应避免洗涤细胞,因为那样会增加mRNA降解的可能性。
破裂某些酵母菌和细菌可能需要使用匀浆器。
可选方案:
当样品富含蛋白质,脂肪,多糖或是细胞外物质例如肌肉,脂肪组织和植物的块茎部分时可能需要一额外的分离步骤。
匀浆化后在2~8°
C的条件下以12,000×
g的离心力离心10分钟,移除匀浆中不溶解的物质,余下的沉淀中包含有细胞外膜,多糖,以及高分子量DNA,而上层的超浮游物含有RNA。
在来自于脂肪组织的样品中,大量的脂肪漂在最上层因而应该除掉。
在每一个个案中,将清亮的匀浆溶液转移到一干净的试管中加入氯仿并继续进行下述的分离步骤。
2.分离阶段
将匀浆样品在15-30°
C条件下孵育5分钟以使核蛋白体完全分解。
每1mlTRIzol加0.2ml氯仿。
盖紧样品管盖,用手用力摇晃试管15秒并将其在30°
C下孵育2~3分钟。
在2~8°
C下以不超过12,000×
g的离心力高速冷冻离心15分钟。
离心后混合物分成三层:
下层苯酚-氯仿层,中间层,上层无色的水样层。
RNA无一例外地存在于水样层当中。
水样层的容量大约为所加TRIzol容量的60%。
3.RNA的沉淀
将水样层转移到一干净的试管中,如果希望分离DNA和蛋白,有机层同样要予以保留。
通过将水样层和异丙醇混合来沉淀RNA。
最初均化时的每1mlTRIzol对应0.5ml异丙醇。
将混合的样品在15-30°
C条件下孵育10分钟并在2~8°
g的离心力高速冷冻离心10分钟。
RNA沉淀在离心前通常不可见,形成一胶状片状沉淀附着于试管壁和管底。
4.RNA的漂洗
移去上层悬液。
用75%的乙醇洗涤RNA沉淀一次,每1ml的TRIzol至少加1ml的75%乙醇。
旋涡振荡混合样品并在2~8°
C下以不超过7,500×
g的离心力高速冷冻离心5分钟。
5.RNA的再溶解
在操作的最后,简单干燥RNA沉淀(空气干燥或真空干燥5~10分钟)不要在真空管里离心干燥RNA。
尤为重要的是,不能让RNA沉淀完全干燥那样会极大地降低它的可溶性。
部分溶解的RNA样品其A260/280比值<
1.6。
用移液管尖分几次移取无RNA酶的水或0.5%SDS溶液来溶解RNA,并在55~60°
C下孵育10分钟(当RNA以后要用于酶切反应时,避免使用SDS。
)RNA还能被100%甲酰胺(除去离子)再溶解并保存在–70°
C。
RNA抽提注意事项:
1.从少量的组织(1~10mg)或细胞(102~104)中分离RNA样品:
往组织或细胞中加入800µ
lTRIzol。
待样品裂解后,加入氯仿并进行步骤2中的抽提操作。
在用异丙醇沉淀RNA之前,加入5~10μg无RNA酶的glycogen作为水样层的载体。
为降低其黏度在加入氯仿前用26号注射器抽吸两次以切断基因组DNA。
Glycogen会留在水样层中并和RNA共析出。
在浓缩到4mg/ml之前它不会抑制逆转录反应第一链的合成也不会抑制PCR。
2.在匀化后和加入氯仿之前,样品可以在–60~–70°
C保存至少一个月。
RNA沉淀(步骤4,RNA漂洗)溶于75%的乙醇在2~8°
C至少可以保存一周,在–5~–20°
C下至少可保存一年。
3.台式离心机最大能达到2,600×
g的离心力,如果将离心时间延长到30~60分钟可以满足步骤2和步骤3中的操作
疑难解答:
每1mg组织或1×
106培养细胞预期的RNA产量
1.肝和脾,6~10μg。
2.肾,3~4μg。
3.骨骼肌和脑组织,1~1.5μg。
4.胎盘,1~4μg。
5.上皮细胞(1×
106culturedcells),8~15μg。
6.纤维母细胞(1×
106culturedcells),5~7μg
抽提得率低
1.样品均化或裂解不完全。
2.终RNA不完全再溶解。
A260/A280比率<
1.65
1.在分光光度计测量前用水而不是用TE缓冲液稀释RNA样品。
低离子强度和低pH溶液会增加280nm处的光吸收值。
2.样品匀浆化时所加的TRIzol量太少。
3.匀浆化后样品没有在室温下放置5分钟。
4.分离的水样层中污染有苯酚层。
5.终RNA没有完全溶解。
RNA降解
1.从动物体取下的组织没有立即进行抽提或冰冻保存。
2.用于抽提的样品,或抽提的RNA样品保存于–5~–20°
C,而不是存放于–60~–70°
3.细胞经胰酶消化而分散。
4.水溶液或试管污染有RNA酶。
5.用于琼脂糖凝胶电泳的福尔马林pH低于3.5。
DNA污染
1.样品匀浆化时所加的TRIzol量太少。
2.用于抽提的样品包含有机溶媒(例如,乙醇,DMSO),强缓冲液,或碱性溶液。
蛋白多糖和多糖污染
下述的对RNA沉淀方法(步骤3)的改进能从抽提的RNA中移去复合污染。
以匀浆化时每1mlTRIzol为例,在水样层中加入0.25ml异丙醇后再加入0.25ml的高盐溶液(0.8M柠檬酸钠和1.2MNaCl)。
将终溶液混匀,离心并继续进行前述的抽提操作。
改进后的沉淀法能有效地析出RNA而多糖和蛋白多糖仍以可溶的的形式留在溶液中。
对于含有大量多糖的植物,要抽提其RNA将改进后的沉淀法和在最初匀浆化时多加一次离心(RNA抽提指南,可选方案)合并使用是十分必要的。
*总RNA快速抽提试剂盒
适用范围:
全血、骨髓、组织、细胞、体液
室温,保质期2年。
RB1液置4℃避光保存保质期更长。
性能介绍:
样本量
全血、骨髓1-2ml,培养细胞<
1×
107,组织<
30mg,体液根据细胞量
耗时
培养细胞:
22min;
全血:
25min
洗脱体积
25-50μl
产量
3-10μg/ml全血,100-300μg/1×
107细胞,1-6μg/mg组织
纯度
OD260/OD280:
1.9-2.1
特点
特别设计针对1-2ml全血的提取,无需淋巴细胞分离液离心,不丢失粒细胞,因此获得的RNA产量增加一倍
是替代Trizol的升级产品,获得的RNA产量与Trizol提取相同,但酚和乙醇残留少,提取过程中被RNase污染机会少,提取速度快
使用Trizol提取少量RNA时,反复离心沉淀往往造成RNA丢失,每次提取的得率不一。
本试剂盒可以捕获少量RNA,不同提取批次间变异小
用途
RT-PCR,表达芯片分析,构建cDNA文库,RPA,NorthernBlot等
GS005-1
(50次)
GS005-2
(200次)
RB1
200ml
RB2
洗液
洗脱液
内套柱,外套柱
50套
200套
钢网,平皿,研磨棒
需要时另配(提取组织RNA时用)
1份
操作流程
实验操作前请先认真阅读“注意事项”
1.样本预处理
a.抗凝全血、骨髓:
取1-2ml放入离心管中,12,000rpm离心2min,吸取中间白膜层细胞100μl至1.5mleppendorf管中(吸取时用普通加样枪头口太小,剪去约5mm尖即可。
吸取的白膜层细胞中混有大量红细胞,不影响后继提取);
b.组织块:
剪切成小块后放入平皿(置冰袋上预冷)中的钢网上,加入PBS或生理盐水(约1ml/30mg组织),用研磨棒将组织研磨挤压过钢网,收集过网悬液,取100μl放入eppendorf管中;
c.培养细胞:
悬浮细胞离心后留下细胞团块和适量上清(>
100μl/1×
107细胞),充分吹打直至没有细胞团块,取100μl放入eppendorf管中;
贴壁细胞消化后处理同上。
d.体液及其它液体性样本:
尿液、腹水、胸水、脑积液等根据需要取1-10ml,3,000rpm离心2min,留下沉淀及约100μl上清,充分震荡悬浮沉淀,取100μl放入eppendorf管中;
2.处理好的样本中,加入RB1液1ml,充分颠倒混匀直至完全溶解,室温放置5min。
3.加入氯仿200μl,充分颠倒混匀1min,成均一的乳糜状,离心5min。
4.将上清液小心转移到RNase-free的1.5mleppendorf里(离心分层后,可以吸取上层无色液体约为350µ
l,注意不要吸取任何中间层物质)。
5.加入RB2液350μl,充分颠倒混匀1min。
6.将混匀后的液体吸入或直接倒入内套管,离心1min。
7.弃去外套管中液体,内套管中加入500μl洗液,离心1min。
再重复此过程洗一次。
8.取出内套管,弃去外套管中液体,仍然套回内套管,不加洗液,离心1min。
9.将内套管移入新的eppendorf管中,在膜中央加入洗脱液(或pH>
7.0的DEPC处理水)25-50μl,室温静置1min,离心1min,获得总RNA。
注意事项
重要提示:
RB1具有强烈腐蚀性,操作时要戴手套和防护眼镜,最好在通风柜中进行,若不慎沾染,立即用大量清水冲洗,必要时到门诊处理。
离心速度均为12,000rpm-14,000rpm,室温离心(有条件可4℃离心)。
以eppendorf5417离心机为例,12,000rpm=13,362g,其它类型离心机转速应达到相近的g数。
首次使用时在洗液瓶中加入45ml无污染的分析纯无水乙醇,用后拧紧瓶盖。
氯仿自备。
避免环境中RNA酶污染,操作要戴手套,所有枪头和eppendorf管以DEPC水处理。
血液抽取后应在4小时内提取RNA。
冻存的血液RNA大部分丢失,不能用于提取。
尽量保证在膜中央加入洗脱液25μl-50μl,低于25μl将不能保证充分浸润吸附膜。
洗脱液pH<
7.0时会明显降低RNA的洗脱效率,而国内实验室用水大多呈偏酸性,自备洗脱液时应当注意。
本试剂盒提供的洗脱液为pH7.6。
*基因组DNA快速提取试剂盒
适用范