化学高三化学实验考前回顾文档格式.docx
《化学高三化学实验考前回顾文档格式.docx》由会员分享,可在线阅读,更多相关《化学高三化学实验考前回顾文档格式.docx(30页珍藏版)》请在冰豆网上搜索。
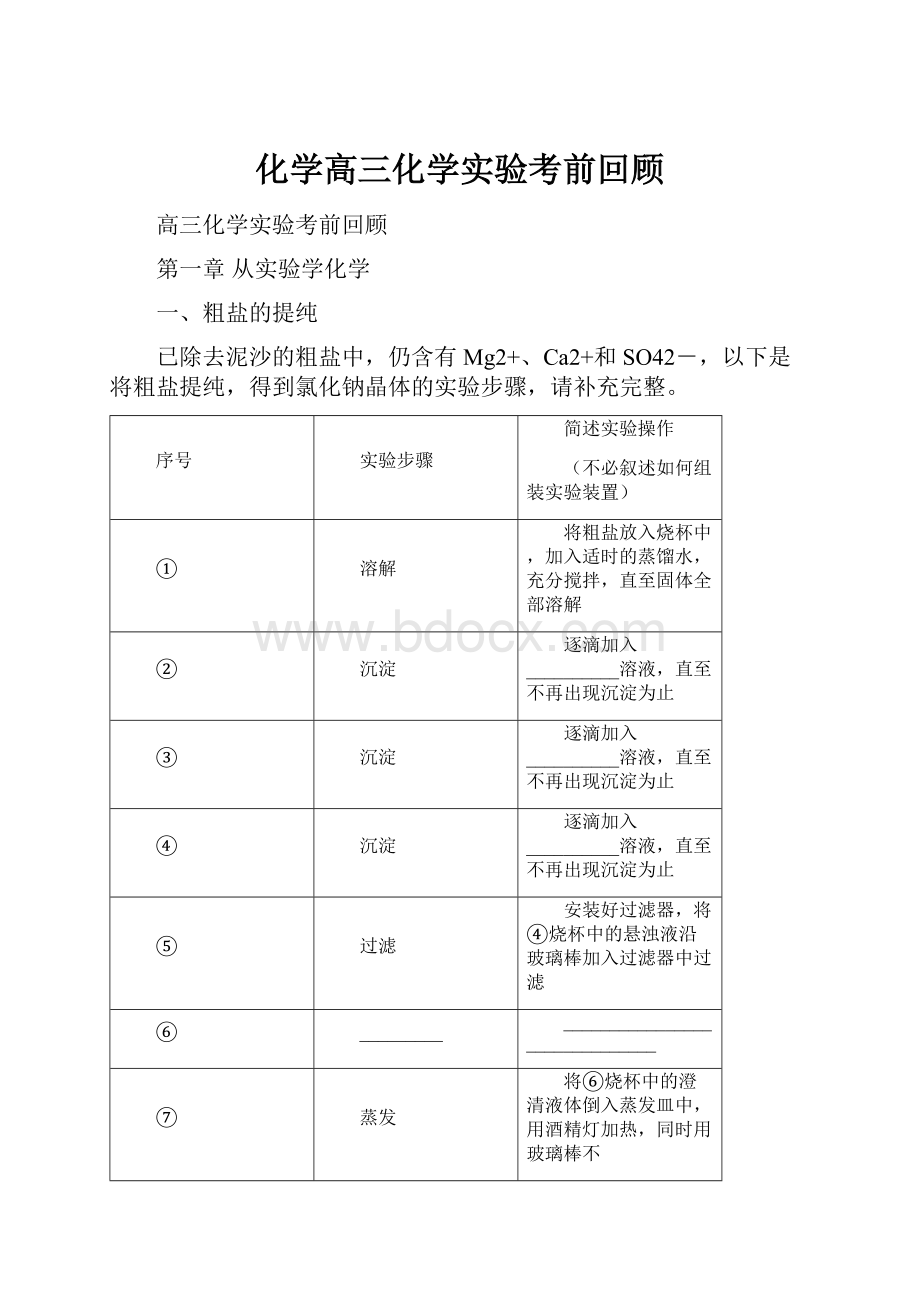
漏斗里的________要低于________。
倾倒液体的烧杯口要紧靠________;
玻璃棒末端要轻轻靠在________;
漏斗紧贴____________。
(2)蒸发溶液的操作应注意的问题:
蒸发皿内盛液量不应超过蒸发皿容积的________。
蒸发过程中要用________搅拌溶液,以免________________,溶液不能蒸干,当____________则停止加热,用________将其蒸干。
取、放蒸发皿应使用________。
试简述从FeCl3溶液中获得FeCl3固体的方法?
____________________________________
(3)甲同学在多次过滤后,发现烧杯中的滤液仍浑浊。
分析他操作不当的原因可能是①______
___________________________________,②______________________________________
(4)乙同学过滤后,滤液是澄清的,当取少量蒸发后的氯化钠晶体,溶于水,滴加硫酸钠溶液时,却出现白色沉淀。
分析乙在实验步骤设计上存在的问题可能是_________________
____________________________________________________________________________
二、蒸馏水的制取
蒸馏水制取原理:
利用杂质与水沸点的不同,除去难挥发或不挥发的杂质。
仪器和用品:
沸石,温度计,蒸馏烧瓶,石棉网,铁架台,酒精灯,冷凝管,接引管(牛角管),锥形瓶。
操作:
连接好装置,通入冷凝水,开始加热。
弃去开始镏出的部分液体,用锥形瓶收集约10mL液体,停止加热.
现象:
随着加热,烧瓶中水温升高至100度后沸腾,锥形瓶中收集到蒸馏水.
注意事项:
①温度计的水银球在_____________处。
②垫石棉网加热蒸馏烧瓶,蒸馏烧瓶中放少量碎瓷片……防
止__________。
③冷凝管中冷却水的流向:
从__________进,___________出。
④先打开冷凝水,再加热。
⑤液体量在容积的______________为宜,溶液不可蒸干。
三、萃取和分液
原理:
用一种溶剂把溶质从它与另一溶剂所组成的溶液里提取出来。
主要仪器:
分液漏斗,烧杯
步骤:
①检验分液漏斗是否漏水;
②量取10mL碘的饱和溶液倒入分液漏斗,注入4mLCCl4,盖好上口玻璃塞;
③用右手压住分液漏斗口部,左手握住活塞部分,把分液漏斗倒转过来用力振荡;
④将分液漏斗放在铁架台上,静置;
⑤待液体分层后,将分液漏斗的上口玻璃塞打开,从下端口放出下层溶液,从上端口倒出上层溶液。
①检验分液漏斗是否漏水。
②萃取剂的选择必须符合三个条件:
a.与_________互不相溶;
b.溶质在_________中的溶解度大于在_________中的溶解度;
c.与_________之间不能发生反应
③上层溶液从上口倒出,下层溶液从下口放出。
思考:
分液是实验室常见的基本操作之一。
(1)具有_______________的两种液体混合物可用分液的方法分离。
(2)某学生在一次分液操作中,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步出及判断依据。
_____________________。
四、一定物质的量浓度的溶液的配制
1.配制250mL0.5mol/LNaOH溶液(用固体NaOH配制)
(1)在下列仪器中:
A托盘天平;
B量筒;
C烧杯;
D玻璃棒;
E漏斗;
F500mL容量瓶;
G药匙;
H250mL容量瓶;
I胶头滴管;
J坩埚。
①需要用到的仪器有________________;
②称量NaOH固体时要注意用小烧杯盛放其在天平上进行称量;
③容量瓶使用前应_______,中学阶段常用仪器使用前须查漏的还有_____、_____;
④容量瓶上标有:
A温度;
B浓度;
C容量;
D压强;
E刻度线;
F酸式或碱式这六项中的__________。
(2)配制步骤为:
①_____;
②_____;
③_____;
④_____;
⑤_____;
⑥_____;
⑦_____。
(3)下列操作对所配制的NaOH溶液浓度有何影响?
(选填“偏高”、“偏低”、“无影响”)
①在烧杯中溶解时,有少量液体溅出_____;
②没有用水冲洗烧杯2~3次_____;
③定容时,俯视液面使与刻度相切_____;
④溶液配好摇匀后,发现液面低于刻度线,又加水至液面与刻度相切_____;
⑤将未冷却的溶液注入容量瓶后,马上定容_____;
⑥样品中混有Na2O杂质_____;
2.实验室用98.0%的密度为1.84g/mL浓H2SO4来配制100mL1.00mol/LH2SO4。
某学生操作步骤如下:
A、计算需量取该种浓硫酸的体积;
B、检查100mL容量瓶是否漏水;
C、量取浓硫酸;
D、在容量瓶中先加入少量水,然后将量取的浓硫酸缓缓注入容量瓶中,并用玻璃不断搅拌;
E、再将蒸馏水注入容量瓶,至液面接近标线1~2cm时,改用滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻度线相平;
F、盖紧瓶塞,反复颠倒,摇匀溶液。
请回答了列问题:
(1)请你计算A中所需浓硫酸的体积为_____________mL。
(2)进行C步操作时,应选用下列量器中的____________。
a.50mL量筒b.25mL碱式滴定管c.25mL酸式滴定管
(3)上述步骤中_________有错,正确的操作应是__________;
(4)在C步操作时,若某同学初读数时方法正确,末读数时俯视刻度线,则最终所配溶液浓度_____(偏高、偏低或无影响)
(5)用配制好的溶液,再来配制50mL0.2mol/L的硫酸,需量取原配好的溶液____mL。
3.欲粗略配制1.0mol/LNaOH溶液100mL,下列操作方法不正确的是_____;
A.量取2.0mol/LNaOH溶液50mL置于烧坏中,加50mL水,搅拌混合均匀
B.量取2.0mol/LNaOH溶液33mL置于烧杯中,再加入0.5mol/LNaOH溶液67mL,搅拌均匀
C.称取40gNaOH置于烧坏中,加100mL水,搅拌使之完全溶解
D.称取4.0gNaOH置于量筒中,加100mL水,搅拌使之完全溶解
4.某研究性学习小组欲用化学方法测量一个不规则容器的体积。
把35.1gNaCl放入500mL烧杯中,加入150mL蒸馏水。
待NaCl完全溶解后,将溶液全部转移到容器中,用蒸馏水稀释到完全充满容器。
从中取出溶液100mL,该溶液恰好与20mL0.100mol/LAgNO3溶液完全反应。
则该容器的体积易计算可知为_________L。
第二章化学物质及其变化
一、Fe(OH)3胶体的制取、胶体的性质
1.实验室制取Fe(OH)3胶体溶液的方法是_______________________________________;
其间发生的化学反应的方程式可表示为_______________________________________;
用__________方法除去胶体中的浑浊;
根据_______________现象证明胶体已经制成;
用__________方法精制胶体;
如何用实验方法证明胶体和Cl-两者已经分离________;
二、电解食盐水的实验室装置*
1.请从下图中选出必要装置进行电解食盐水实验。
要求准确测量产生氢气的体积(氢气的体积小于25mL),并通过实验证明生成的气体是氯气。
(1)铁棒A、炭棒B应分别与电源的________极、________极相连接。
(2)请选用上图所示的仪器,设计出实验装置,并根据所设计的实验方案,将接口连接顺序用字母表达出来_____________A-B_____________。
(3)实验中生成5.6mL氢气时(标准状况下),U形管内50mL溶液的pH值约为__________。
三、铁的电化腐蚀探究(鲁教版)
1.某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如右图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示。
时间/小时
0.5
1.0
1.5
2.0
2.5
3.0
A瓶(盛干燥铁丝)
B瓶(盛沾了食盐水的铁丝)
0.4
1.2
3.4
5.6
7.6
9.8
C瓶(盛沾了清水的铁丝)
0.3
0.8
3.5
D瓶(盛完全浸没在食盐水中的铁丝)
(1)导管中水面为什么会上升?
___________________________________________________。
(2)上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧杯号):
________________;
(3)影响铁生锈的因素有:
_______________________________________________________。
四、离子反应的实质证明性实验(鲁教版)
实验目的:
使用中学常用实验器材,试设计一个实验证明Ba(OH)2与H2SO4在溶液中的反应是离子反应。
要求作出有关实验原理、过程、现象的说明。
实验装置:
见右图。
实验原理:
根据溶液的导电性与单位体积内离子总数成比例和溶液在
不同反应阶段表现出不同导电性能,来证明溶液中自由移
动的离子浓度的变化,从而证明反应是离子反应。
实验方法:
利用测定导电能力的装置,在烧杯中先加入Ba(OH)2溶液,再一边不断滴入H2SO4,一边适时地轻轻摇荡。
实验现象:
_____________________________________________________________________。
1.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
__
___________________________________________________________________________
___________________________________________________________________________。
2.在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:
_______
___________________________________________________________________________
第三章金属及其化合物
一、Na的性质
1.金属钠可用小刀切割,因为__________,其断面________________________________,
但金属表面很快变暗,这是因为______________________________________________,
其原理用化学方程式表示为__________________________________________________。
注;
使用剩余的药品不允许再放回原试剂瓶,但钠、钾、白磷等须放回原试剂瓶。
2.将一小块钠投入一盛有水的烧杯中,发生下列现象,请说明原因:
①钠浮在水面上__________________________________________________________;
②钠与水剧烈反应并熔成一个闪亮的小球____________________________________;
③小球在水面上四处游动__________________________________________________;
④反应后在溶液中加几滴酚酞溶液,溶液变红________________________________;
⑤写出钠与水反应离子方程式______________________________________________,
其中_____是氧化剂,____元素被还原,NaOH是_____产物。
3.用右图的实验装置可以进行钠跟水的反应实验,并可收集、检验生成的气体。
Na的密度为0.97g/mL,煤油的密度为0.87g/mL,请回答下列问题:
(1)液体物质添加完毕后,关闭活栓,打开右边胶塞,向煤油中加入一小
块钠,立即塞好胶塞,反应开始前钠的位置在____处(填a、b、c);
(2)反应后,钠在煤油层和水层界面之间上下跳动,反应平缓连续进行。
试说明产生上述现象的原因:
_________________________________;
(3)装置中的漏斗在反应过程中的主要作用是_______________________;
(4)本实验除能使反应平缓连续进行、收集并检验气体外,还有一个优点是_________。
这是因为_______________________________________________________________________。
二、过氧化钠的性质(鲁教版)
1.高中化学有一个经典的演示实验,用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂上滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a:
有氧气生成;
b.____________。
(2)写出Na2O2和H2O反应的化学方程式并标明电子转移数目:
____。
(3)某学校研究性学习小组拟用右图装置进行实验,以证明上述结论。
①用以验证结论a的实验操作方法及现象是:
___________________________________;
②用以验证结论b的实验操作方法及现象是:
___________________________________。
三、碳酸钠和碳酸氢钠的性质
1.高中教材中有这样一个实验:
在两支试管中分别加入3mL稀盐酸,将两个分别装有0.3gNaHCO3、0.3gNa2CO3粉末的小气球分别套在两支试管口。
将气球内的NaHCO3、Na2CO3同时倒入试管中,观察到现象如下:
①试管中(填产生沉淀或气体及反应速率等相关现象)______________________________;
②两试管中气球大小(包含试管)体积之比约为(填最简单整数比)(盐酸均足量)_______;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度有升高。
由此他得出:
不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。
类似如中和热,甲同学写出了下列热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3-(aq)+H+(aq)=H2O(l)+CO2(g),△H>
0;
CO32-(aq)+2H+(aq)=H2O(l)+CO2(g),△H<
甲下结论的方法是否正确。
______(填正确或不正确)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
试剂1
试剂2
混合前温度
混合后最高或最低温度
50mL水
2.5gNaHCO3固体
20℃
18.5℃
3.2gNa2CO3固体
23.0℃
35mL稀盐酸
含2.5gNaHCO3的饱和
溶液15mL
18.8℃
含3.2gNaCO3的饱和
溶液15ml水
20.6℃
50mL稀盐酸
17.4℃
3.2gNa2CO3固体,
23.5℃
请你帮助填写相关内容:
①该研究报告的题目是《____________》;
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为_______和_______;
通过上述实验可得出多条结论,如:
a:
NaHCO3的溶解是_________(吸热或放热)过程;
b:
Na2CO3的饱和溶液和盐酸的反应是____(吸热或放热)反应;
c:
NaHCO3固体与稀盐酸反应的反应热约是______的热效应之和。
2.在0.5mol/L纯碱溶液中滴入酚酞试液变红,若在该溶液中再逐滴滴入过量BaCl2溶液,所观察到的现象是_____________________________;
其原因是(用离子反应方程式和简要文字说明):
__________________________________________________________;
3.甲、乙两学生同时加热滴有酚酞的小苏打溶液(粉红色),甲学生加热时,溶液红色变深,冷却到室温时又变回粉红色。
乙学生加热后,红色也变深,冷却到室温,红色稍变浅但变不到原粉红色,其原因可能是:
_____________________________________________。
四、铝及其化合物的性质
1.铝与氧气的反应
实验现象
解释与结论,或反应方程式
在空气中
在氧气中
把一小段铝箔的一端固定在粗铁丝上,另一端裹一根火柴。
点燃火柴,待火柴快燃尽时,立即把铝箔伸入充满氧气的集气瓶中(集气瓶底部要先放一些细沙),观察现象
2.把铝放入过量的NaOH溶液中,发生反应的离子方程式为_________________________。
若向反应后的溶液中通入足量的CO2气体,出现的现象是__________________________;
若向反应后的溶液中滴加盐酸,看到的现象是____________________________________。
五、铁及其化合物的性质
1.将铁粉溶于足量稀酸后,所得溶液分装在A、B、C三试管中:
(1)在A试管中滴加双氧水,然后滴入KSCN溶液,溶液呈红色,反应的离子方程式___________________________________、_____________________________。
(2)在B试管中滴入KMnO4溶液,溶液紫色褪去,反应的离子方程式是:
___________。
(3)在C试管中滴入KSCN溶液,然后在空气中放置片刻后,溶液又显红色,反应的离子方程式是________________________________________________________________。
2.在烧制砖瓦时,用粘土做成的坯经过烘干烧后,铁的化合物转化成_______而制得红色砖瓦。
若烘烧后期从窑顶向下浇水,窑内会产生大量的__________气体,它们把该红色物质还原成黑色的化合物是___________,同时还有未烧完的碳颗粒,而制得青瓦砖。
3.铁与水蒸气的反应实验设计:
在如图所示的装置中,试管里依次放入了湿棉花和还原铁粉,
加热试管,将生成的气体通入蒸发皿中的肥皂液中,一段时
间后,用坩埚钳夹取火柴点火,观察现象。
现象与解释:
(湿棉花在受热时提供了与铁反应的水蒸气)红热的铁与水蒸气反应放出的气体,使得蒸发皿中产生大量的肥皂泡,点燃放出的气体,能够燃烧(甚至爆鸣),(可知有氢气生成)而试管内固体仍为黑色,但已是Fe3O4。
反应方程式为____________________
_____________________________________。
第四章非金属及其化合物
一、硅及其化合物的性质
1.为确认CH3COOH、H2CO3和H4SiO4的酸性强弱,有人设计用如图装置,一次实验即可达到目的(不必再选用其它酸性溶液)。
请依据此实验填空:
(1)锥形瓶内装某可溶性正盐固体,分液漏斗中所盛试剂是________。
(2)装置B所盛的试剂是______________________________________;
装置B所盛试剂的作用是__________________________________。
(3)装置C中所盛的试剂是____________;
出现的现象是__________________________。
2.将一小木条或滤纸条在水中反复浸透后,放在酒精灯外焰加热。
现象如何?
________。
将一小木条或滤纸条在硅酸钠溶液(或市售的水玻璃)中反复浸透后,放在酒精灯外焰加热。
__________________________________________________________。
3.滴有酚酞的饱和硅酸钠溶液呈________色,若往该溶液中逐滴滴入6mol/L的盐酸,现象是_______________,用离子反应方程式加以解释:
______________________________。
二、氯及其化合物的性质
1.在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。
进行此实验,所用仪器如下图:
(1)连接上述仪器的正确顺序是(填各接口处的字母):
____接____,____接,____接____,____接____。
(2)在装置中:
①饱和食盐水起的作用是________,②浓硫酸起的作用是______________。
(3)如果将过量二氧化锰与20mL12mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①___________________;
②____________________________。
(4)为了提高浓盐酸的利用率,你对实验的建议是:
①____________;
②_______________。
(5)化学实验中检验是否有Cl2产生