中考化学模拟试题Word文件下载.docx
《中考化学模拟试题Word文件下载.docx》由会员分享,可在线阅读,更多相关《中考化学模拟试题Word文件下载.docx(42页珍藏版)》请在冰豆网上搜索。
6•图1中甲、乙、丙、丁表示相邻两物质相互混合过程中溶液酸碱度的变化,其中可能符合图2所示变化关系的是()
图1團2
A.甲
B.乙
C.丙
D.T
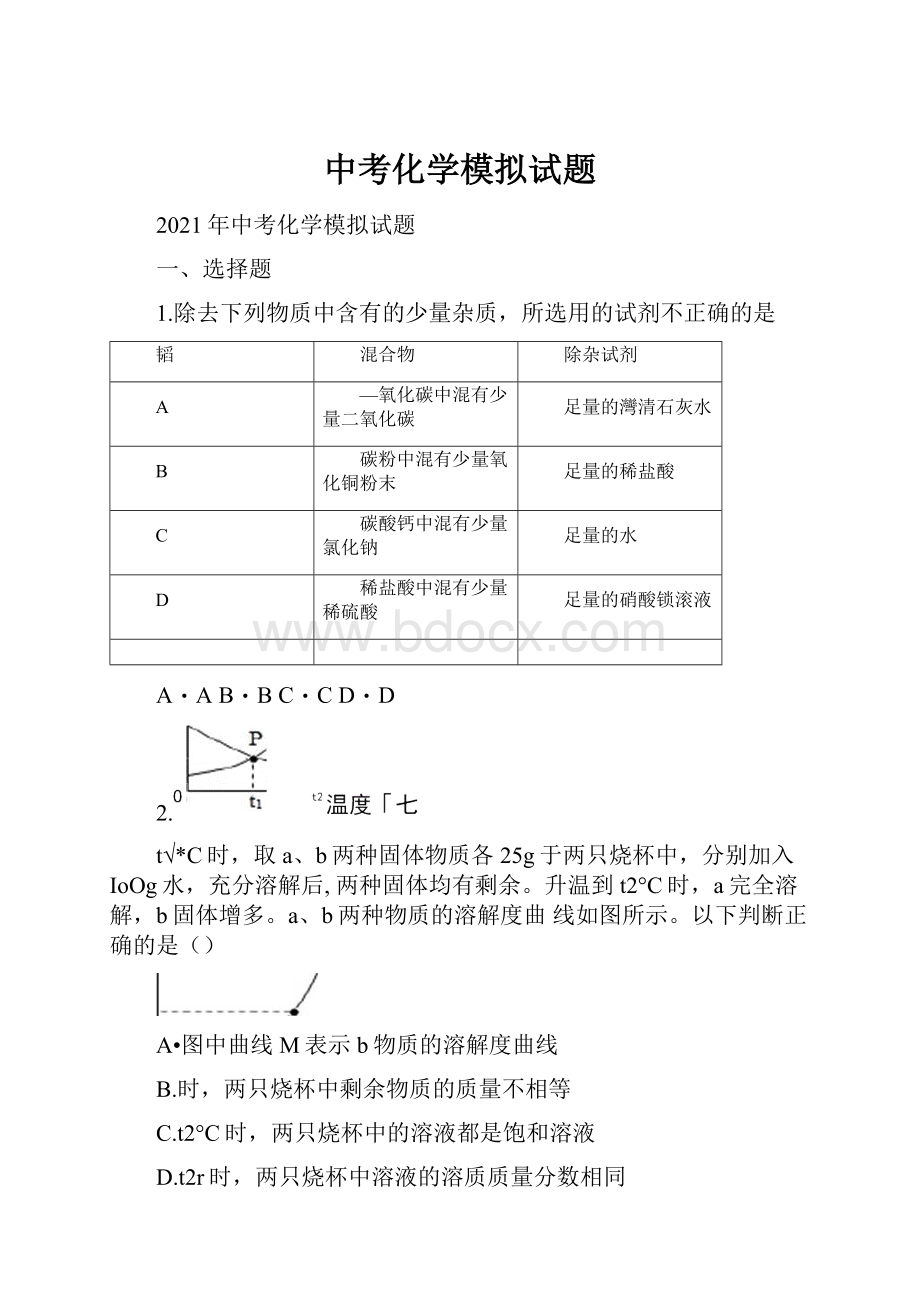
7.如图是A、B、C三种固体物质的溶解度曲线,下列分析正确的是()
A.20C时等质量的A和C两种物质的溶液中溶质的质量相等
B.50°
C时把50gA放入IOog水中能得到A的饱和溶液,英溶质质量分数为50%
C.将50°
C时A、B、C三种物质的饱和溶液都降温至20°
C时,这三种溶液的溶质质量分数的大小关系是B>
A=C
D.将C的饱和溶液变为不饱和溶液,可采用降温的方法
8.在硝酸银、硝酸铜的混合溶液中加入一泄量锌粉,反应停止后过滤,滤液仍为蓝色,有
关判断正确的是()
A.滤渣中一定有银、没有铜和锌B.滤渣中一定有银和锌,可能有铜
C.滤液中一泄有硝酸锌、硝酸铜、硝酸银D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
9.下表除去杂质的方法中,正确的是
选项
物质(括号内为杂质)
除去杂质的方法
Cu(NO3)2溶液(AgNO3)
加过量铜粉,过滤
KCl溶液(CaCI2)
加适SNa2C03溶液,过滤
Fe(Zn)
加足量稀盐酸,过滤
CO(CO2)
通过灼热的氧化铜粉末
10.(2012年山东烟台,18题,2分)电影《黄金大劫案》上映后,里而用"
王水"
(浓盐酸与浓硝酸的混合液)溶解黄金的情引起了广泛的热议。
黄金溶解在"
中形成HAUal
(四氯合金酸),没有氢气产生。
根据以上信息,下列有关说法正确的是()
①"
王水”溶解黄金是化学变化:
②金比氢活泼;
③HAUCI4中,AU的化合价为+3价:
④可以将PH试纸伸入“王水"
中测其酸碱度:
⑤"
可以用铁质容器盛装。
A.①④⑤B-①②③C.③④⑤D.①③
11.下列图像不能正确反映对应变化关系的是
钙7CaO
A.密ZCa(OH)2向等质量的氧化钙、氢氧化钙中分別加入等质量分数的稀
0稀盐酸的质量g
盐酸至过量
向一左质量氮化亚铁和氯化铝的混合溶液中加入镁粉至过疑
向等质量的镁、铝中分别加入等质咼分数的稀硫酸至过童
0稀硫酸的质量塔
12.下列0组物质的溶液,不用英他试剂没,仅通过观察和用组内溶液相互混合的方法,
不能将其逐一鉴别出来的是()
A.NaOHCa(OH)2HClNa2CO3B.KClBa(NO3)2CuSO4NaOH
C・AgNO3HClNa2CO3CaCl2D・Ba(OH)2KClNa2SO4Na2CO3
13.往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是()
A・a至b段有蓝色沉淀生成
B.d点溶质种类为三种
C.C至d段,溶液PH不断减少
D.C点所含的溶质种类最少
14.某白色固体A,含有K2SO4、NaOH.CaeO3、BaCb中的一种或几种,取少:
⅛A进行如下实验。
注:
BaSO4难溶于盐酸;
K2SO4.BaCb的水溶液均呈中性。
据此实验可知,固体A中的物质最多有
A.1种B.2种C.3种D.4种
15・下图所示的四个图像,能正确反映对应变化关系的是
O换晓曲偵%”∙>
∣<
J⅛ΛΛ的质*l⅛∏&
朋統的JfckU•反QBfIhIAI*
ABCD
A.电解水一段时间
B.向二氧化锈中加入一立质量的过氧化氢溶液
C.向一定质量铁粉中加入硫酸铜溶液
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
16.下列物质提纯或除杂所用试剂和分离方法正确的是
分离方法
Ca(OH)2(CaCO3)
HCI溶液
溶解、过滤
NaCI(Na2SO4)
适量BaCI2
吸附
KCl(MnO2)
H2O
溶解、过滤、蒸发、结晶
SO2(HCI)
NaOH
洗气
A.AB・BC・CD・D
17.下列有关实验的分析中,合理的是
A.测碱溶液的PH结果偏小一一直接把试纸伸入待测液中
B.用KMnO4制氧气时试管炸裂一一在试管口没有放一团棉花
C.粗盐提纯实验后所得产率偏低一一蒸发时有一些液体、固体溅岀
D.用6%NaCl溶液加水配制3%NaCl溶液结果偏小一一量筒量取水的体积时俯视读数
18.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是
:
厂0丙
•∙I
1■■」
Qh(2bi⅛度/C
A.t『C时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:
甲>乙
B.将tj°
C时甲、丙的饱和溶液升温到t2°
C,两种溶液中溶质的质疑分数相等
C.将t2°
C时甲的饱和溶液变为t3°
C时甲的饱和溶液,可以采用蒸发水的方法
D.将t3°
C时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:
甲>乙>丙
19.下列物质能在pH=13的无色溶液中大量共存的是()
A.HClXAgNO3、Na2CO3B.NaNO3xKNO3、NH4CI
C.K2SO4xK2CO3xNaOHD.KMnOdxCUSO4、NaNO3
20.
相同质量的M、N两种活泼金属,分别与足疑质量分数为8%的盐酸反应(M、N在生成物中均为+2价),生成出质量和反应时间的关系如图。
下列叙述正确的是()。
反应时间
A.金属的活泼性N>
M
B.两个反应生成H2的体积相等
C.相对原子质⅛Λr>
D.两个反应消耗盐酸的质⅛-⅛相等
21.下列方法能达到除去杂质目的的是
物质
所含杂质
铜粉
木炭粉
在空气中灼烧
二氧化碳
水蒸气
通过足量的氢氧化钠固体,干燥
氯化钾
碳酸钾
加适量的稀盐酸,蒸发结晶
硫酸亚铁溶液
硫酸铜溶液
加入少量铁粉过滤
A.AB・BC・CD・D
22.有一包白色粉末,可能含有MgSO4、Na2SO4.K2S0d.CUSO“NaOH.BaCJ中的一种或几种。
某化学兴趣小组对这包白色粉末的成分展开如下探究:
[査阅资料]氯化顿溶液显中性。
步骤
(1):
取13g白色粉末,投入50g水中,搅拌,得到无色溶液。
步骤
(2):
向
(1)所得溶液中加入IOOg足量的Ba(NO3)2,得到白色沉淀,过滤得滤液质疑139,7g.
结合以上探究过程,下列推理正确的是()
A.白色粉末一定是纯净物
B.白色粉末中至少含Na2SO3K2SO4XNaOH中的某一种或几种
C.白色粉末中至少含Na2SO4K2SO4中的某一种
D.白色粉末中一泄不含CuSO4和BaCl2,可能含有NaOH
23.
根据实验操作所绘制的图象中,正确的是()
量关系
余体质∙∙*g剩固的量氏
质量Zg氯化钠的
用一左量的一氧化碳和氧化铁反应,剩余固体质量与反应时间的
向等质虽的金属镁和铝中加入足量且质量分数相等的稀硫酸,
生成氢气的质量与加入稀硫酸质量的关系
向久置空气中NaOH溶液中加入盐酸,生成氯化钠质量与加入
0盐酸体积曲L
盐酸的体积关系
24・向一立质量的Na2S0α.MgSO4混合溶液中先后滴加150.0g3.42%的稀Ba(OH)2溶液、
100.0g稀H2SO4,产生沉淀的质量与滴加的溶液质量关系如图所示。
下列说法不正确的是
A.m=5.24
B.a点沉淀的成分为两种
C.所用稀H2SO4的质量分数为3.92%
D.向e点所得溶液中滴加紫色石蕊试液,溶液呈红色
25.下列实验操作中不能达到实验目的的是
••
实验目的
实验操作
鉴别NaCI和NHtNoS固体
分别加少量水溶解
鉴别NaOH溶液和澄淸石灰水
分别通入二氧化碳
除去ZnSoI溶液中混有的少量CuSO:
加入足量的锌粉,充分反应后过滤
除去KoS(λ溶液中混有的少虽KOH
加入适量的稀盐酸
A.AB.BC.CD.D
二、实验题
26.小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固泄在橡胶塞上,迅速塞紧,装垃如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)O当温度恢复至室温,且量筒内水面髙度不变时读数(此时瓶内氧气含量近似为零)。
记录起始和最终量简的读数以及所需时间如表。
序号
样品
⅛筒起始读数∕mL
量筒最终读数∕mL
所需时间
∕min
1
Ig铁粉、0.2g碳和10滴水
100
70
约120
2
Ig铁粉、0.2g碳、10滴水
和少量NaCl
约70
3
约480
一温度计
包有样品的滤纸包
(1)实验①和②说明NaCl可以铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是(填“放热”或
"
吸热”)过程。
(3>实验结朿后取岀滤纸包,观察到有红棕色物质生成,该物质的化学式是O
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据讣算氧气的体积含量是
(小数点后保留1位)。
27.
某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分別用A〜H编号后,做如下实验:
(I)试验中观察到有气泡出现的试管是•有沉淀生成的试管是
(2)写出实验中无明显现象产生的试管中发生反应的化学方程式o
(3)试验后某试管中为红色溶液,当向其中加入过量的后,溶液变为蓝色。
由
此推断,该试管中最初盛有的物质是.
(4)试验后某试管的底部有白色固体,过滤后向过滤液中滴加盐酸,一段时间后有气泡冒
出,由此推断,该试管中最初发生反应的化学方程式:
”
(5)试验后某试管中只得到无色溶液,向英中加入足量的Na2CO3溶液,无明显现象。
由此
推断,该试管中最初发生反应的化学方程式O
28・某化学兴趣小组用下图所示装置进行实验(装置的气密性良好)。
(1)如图所示,让瓶内充满二氧化碳气体,先向广口瓶中加入A的溶液,振荡广口瓶,气球膨胀;
再向广口瓶中滴加B中的溶液,振荡广口瓶,气球又缩小,如此重复操作,气球可以反复膨胀和缩小。
贝叽
1分液漏斗A中可能是溶液,反应的化学方程式是
2分液漏斗B中可能是溶液。
(2)如图所示,将滴管甲中的液体挤出,气球明显鼓起,一段时间后恢复原状:
再将滴管
乙中的液体挤岀,气球有明显鼓起且不恢复原状。
则滴管甲、乙和烧杯①、②中的物质可能是(填字母序号)。
29.
在髙效复习课堂中,同学们利用"
盐酸、硝酸钙、氢氧化钠、碳酸钠”四种物质的溶液对"
复分解反应发生的条件”进行再探究.
(知识回放)通过判断上述四种溶液两两之间能否发生反应,若能写出英中符合下列条件的两个化学方程式:
(!
)_个中和反应:
②一个有沉淀生成的反应O
(挖掘实质)
1图1是HCl和NaOH在水中解离出离子的示意图,小丽发现HCl任水中会解离出H+和Cl'
NaOH在水中会解离岀Na+和0H-,以此类推硝酸倾在水中会解离出的离子是(填
离子符号)。
2图2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以
表示为H÷
+0H∙=H2O,我也能用同样的方式表示上述四种溶液两两之间发生反应时有气体生成的反应的实质°
(实践运用)
1通过上述探究发现,在溶液中屮和OH-不能大量共存,我还发现在溶液中和(填
离子符号)也不能大量共存。
2利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液,经
测泄,该溶液显酸性,则在该溶液中一泄含有的离子是。
30.母亲节前夕,阳阳对妈妈给外婆购买的"
XX牌"
苏打饼干及其配料表产生了浓厚的兴趣.在化学课上,阳阳听老师说过,苏打是碳酸钠(NazCOJ)的一个俗爼,她再仔细阅读该饼干的配料表如下:
小麦粉、小苏打•••.她思考:
配料中小苏打有何作用?
如何鉴别苏打(Na2CO3)和小苏打(NaHcO3)?
下面是阳阳进行的研究性学习过程,请你参与并回答相关问题.
(资料获悉)
(1)相同条件下,Na2CO3溶液比NaHCO3溶液的碱性强:
(2)20oC时,Na2CO3^NaHCO3的溶解度分别为21.3g和9.6g:
(3)NaHCo3在270OC时能发生如下分解反应:
2NaHC03加热Na2CO3+H2O+CO2个,而Na2CO3受热不易分解.
(实验过程)
实验一:
验证Na2CO3和NaHCO3热稳泄性的差异.在老师的指导下,你们按如图所示进行实验若实验现象为,则能得出NaHCO3受热易分解,Na2CO3受
热不易分解.
实验二:
用酸碱度的差异鉴别Na2CO3和NaHCO3.你们若用广泛PH试纸测泄相同条件下两种溶液的pH,则PH较大的是.
实验三:
用20°
C时溶解度的差异鉴别Na2CO3和NaHCO3
请完成下表:
(忽略溶解过程中热量的变化)
预期的现象和结论
(3)
(4)
(交流总结)
(1)配料中小苏打主要起发泡作用.
(2)可以通过溶解度、酸碱度等差异来鉴别NazCOMHNaHCO3.
通过上述研究性学习过程.你们认为小苏打(NaHCO3)除用于食品工业外,在日常生活及
实验室中还有哪些应用,试举一例:
.
31.请你参与下列探究:
【问题情景】在课外活动中,小斌按照课本实验(见图1)探究微粒的性质时,闻到了刺
激性的氨味,于是,小斌在老师的指导下,设计了如图2的实验装巻,进行同样的实验,
结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论。
【实验探究与结论】小斌用图2装置进行实验。
(1)滴入少量浓氨水后,湿润的酚酥滤纸条发生的变化是:
从微观角度分析,Ilt
现象可说明的结论是。
(2)"
图2的实验装置,快速出现实验现象"
说明固体氢氧化钠遇到浓氨水时可能会(填"
放热”或"
吸热"
)。
(3)和课本实验比较,小斌改进后的装垃的优点是(写出两点)
①:
②O
【思维拓展】小媚受小斌实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质。
(1)打开活塞K滴入稀盐酸后,小试管中发生的反应的文字表达式为,发现两条
用紫色石蕊试液润湿的试纸都变红,请你分析两条试纸变红的情况是—。
A.下而先变红,上而后变红B.上而和下而一起变红
C.上而先变红,下而后变红D.以上均有可能
小媚从课本实验中知道,二氧化碳和水本身都不能使石蕊变色,因而她认为以上两个变化可验证的二氧化碳的性质是、。
(2)小柔认为小媚的装置还可以验证:
①二氧化碳能使澄淸石灰水变混浊:
②二氧化碳
不能燃烧,也不支持燃烧。
小柔为完成自己的两个验证实验,对小媚的实验进行的简单改进:
验证①、验证②o
【参考答案】试卷处理标记,请不要删除
1.D
解析:
【解析】A、二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,而一氧化碳不反应,能成功除杂,不符合题意:
B、氧化铜和盐酸反应生成氯化钙和水,碳和盐酸不反应,能成功除杂,不符合题意;
C、碳酸钙难溶于水,而氯化钠易溶于水,加水充分溶解后固体只有碳酸钙,能成功除杂,不符合题意:
D、硝酸领和硫酸反应生成硫酸倾沉淀和硝酸,会在盐酸中引入新的杂质,不能达到除杂目的,符合题意:
选D
2.C
【解析】
【分析】
根据固体的溶解度曲线可以:
①查岀某物质在一立温度下的溶解度,从而确龙物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【详解】
A、升温到t2°
C时,a完全溶解,b固体增多,所以b物质的溶解度随温度的升高而减小,a物质的溶解度随温度的升高而增大,所以图中曲线M表示a物质的溶解度曲线,错误;
B、tfC时,a、b物质的溶解度相等,所以tl°
C时,取a、b两种固体物质各25g于两只烧杯中,分別加入Ioog水,充分溶解后,两种固体均有剩余,两只烧杯中剩余物质的质量相等,错误;
C、升温到t2C时,a完全溶解,b固体增多,所以t2°
C时,两只烧杯中的溶液都是饱和溶液,正确:
D、tl°
C时,取a、b两种固体物质各25g于两只烧杯中,分別加入IOog水,充分溶解后,两种固体均有剩余,升温到t2。
C时,a完全溶解,b固体增多,t2°
C时,溶剂质量相等,溶质质量不相等,所以两只烧杯中溶液的溶质质量分数不相等,错误。
故选C。
3.B
A、根据图示可以看岀反应过程中温度升高,即有热量放岀。
故A不符合题意;
B、50s时压强不变,50〜10OS时压强逐渐变大,说明此时间为稀盐酸和铝的反应,因此50s时溶液中溶质是氯化铝和氯化氢。
故B符合题意:
C、0〜50s时容器内压强不变,发生的是氧化铝和稀盐酸的反应,二者反应生成水和氯化铝,没有气体参加或生成,所以压强不变。
故C不符合题意;
D、约IooS时压强、温度都达到了最大值,说明反应完全,IOO-150s时压强减小是因为反应结束,温度逐渐降低。
故D不符合题意。
故选B。
4.C
A、气体的溶解度随着温度升髙而减小,随着压强增大而增大,图像与事实相符,故A正确:
B、氧化锌和稀盐酸反应生成氯化锌和水,氢氧化锌和稀盐酸反应生成氯化锌和水,反应的
分別加入等质量分数的稀盐酸至过量时,反应的盐酸质疑相等时,生成氯化锌质量相等,最终氧化锌和盐酸反应生成的氯化锌质量大,图像与事实相符,故B正确:
C、氯酸钾分解生成氯化钾和氧气,生成氯化钾和氧气的时间应该相同,图像与事实不相符,故C错误:
D、向一立量的氢氧化钠溶液中加入足量的水,溶液的PH会逐渐降低至无限接近于7,但不会低于7,图像与事实相符,故D正确。
【点睛】
本题是一道图像坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,确定正确的图像。
5.B解析:
t**C时,Na2CO3溶解度为Ag,现有饱和Na2CO3溶液(100+A)g,溶质质量分数为a%:
向该溶液中投入无水碳酸钠Ag,静置后析岀碳酸钠晶体(Na2CO3-IOH2O)Bg:
加水使晶体全部溶解,所得溶液质量分数为a%,说明所得溶液还是该温度下的饱和溶液,所以就相当于计算该温度下溶解Ag无水碳酸钠所需要的水的质量,该温度下,Na2CO3溶解度为Ag.说明加入IOOg水该温度下正好饱和,所以加入水的质量为IOOg,故选B∙,
6.D
A、甲是碳酸钠溶液和氢氧化钙溶液混合,反应后溶液呈碱性,不符合题意;
B、乙是碱性的碳酸钠溶液中加入水,溶液的碱性逐渐变弱,但不会变为酸性,不符合题意:
C、丙是酸性的硫酸溶液和水混合,溶液的酸性减弱,PH增大,原来的硫酸溶液PH也应小于7,不符合题意;
D、硫酸溶液加入氢氧化钙溶液中,溶液的PH由大于7逐渐减小,硫酸过量,PH小于7,符合题意。
故选D。
7.D
A.20C时,A和C的溶解度相等,等质量的A和C两种物质的饱和溶液中溶质的质量相等,此选项错误;
C时,A的溶解度是50g,把50gA放入Ioog水中能得到A的饱和溶液,其溶质质量
50g
分数为:
J—×
100%≠50%,此选项错误:
50g+100g
C.A、B两种物质的溶解度随温度的降低而减小,20C时,A、B两种物质的溶解度大小关系是B>
A,所以将50C时A、B、两种物质的饱和溶液都降温至20。
C时,溶质质量分数的大小关系是B>
A。
C的溶解度随温度的降低而增大,将50°
C时C的饱和溶液降温至20°
C时,C溶液的溶质质量分数不变,由于20。
C时A的溶解度大于50C时C的溶解度,所以50°
C时A、B、C三种物质的饱和溶液都降温至20C时,这三种溶液的溶质质量分数的大小关系是B>
A>
C,此选项错误:
D∙C的溶解度随温度的降低而增大,将C的饱和溶液变为不饱和溶液,可采用降温的方法,此选项正确。
在溶解度曲线上,溶剂的质量都是100g,所以分析溶质的质星分数时,只需要比较溶质的多少即可,溶解度变大时,溶质不变,溶解度减小时,溶质质量等于减小后的溶解度。
8.D
A、锌先与硝酸银发生置换反应生成硝酸锌与银,所以滤渣中一泄有银,反应后的滤液显蓝色,表明滤液中仍含有硝酸铜,锌可能与部分硝酸铜反应,也有可能没有与硝酸铜反应,所以滤渣中可能含有铜,也可能不含铜,滤渣中一左没有锌,否则会继续和硝酸铜反应,选项错误:
B、锌先与硝酸银发生苣换反应生成硝酸锌和银,所以滤渣中一定有银,滤液仍为蓝色,表明滤液中有硝酸铜的剩余,说明锌可能与部分硝酸铜反应,有可能没有