北京中考化学一模汇编物实验原理分析科学探究学案Word格式文档下载.docx
《北京中考化学一模汇编物实验原理分析科学探究学案Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《北京中考化学一模汇编物实验原理分析科学探究学案Word格式文档下载.docx(16页珍藏版)》请在冰豆网上搜索。
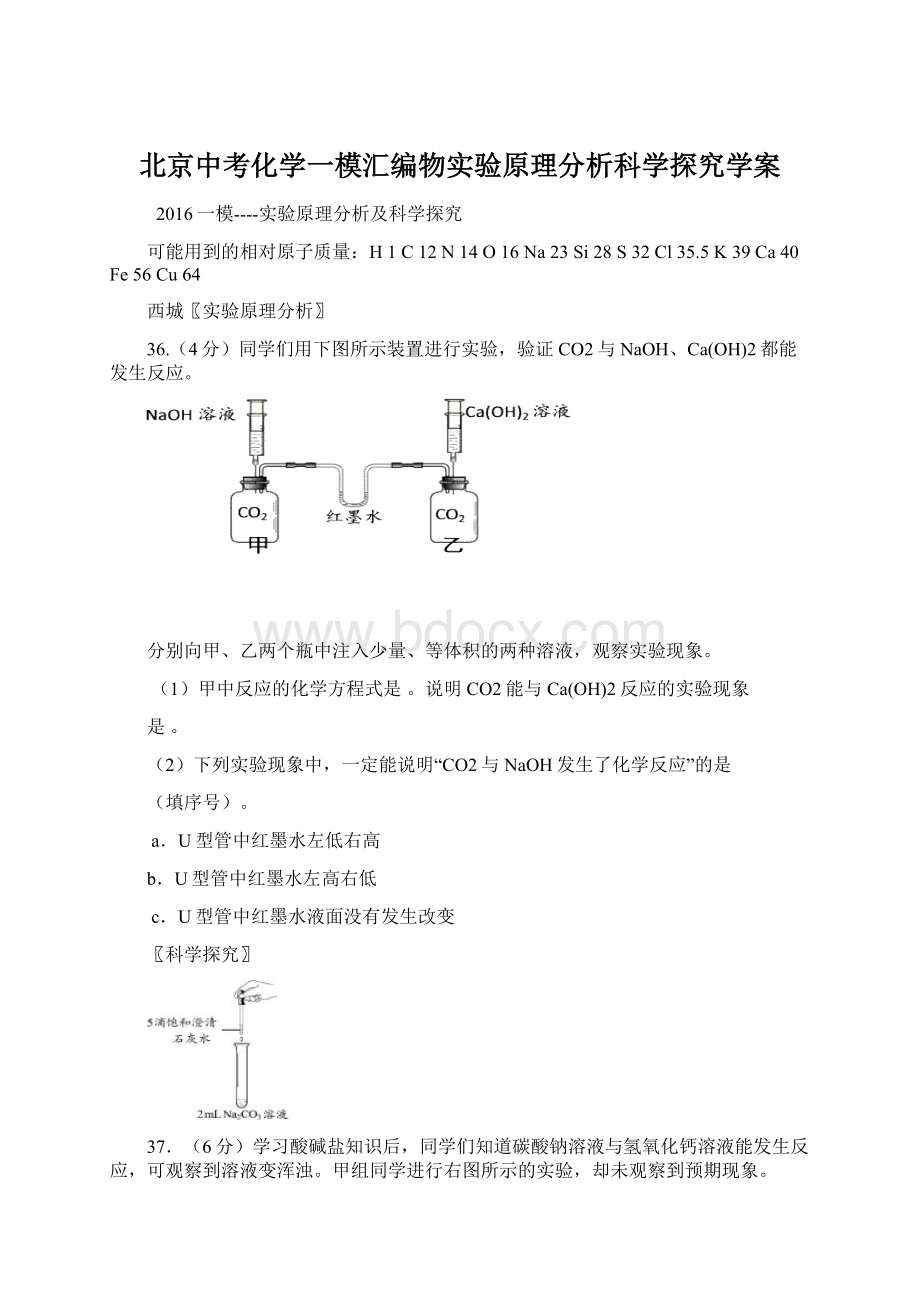
浑浊
0.5
【解释与结论】
(1)补全上述实验操作:
取4支试管,向其中分别加入。
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是。
(3)乙组实验证明:
猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是。
【实验反思】
(1)丙组同学对乙组所做实验中未出现浑浊的原因进行探究。
设计了多组实验,其中部分同学的实验过程及结果如下:
丙组同学的实验目的是。
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊。
其实验操作是。
东城〖实验原理分析〗
36.(4分)利用下图装置在实验室模拟炼铁,并将得到的尾气中的一氧化碳和二氧化碳进行分离和收集。
(提示:
NaOH溶液可以吸收CO2气体。
)
实验步骤如下:
(1)检查装置气密性。
(2)取一定质量的氧化铁加入硬质玻璃管中,其它容器中各加入适量试剂(如图所示)。
(3)关闭分液漏斗开关和K2,打开K1,通入CO气体一段时间,排除装置内的空气。
此时装置存在的缺陷是。
(4)继续通CO,在出口M处将气体干燥并用小试管收集后检验气体纯度。
待装置内气体纯净后,打开分液漏斗开关K,将足量的氢氧化钠溶液放入锥形瓶中,使液面没过导管下端,关闭开关K,点燃酒精喷灯,装置A的玻璃管中反应的化学方程式是。
当装置C中的现象是_______时,说明装置B中的反应是充分的,立即关闭K1,打开K2,装置D中收集到的气体是CO。
(5)一段时间后,停止加热,继续通CO气体至装置A的药品冷却。
经称量氢氧化钠溶液增重2.64g,此时生成Fe的质量是__________g(结果精确到0.1g)。
37.(6分)用久置的镁条做实验时,需要用砂纸把表面的灰黑色打磨掉,直到露出光亮的银白色。
实验小组同学对镁条表面“灰黑色外衣”的成分进行如下探究。
【提出问题】镁条表面“灰黑色外衣”的成分是什么?
【猜想与假设】
Ⅰ.是镁与空气中的氧气反应生成的氧化镁。
Ⅱ.是镁与空气中的二氧化碳反应生成的黑色碳单质。
Ⅲ.根据铜锈的成分是碱式碳酸铜,推测镁条表面的“灰黑色外衣”是镁在潮湿的空气中生锈得到的碱式碳酸镁。
同学们经讨论,从颜色上否定了只含有氧化镁,因为氧化镁是________。
【查阅资料】
①碱式碳酸镁的性质有:
受热可分解;
常温下能与稀硫酸反应。
②白色的硫酸铜粉末遇水能变为蓝色。
③碳不与稀硫酸反应,但与浓硫酸在加热条件下能反应并生成CO2、SO2和H2O。
同学们认为碳与浓硫酸反应生成三种产物的共同点是(答出一点即可)。
【进行实验】
(1)同学们用久置的镁粉进行了如下实验。
实
验
装
置
现
象
无水硫酸铜粉末逐渐由白色变为蓝色
澄清石灰水变浑浊
结
论
久置的镁粉中除镁元素外,还含有的元素是
久置的镁粉中含有碱式碳酸镁
(2)同学们发现,经加热一段时间后,试管中镁粉会突然“噗”地燃烧起来,出现红热,很快停止,并有黑色固体粘附在试管壁上。
①将试管取下,冷却后加入足量稀硫酸,大部分固体溶解,并有气泡出现,但黑色固体没有消失。
请写出有气体生成的一个反应化学方程式________。
②将实验①试管中的混合物进行_______(填操作名称),除去其中溶液,向黑色固体中加入浓硫酸,加热。
黑色固体全部溶解,得澄清溶液并伴有刺激性气味的气体产生。
实验
(2)说明,镁在CO2中可以燃烧,生成了碳单质。
【实验结论】
综合上述实验现象,实验小组认为镁条表面“灰黑色外衣”中含有碳和碱式碳酸镁。
【反思与评价】
有的同学提出,实验
(2)不足以证明镁条表面“灰黑色外衣”中含有碳,他的理由是_____________。
海淀〖实验原理分析〗
36.(4分)为了研究反应中压强的变化情况,利用下图进行实验。
(1)检查装置气密性:
打开a,关闭b,在A中加入水,,则装置的气密性良好。
用同样原理可以检查装置另一侧的气密性。
(2)在A、B中分别加入澄清石灰水,在集气瓶内放入一定量的大理石,将a、b都打开,用注射器加入足量稀盐酸直至液面浸没下端管口,保持注射器活塞不动。
此时,可观察到的现象是。
(3)关闭b,集气瓶中持续产生气体,A中的现象是。
判断A中是否发生化学反应:
(若没有反应,写出理由;
若发生反应,写出化学方程式)。
37.(6分)某化学小组用石灰石(含杂质SiO2、CaO,还可能含有少量的Fe2O3)与足量的稀盐酸制备二氧化碳气体,实验结束后对废液中的溶质成分进行探究(溶解于水中的气体成分忽略不计)。
【提出问题】废液中的溶质含有哪些物质?
①SiO2不溶于水,且不与稀盐酸反应。
②FeCl3溶液遇到硫氰化钾(KSCN)溶液能够很灵敏的显现出红色。
③FeCl3只能在较强的酸性溶液中存在,若pH>3.8时,FeCl3会完全与水发生反应生成Fe(OH)3沉淀。
④已知反应:
CaCl2+Na2CO3===CaCO3↓+2NaCl。
【假设猜想】
(1)该小组同学一致认为废液中一定含有CaCl2,用化学方程式表示其原因是。
(2)结合以上资料,该小组同学作出以下三种合理的猜想
猜想1:
溶质只含有CaCl2
猜想2:
溶质含有CaCl2和HCl
猜想3:
溶质含有
【实验验证】
实验结论
步骤1:
取少量过滤后的废液于试
管中,滴加溶液
溶液没有变红
废液的溶质中
不含FeCl3
步骤2:
另取少量过滤后的废液于试管中,加入过量的Na2CO3溶液
猜想2成立
【反思评价】
(1)上述步骤2中,小姚同学提出可以通过检测废液的pH来判断是否含有HCl。
你认为该方案是否合理,其原因是。
(2)根据实验结论,实验结束后若要回收CaCl2溶液,正确的操作是:
向废液中加入过量的,过滤。
朝阳【实验原理分析】
36.(4分)化学小组用下图所示装置研究酸碱盐的性质(夹持装置已省略)。
资料:
Na2CO3溶液可与中性的CaCl2溶液发生复分解反应。
(1)关闭K2,打开K1和分液漏斗玻璃塞、活塞,向B中加入稀盐酸,使其浸没大理石后关闭分液漏斗活塞。
A中反应的化学方程式为_________,B中反应的化学方程式为_________。
(2)当B中的物质仍在反应时,关闭K1,打开K2。
一段时间后C中的现象为_________;
充分反应后,C中一定含有溶质NaCl的原因是_________。
【科学探究】
37.(6分)在一次化学实验中,同学们将饱和硫酸铜溶液滴加到5mL饱和氢氧化钠溶液中,观察到以下异常现象:
实验序号
滴加CuSO4溶液的量
①
第1~6滴
产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液
②
第7~9滴
产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀变成黑色
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式_________。
【提出问题】
实验①中蓝色沉淀为什么消失?
I.氢氧化铜在室温下稳定,70℃~80℃时可分解生成氧化铜。
II.铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色。
I.蓝色沉淀消失可能是氢氧化铜发生分解反应。
II.蓝色沉淀消失可能是氢氧化铜溶解在氢氧化钠溶液中,形成亮蓝色溶液。
甲同学认为猜想Ⅰ不成立,理由是_________。
乙同学为验证猜想Ⅱ,进行了如下实验。
(1)1号试管中现象为_________。
(2)上述实验得出的结论是_________。
(1)进一步查阅资料可知,氢氧化铜在氢氧化钠溶液中溶解生成铜酸钠,反应的化学方程式为_________。
(2)丙同学推知饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是_________。
通州【实验原理分析】
36.(5分))利用如图装置进行燃烧条件的探究。
(资料:
S+O2
SO2)
A
(1)打开K1、K2、K4,关闭K3,向装置中通入二氧化碳气体,当观察到________,则证明该装置内的空气已经排净。
关闭K1,点燃酒精灯,加热硫粉,观察到硫粉并不燃烧。
以上操作都需要打开K4,原因是________。
(2)待冷却后,打开K1,向装置中通入氧气,证明装置内的二氧化碳已经排净的方法和现象是_________。
(3)打开________,关闭________,点燃酒精灯,加热硫粉,观察到硫粉燃烧,发出明亮的蓝紫色火焰。
该实验装置的主要优点是消除了有害气体对环境的污染。
37.(6分)化学兴趣小组欲探究自己使用的某品牌牙膏的主要成分。
(1)牙膏的成分有活性物质、摩擦剂、保持牙膏湿润的甘油等物质。
(2)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。
(3)牙膏除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
(4)SiO2不溶于水,也不与盐酸反应。
Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠(NaAlO2)和水,该反应的化学方程式为________。
偏铝酸钠和适量稀盐酸反应生成氢氧化铝,氢氧化铝和稀盐酸可以发生中和反应。
物质
Al(OH)3
NaAlO2
AlCl3
溶解性
不溶
溶
(5)相关物质的溶解性表:
该品牌牙膏含有上述摩擦剂中的两种成分,为探究摩擦剂的组成,化学兴趣小组取适量该牙膏加水充分搅拌、静置、过滤、洗涤、干燥,得到该牙膏中的摩擦剂。
【提出猜想】猜想1:
摩擦剂的成分为Al(OH)3和CaCO3。
摩擦剂的成分为_______________。
摩擦剂的成分为SiO2和Al(OH)3。
【设计实验】
实验步骤
预期实验现象
预期实验结论
组装下图装置进行实验。
取少量摩擦剂于锥形瓶中,加入适量的________。
固体全部溶解,有气泡,石灰水变混浊
则猜想1成立
锥形瓶中发生的化学反应方程式为________。
摩擦剂部分溶解
石灰水无明显变化
则猜想3成立
【实验结论】经过实验验证,猜想1成立。
【实验反思】同学们为进一步确认摩擦剂中含有氢氧化铝,先在少量牙膏样品中加入过量的氢氧化钠溶液,静置一段时间,取上层清液,再滴加稀盐酸至过量。
整个实验过程中观察到的现象为________,依据该现象可以判断摩擦剂中一定含有氢氧化铝。
顺义【实验原理分析】
33.(5分)甲、乙两个实验小组利用下图装置(夹持装置已略去),做了一个兴趣实验,证明了二氧化碳与氢氧化钠的反应产物中有碳酸钠生成。
他们的实验步骤如下:
①在玻璃管中加入一定量碳酸钙,关闭K1、K3,打开K4,从
分液漏斗放入稀盐酸并收集二氧化碳
②打开K1,使玻璃管中的液体流入烧杯,并用清水冲洗
③关闭K1,从分液漏斗向玻璃管中加入氢氧化钠溶液
④使二氧化碳与氢氧化钠充分反应
关闭K3,打开K4,从分液漏斗放入稀盐酸
打开K1,使玻璃管中的液体流入烧杯
回答下列问题:
(1)步骤①中发生反应的化学方程式为__________。
(2)步骤④的具体操作是________。
(3)整个过程中注射器的作用是__________。
(4)在步骤
中,甲乙两组观察到了不同的现象。
甲组发现烧杯中液体变浑浊;
乙组发现烧杯中产生了大量气泡。
两组产生不同现象的原因是________。
34.冬季取暖人们常用到暖宝宝(右图),其热量来源于铁的缓慢氧化。
化学小组的同学突发奇想,想利用暖宝宝测定空气中氧气的含量。
查阅资料:
(1)暖宝宝的主要成分铁粉、木炭、食盐。
(2)暖宝宝反应的主要原理是铁粉与氧气、水共同作
用生成氢氧化铁,反应的化学方程式为
__________。
设计实验:
化学小组的同学设计了右图1所示装置。
检查装置气密性
向250mL集气瓶中加入20mL水
读取温度计示数为18oC,撕掉暖宝宝上的贴纸,塞紧橡胶塞。
观察温度计示数的变化
待温度计示数为18oC时,打开止水夹。
回答下列问题:
(1)检查装置气密性的方法是________。
(2)小组同学的设计中,集气瓶内水的作用是__________。
(3)实验结果如图2所示,则小组同学得出的结论是__________。
实验反思:
反思实验过程,你认为小组同学实验产生误差的可能原因有_________(写出一条即可)。
你证明这确实是造成误差原因的方案是________。
密云
【实验原理分析】
35.(5分)春节期间燃放烟花爆竹会使空气中有害气体SO2的含量增加,为粗略测定空气中SO2的含量,化学小组的同学们设计了如下图所示的实验装置进行实验:
【资料】
①SO2+I2+2H20=H2SO4+2HI,碘遇淀粉能使淀粉显蓝色,而HI溶液不能使淀粉显蓝色。
②我国空气质量标准中SO2浓度限值(mg/m3)如下表;
一级标准
二级标准
三级标准
≤0.15
≤0.50
≤0.70
【实验步骤】
①检查气密性;
②向C装置中加入1.0mL溶质质量分数为1.27×
10﹣6g/mL的碘水(ρ≈1.0g/mL),滴入
2~3滴淀粉溶液,此时溶液显蓝色;
③打开弹簧夹_____(填“a”或“b”),关闭另一个弹簧夹,抽拉注射器吸取250mL空气,再开、闭相应弹簧夹,缓缓推气体进入C装置,重复上述操作多次。
当C中溶液颜色______时,停止推动注射器的活塞;
④实验数据处理。
请回答下列问题:
(1)完善步骤③的内容__________;
_____________。
(2)检查此装置气密性的操作是:
_______________;
(3)该小组在同一地点进行了3组实验,推动活塞次数记录如下表(每次抽气为250mL)。
进行3组实验的目的是__________;
综合3次实验数据分析:
该测定地点的空气质量属于____ 级标准
2
3
推动次数
4
36.(5分)小新在实验室制取二氧化碳时发现:
如果用大理石和稀硫酸混合制二氧化碳,一开始产生一些气泡,可是很快气泡产生的速度越来越慢,最终停止了。
其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止。
因此通常不选用大理石与稀硫酸反应制取二氧化碳。
对此,小新产生了疑问并大胆猜想展开实验。
(1)
【猜想一】选择合适的硫酸的浓度能使反
应快速进行
【进行实验】在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,实验选取5种浓度(如右图)的硫酸分5组完成,每次记录15分钟内生成气体的体积,记录在下表:
试管编号
气体体积(mL)
35
47
55
51
42
(2)
【猜想二】选择合适的温度可以使反应快速进行
【进行实验】向5只分别盛有1g、直径为2mm大理石的大试管中各加入5mL相同浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
B
C
D
E
温度℃
40
50
60
70
80
现象
有气泡
气泡比A试管多
气泡明显比B号试管多,持续时间更长
大量气泡产生,与常温用盐酸反应相似
反应非常剧烈,大理石迅速溶解并产生大量气体
(3)
【实验分析】
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适的是_____%。
②在合适的硫酸浓度下,应选择最合适的反应温度为_____℃。
③除选用合适温度和浓度硫酸之外,在反应过程中,为防止微溶物硫酸钙覆盖在大理石上,应
增加_________操作,更有利气体的制备。
(4)你认为还可以研究________对该反应速率的影响,请你设计实验简述实验步骤__________________。
延庆
36.(4分)如图是某研究性学习小组进行CO2与NaOH溶液反应的探究实验装置.
【查阅资料】水的沸点与气体压强有关,气体压强小,沸点低;
气体压强大,沸点高。
【实验探究】实验步骤如下:
步骤①:
如图所示,锥形瓶A盛满CO2气体,锥形瓶B盛有96℃以上但未沸腾的热水,烧杯中加入同样温度的热水(起保持锥形瓶B中水温恒定的作用).
步骤②:
取2支注射器,一支抽取20mL水,另一支抽取20mL浓NaOH溶液.
步骤③:
将注射器中20mL水注入锥形瓶A中,振荡后观察,锥形瓶B中的热水没有沸腾.
步骤④:
取下盛水的注射器,再将盛20mL浓NaOH溶液的注射器迅速连接到锥形瓶A上,注入该溶液并振荡,观察到明显的现象。
(1)实验开始前,依上图连接好装置(锥形瓶A、B和烧杯均未盛装物质),将一支空注射器连接到锥形瓶A上,并将其活塞缓慢向上拉,几秒钟后松手,观察活塞是否复位,这个操作的目的是 。
(2)锥形瓶A中CO2与NaOH溶液反应的化学方程式是_____________________。
(3)步骤④锥形瓶B中产生的明显现象是 ;
产生明显现象的原因是 。
37.(6分)某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣。
在老师的指导下,用自制的实验装置(主体部分如右图所示)进行电解饱和食盐水制取氢氧化钠的实验。
一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究。
提示:
I.电解饱和食盐水的反应,见本试卷30题。
II.忽略其他可能发生的反应对以下实验的影响。
探究活动一:
检验待测液中含有氢氧化钠
(1)检验含有氢氧化钠的方法是。
探究活动二:
测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐加入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
加入稀盐酸的体积/mL
2.0
4.0
6.0
8.0
9.8
烧杯中溶液的pH
13.0
12.9
12.8
12.6
12.3
7.0
(2)写出氢氧化钠与稀盐酸反应的化学方程式:
。
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为mL。
【实验2】用沉淀法测定
资料摘要:
氢氧化钠与氯化镁溶液中发生反应:
2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:
(4)步骤②加入的氯化镁溶液必需足量,其目的是。
滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:
静置,(写出实验步骤、现象和结论)。
(5)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所测定氢氧化钠的质量分数将
(选填“偏大”、“偏小”或“没影响”)。