高考化学考前冲刺单选化学反应平衡Word文档下载推荐.docx
《高考化学考前冲刺单选化学反应平衡Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《高考化学考前冲刺单选化学反应平衡Word文档下载推荐.docx(33页珍藏版)》请在冰豆网上搜索。
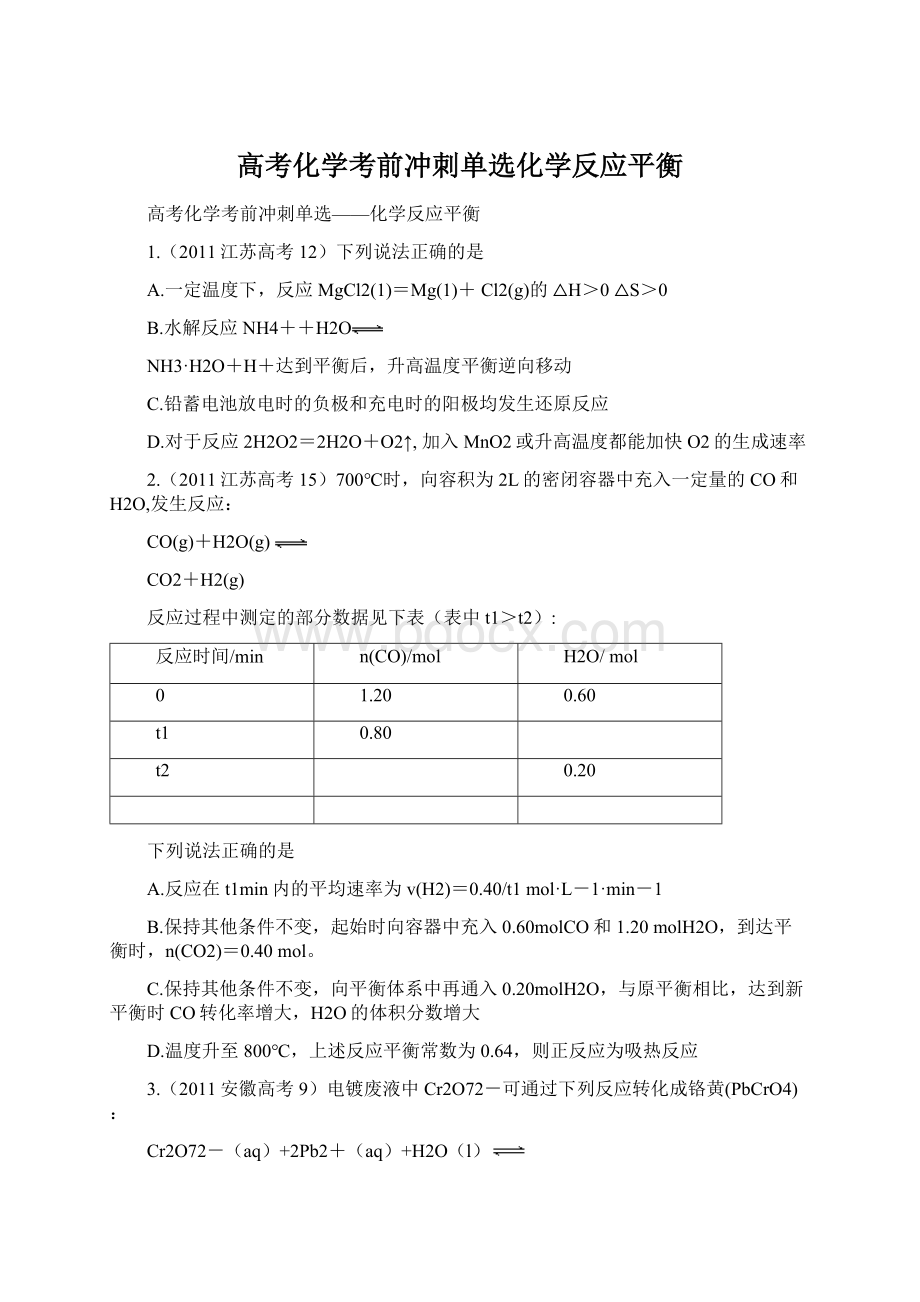
Sn(s)+Pb2+(aq)
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如下图所示。
下列判断正确的是
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
6.(2011天津)向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
由图可得出的正确结论是
A.反应在c点达到平衡状态
B.反应物浓度:
a点小于b点
C.反应物的总能量低于生成物的总能量
D.△t1=△t2时,SO2的转化率:
a~b段小于b~c段
7.(2011重庆)一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10的是
A.CO2(g)+2NH3(g)
CO(NH2)2(s)+H2O(g);
△H<0
B.CO2(g)+H2(g)
CO(g)+H2O(g);
△H>0
C.CH3CH2OH(g)
CH2=CH2(g)+H2O(g);
D.2C6H5CH2CH3(g)+O2(g)
2C6H5CH=CH2(g)+2H2O(g);
8.(2011海南)对于可逆反应
,在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是
A.H2(g)的消耗速率与HI(g)的生成速率之比为2:
1
B.反应进行的净速率是正、逆反应速率之差
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
9.(2011全国II卷8)在容积可变的密闭容器中,2mo1N2和8mo1H2在一定条件下发生反应,达到平衡
时,H2的转化率为25%,则平衡时的氮气的体积分数接近于
A.5%B.10%C.15%D.20%
10.(2011四川)可逆反应①X(g)+2Y(g)
2Z(g)、②2M(g)
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。
反应开始和达到平衡状态时有关物理量的变化如图所示:
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:
15
C.达平衡(I)时,X的转化率为
D.在平衡(I)和平衡(II)中M的体积分数相等
11.(2011江苏高考14)下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.在0.1mol·
L-1NaHCO3溶液中:
c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1mol·
L-1Na2CO3溶液中:
c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3-)
C.向0.2mol·
L-1NaHCO3溶液中加入等体积0.1mol·
L-1NaOH溶液:
c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol·
L-1]:
c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
12.(2011安徽高考12)室温下,将1.000mol·
L-1盐酸滴入20.00mL1.000mol·
L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。
下列有关说法正确的是
A.a点由水电离出的c(H+)=1.0×
10-14mol/L
B.b点:
c(NH4+)+c(NH3·
H2O)=c(Cl-)
C.c点:
c(Cl-)=c(NH4+)
D.d点后,溶液温度略下降的主要原因是NH3·
H2O电离吸热
13.(2011浙江高考13)海水中含有丰富的镁资源。
某同学设计了从模拟海水中制备MgO的实验方案:
模拟海水中的离
子浓度(mol/L)
Na+
Mg2+
Ca2+
Cl―
0.439
0.050
0.011
0.560
0.001
注:
溶液中某种离子的浓度小于1.0×
10-5mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:
Ksp(CaCO3)=4.96×
10-9;
Ksp(MgCO3)=6.82×
10-6;
Ksp[Ca(OH)2]=4.68×
Ksp[Mg(OH)2]=5.61×
10-12。
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2gNaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
14.(2011福建高考10)常温下0.1mol·
L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2mol·
L-1盐酸
D.提高溶液的温度
15.(2011广东非公开11)对于0.1mol•L-
1Na2SO3溶液,正确的是
A、升高温度,溶液的pH降低
B、c(Na+)=2c(SO32―)+c(HSO3―)+c(H2SO3)
C、c(Na+)+c(H+)=2c(SO32―)+2c(HSO3―)+c(OH―)
D、加入少量NaOH固体,c(SO32―)与c(Na+)均增大
16.(2011山东高考14)室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mlpH=11的NaOH溶液,混合液pH=7
17.(2011天津)25℃时,向10ml0.01mol/LKOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓度关系正确的
A.pH>
7时,c(C6H5O-)>
c(K+)>
c(H+)>
c(OH-)
B.pH<
7时,c(K+)>
c(C6H5O-)>
C.V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>
c(OH-)=c(H+)
D.V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+)
18.(2011天津)下列说法正确的是
A.25℃时NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW
B.SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO32-+2I-
C.加入铝粉能产生氢气的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3-
D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
19.(2011重庆)对滴有酚酞试液的下列溶液,操作后颜色变深的是
A.明矾溶液加热B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体D.小苏打溶液中加入少量NaCl固体
20.(2011新课标全国)将浓度为0.1mol·
L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A.c(H+)B.
C.
D.
21.(2011海南)用0.1026mol·
L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为
A.22.30mLB.22.35mLC.23.65mLD.23.70Ml
22.(2011全国II卷6)等浓度的系列稀溶液:
①乙酸、②苯酚、③碳酸、④乙醇,它们的PH由小到大排列的正确是
A.④②③①B.③①②④C.①②③④D.①③②④
23.(2011全国II卷9)温室时,将浓度和体积分别为c1、v1的NaOH溶液和c2、v2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
A.若PH>
7时,则一定是c1v1=c2v2
B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.当pH=7时,若V1=V2,则一定是c2>
c1
D.若V1=V2,C1=C2,则c(CH3COO-)+C(CH3COOH)=C(Na+)
24.(2011四川)25℃时,在等体积的①pH=0的H2SO4溶液、②0.05mol/L的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
A.1:
10:
10
:
B.1:
5:
5×
C.1:
20:
D.1:
25.(2011上海19)常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是
A.b不可能显碱性B.a可能显酸性或碱性
C.a不可能显酸性D.b可能显碱性或酸性
26.(2012上海∙7)水中加入下列溶液对水的电离平衡不产生影响的是
A.NaHSO4溶液B.KF溶液
C.KAl(SO4)2溶液D.NaI溶液
27.(2012上海∙21)常温下amol·
L-1CH3COOH稀溶液和bmol·
L-1KOH稀溶液等体积混合,下列判断一定错误的是
A.若c(OH-)>
c(H+),a=bB.若c(K+)>
c(CH3COO-),a>
b
C.若c(OH-)=c(H+),a>
bD.若c(K+)<
c(CH3COO-),a<
28.(2012安徽∙12)氢氟酸是一种弱酸,可用来刻蚀玻璃。
已知25℃时
①HF(aq)+OH—(aq)=F—(aq)+H2O(l)△H=−67.7KJ·
mol—1
②H+(aq)+OH—(aq)=H2O(l)△H=−57.3KJ·
在20mL0.1·
molL—1氢氟酸中加入VmL0.1mol·
L—1NaOH溶液,下列有关说法正确的是
A.氢氟酸的电离方程式及热效应可表示为:
HF(aq)=H+(aq)+F−(aq)△H=+10.4KJ·
B.当V=20时,溶液中:
c(OH—)=c(HF)+c(H+)
C.当V=20时,溶液中:
c(F—)<c(Na+)=0.1mol·
L—1
D.当V>0时,溶液中一定存在:
c(Na+)>c(F—)>c(OH—)>c(H+)
29.(2012海南∙11)25℃时,amol.L-1一元酸HA与bmol.L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是
A.a=bB.a>
C.c(A-)=c(Na+)D.c(A-)<
c(Na+)
30.(2012四川∙10)常温下,下列溶液中的微粒浓度关系正确的是
A.新制氯水中加入固体NaOH:
c(Na+)=c(Cl−)+c(ClO−)+c(OH−)
B.pH=8.3的NaHCO3溶液:
c(Na+)>
c(HCO3−)>
c(CO32−)>
c(H2CO3)
C.pH=11的氨水与pH=3的盐酸等体积混合:
c(Cl−)=c(NH4+)>
c(OH−)=c(H+)
D.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:
2c(H+)–2c(OH−)=c(CH3COO−)–c(CH3COOH)
3.(2012江苏∙15)25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol·
L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示。
下列有关离子浓度关系叙述正确的是
A.pH=5.5溶液中:
c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.W点表示溶液中:
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.pH=3.5溶液中:
c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol·
L-1
D.向W点所表示溶液中通入0.05molHCl气体(溶液体积变化可忽略):
c(H+)=c(CH3COOH)+c(OH-)
3.(2012天津∙5)下列电解质溶液的有关叙述正确的是()
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1molKOH的溶液与1molCO2完全反应后,溶液中c(K+)=c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-)
3.(2012新课标∙11)已知温度T时水的离子积常数为Kw,该温度下,将浓度为amol∙L−1的一元酸HA与bmol∙L−1的一元碱BOH等体积混合·
可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=
mol∙L−1
D.混台溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
3.(2012浙江∙12)下列说法正确的是:
A.在100℃、101kPa条件下,液态水的气化热为40.69kJ·
mol-1,则H2O(g)
H2O(l)的ΔH=40.69kJ·
mol-1
B.已知MgCO3的Ksp=6.82×
10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·
c(CO32-)=6.82×
10-6
C.已知:
共价键
C-C
C=C
C-H
H-H
键能/kJ·
348
610
413
436
则可以计算出反应
的ΔH为-384kJ·
D.常温下,在0.10mol·
L-1的NH3·
H2O溶液中加入少量NH4Cl晶体,能使NH3·
H2O的电离度降低,溶液的pH减小
35.(2012重庆∙10)下列叙述正确的是
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电力程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH值不变
D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
36.(2012重庆∙11)向10mL0.1mol·
L−1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL,下列叙述正确的是
A.x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>
c(Al3+)
B.x=10时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>
c(SO42-)
C.x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<
c(AlO2-)
D.x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-)=c(Ba2+)
37.(2013福建卷)室温下,对于0.10mol·
L-1的氨水,下列判断正确的是( )
A.与AlCl3溶液反应发生的离子方程式为Al3++3OH—=Al(OH)3↓
B.加水稀释后,溶液中c(NH4+)c(OH—)变大
C.用HNO3溶液完全中和后,溶液不显中性D.其溶液的pH=13
38.(2013大纲卷)右图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是
A.两条曲线间任意点均有c(H+)×
c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
39.(2013江苏卷)下列有关说法正确的是
A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH溶液加水稀释后,溶液中
的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
40.(2013江苏卷)一定温度下,三种碳酸盐MCO3(M:
Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。
已知:
pM=-lgc(M),
pc(CO32-)=-lgc(CO32-)。
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO32-)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-)
41.(2013海南)0.1mol/LHF溶液的pH=2,则该溶液中有关浓度关系式不正确的是
A.c(H+)>
c(F-)B.c(H+)>
c(HF)C.c(OH-)>
c(HF)D.c(HF)>
c(F-)
42.[2013高考∙重庆卷∙2]下列说法正确的是
A.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
B.25℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH
C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成
D.AgCl易转化为AgI沉淀且K(AgX)=c(Ag+)∙c(X—),故K(AgI)<K(AgCl)
43.(2013四川卷)室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号
起始浓度/(mol·
L-1)
反应后溶液的pH
c(HA)
c(KOH)
①
0.1
9
②
x
0.2
7
下列判断不正确的是( )
A.实验①反应后的溶液中:
c(K+)>
c(A—)>
c(OH—)>
c(H+)
B.实验①反应后的溶液中:
c(OH—)=c(K+)—c(A—)=
mol/L
C.实验②反应后的溶液中:
c(A—)+c(HA)>
0.1mol/L
D.实验②反应后的溶液中:
c(K+)=c(A—)>
c(OH—)=c(H+)
44.(2013上海卷)374℃、22.1Mpa以上的超临界水具有很强的溶解有机物的能力,并含有较多的H+和OH-,由此可知超临界水
A.显中性,pH等于7B.表现出非极性溶剂的特性
C.显酸性,pH小于7D.表现出极性溶剂的特性
45.(2013上海卷)H2S水溶液中存在电离平衡H2S
H++HS-和HS-
H++S2-。
若向H2S溶液中
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH值增大
C.滴加新制氯水,平衡向左移动,溶液pH值减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
46.(2013上海卷)部分弱酸的电离平衡常数如下表:
弱酸
HCOOH
HCN
H2CO3
电离平衡常数
(25℃)
Ki=1.77×
10-4
Ki=4.9×
10-10
Ki1=4.3×
10-7
Ki2=5.6×
10-11
下列选项错误的是
A.2CN-+H2O+CO2→2HCN+CO32-B.2HCOOH+CO32-→2HCOO-+H2O+CO2↑
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
47.(2013山东卷)某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=-lg[OH-])与pH的变化关系如图所示,则
A.M点所示溶液导电能力强于Q点B.N点所示溶液中c(CH3COO-)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
48.(2013浙江卷)25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示。
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:
HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10—5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:
c(X—)>c(Y—)>c(OH—)>c(H+)
D.HY与HZ混合,达到平衡时:
c(H+)=+c(Z—)+c(OH—)
49.(2013广东卷)50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:
c(H+)=4.0mol·
L-1B.饱和小苏打溶液中:
c(Na+)=c(HCO3-)
C.饱和食盐水中:
c(Na+)+c(H+)=c(Cl-)+c(OH-)
D.pH=12的纯碱溶液中:
c(OH-)=1.0×
10-2mol·
L-1
50.(2013全国新