修苏塘中 学 化 学 实 验 报 告Word下载.docx
《修苏塘中 学 化 学 实 验 报 告Word下载.docx》由会员分享,可在线阅读,更多相关《修苏塘中 学 化 学 实 验 报 告Word下载.docx(10页珍藏版)》请在冰豆网上搜索。
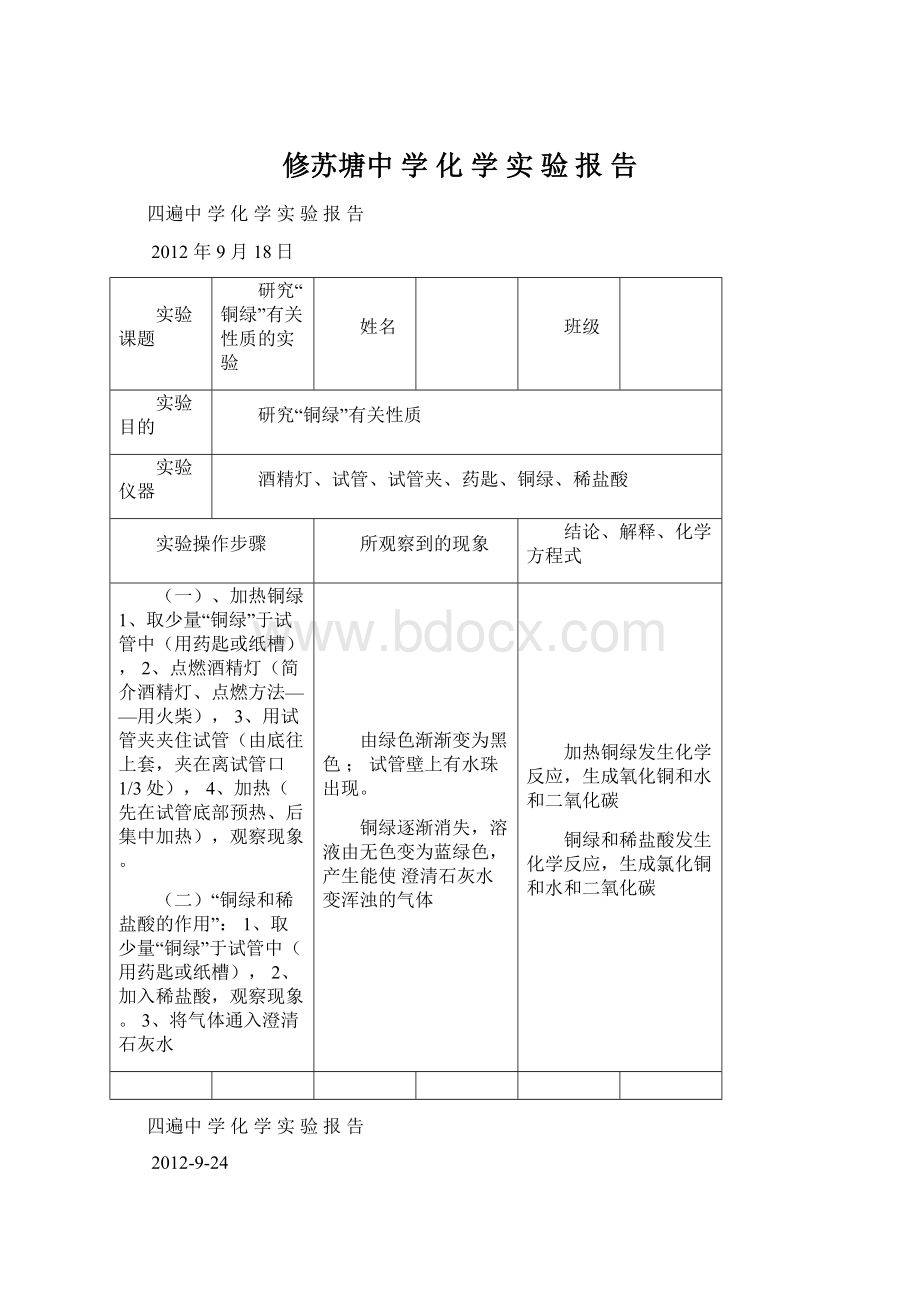
由绿色渐渐变为黑色;
试管壁上有水珠出现。
铜绿逐渐消失,溶液由无色变为蓝绿色,产生能使澄清石灰水变浑浊的气体
加热铜绿发生化学反应,生成氧化铜和水和二氧化碳
铜绿和稀盐酸发生化学反应,生成氯化铜和水和二氧化碳
2012-9-24
氧气的实验室制法
通过实验验证氧气的化学性质,进一步熟练化学实验基本操作
分液漏斗、锥形瓶、铁架台(带铁夹)、带导管的的橡皮塞、镊子、集气瓶、水槽、酒精灯、火柴、6%的过氧化氢溶液、MnO2高锰酸钾棉花木块
1、检查气密性2将高锰酸钾装入试管内,注意要平铺;
3,安装仪器:
将木块放在铁架台上,再将酒精灯放在木块上,然后将试管夹在铁架台上,接着放水槽,接胶皮接管,放集气瓶。
4、点燃酒精灯,5,收集氧气,看见水中有连续均匀的冒出水泡,然后将装满水的集气瓶朝下开始集气,直至瓶内水全部排完,迅速盖上玻璃6,撤离导管7,熄灭酒精灯
2、用双氧水制氧气1、组装仪器,检查装置气密性:
。
2、先向长颈漏斗中放入MnO2,,固定仪器。
3、集气瓶中装满水倒扣在水槽中。
4加双氧水产生大量的氧气5、用带火星的木条验证收集的气体是氧气。
二氧化
产生大量的氧气
高锰酸钾(加热)——锰酸钾+二氧化锰+氧气
过氧化氢——氧气+水
中学化学实验报告
2012年10月10日
二氧化碳与水反应
加深对二氧化碳性质的认识
带导管的的橡皮塞火柴、试管、酒精灯、紫色石蕊试液、
1、在大试管里放入几小块碳酸钙,然后加入10-15ml稀盐酸,立即用带有导管的橡皮塞塞住管口,将导管通入盛有紫色石蕊试液的试管,观察试管里发生的现象。
2、将变红的试液在酒精灯上加热
紫色石蕊试液变红
红色的试液又重新变为紫色
年月日
二氧化碳的制取和性质
掌握实验室制取二氧化碳的方法,掌握用向上排空气法收集气体。
长颈漏斗、锥形瓶、铁架台(带铁夹)、带导管的的橡皮塞、镊子、集气瓶、玻璃片,烧杯
1.按照教材图2-17装置图连接装置,并检验装置的气密性。
2.向锥形瓶内放入块状碳酸钙,然后通过长颈漏斗加入稀盐酸
3、用集气瓶收集气体,过一会儿,用燃着的木条放在集气瓶瓶口,木条火焰熄灭,说明二氧化碳已收集满了。
用玻璃片盖住已收集的集气瓶。
4.把两支短蜡烛放在烧杯的高低铁架上,点燃。
拿起盛满二氧化碳的集气瓶,向烧杯里慢慢倾倒二氧化碳。
观察到的现象
有气泡放出。
下面的蜡烛先熄灭,上面的蜡烛后熄灭
碳酸钙+稀盐酸===氯化钙+水+二氧化碳
二氧化碳密度大于空气,不支持燃烧
20121017
过滤
.掌握过滤实验的操作技能
铁架台、漏斗、烧杯、玻璃棒、酒精灯、小烧杯
1、将滤纸折叠后用水润湿使其紧贴漏斗内壁并使滤纸上沿低于漏斗口
2、倾倒溶液液面低于滤纸上沿,倾倒液体的烧杯口要紧靠玻璃棒,玻璃棒的末端紧靠有三层滤纸的一边,漏斗末端紧靠承接滤液的烧杯的内壁。
3、慢慢倾倒液体,待滤纸内无水时,仔细观察滤纸上的剩余物及滤液的颜色.
滤纸上有残渣,滤液澄清
过滤能够将不溶于液体的固体物质与液体分离开来
2012年11月27日
质量守恒定律实验
加深理解质量守恒定律。
托盘天平、砝码、药匙、量筒、滴管、玻璃棒、烧杯、小试管、锥形瓶。
1、氢氧化钠溶液和硫酸铜溶液反应
(1)、称量烧杯、试管及溶液的总质量
(2)、将试管内的蓝色(或黄色)溶液倒入烧杯内的无色溶液中
(3)、称量混合后烧杯、试管及溶液的总质量
2、碳酸钙与盐酸反应
(1)、用托盘天平称量试管、烧杯、稀盐酸及石灰石的总质量
(2)、将稀盐酸与石灰石混合
产生蓝色沉淀
相等
产生大量气泡
相等
氢氧化钠+硫酸铜==氢氧化铜+硫酸钠
碳酸钙+稀盐酸==氯化钙+水+二氧化碳
参加化学反应的各物质的质量的总和等于反应后生成的各物质的质量总和
2012年12月12日
常见金属的化学性质
通过四组金属与盐酸的化学反应实验,比较不同金属活动性顺序;
掌握发生置换反应的实验条件以及反应实质,学会判断依据
试管、镊子、砂纸,铁片、铝片、铜片、稀硫酸
1、金属与氧气的反应
(1).将镁片在空气中点燃
(2)将铁丝在氧气中点燃
(3)铝片在空气中加热
(4)铜片在空气中加热
2、把金属镁、铁、铝、铜分别浸在稀硫酸中
发出耀眼的白光,放出大量的热,生成白色粉末状固体物质
剧烈燃烧,火星四射,生成黑色固体
表面生成一层白膜
表面变黑
1、镁片表面产生大量的气泡,且气泡产生的速率很快
2、铁片表面产生气泡,速度较慢、溶液由无色变为浅绿色
3铝片表面产生气泡,速度较快
4、铜片表面无气泡
镁+氧气===氧化镁
铁+氧气==四氧化三铁
铝+氧气===氧化铝
铜+氧气==氧化铜
1、镁可以与稀硫酸反应,很剧烈:
镁+稀硫酸==硫酸镁+氢气
2、铁可以与稀硫酸反应
铁+稀硫酸==硫酸亚铁+氢气
3、铝可以与稀硫酸反应,并且较剧烈
4、铜不能与稀硫酸反应
2012年12月14日
实验室制取氢气铁与硫酸铜溶液的置换反应
掌握实验室制取氢气的方法,理解发生置换反应的实验条件以及反应实质
试管、带导管的单孔橡皮塞、小试管、锥形瓶、双孔橡皮塞、长颈漏斗、导管、止水夹、烧杯、水槽、镊子
一制取氢气
1、检查装置气密性,
2、用镊子将锌粒放入锥形瓶中,
3、通过长颈漏斗向锥形瓶中加入稀硫酸,
4、用向下排空气法(排水法)开始收集氢气
二、铁与硫酸铜溶液
在一支试管中加入少量硫酸铜溶液,把用砂纸擦亮的铁丝插入硫酸铜溶液中。
现象:
,方程式:
Fe+CuSO4
FeSO4+Cu
锥形瓶内有气泡产生
铁丝表面变红
锌+稀硫酸==硫酸锌+氢气
方程式:
铁和铜的活动性顺序:
铁>铜
2012年月日
碳酸盐的检验
掌握碳酸盐检验的方法
铁架台、试管、单孔橡皮塞、导管、镊子
1、在试管中添加碳酸盐样品
2、加入稀盐酸,观察现象
3、
4、将产生的气体铜入澄清石灰水
产生气泡
澄清石灰水变浑浊
稀盐酸+碳酸钙==氯化钙+水+二氧化碳
二氧化碳+氢氧化钙==碳酸钙+水
生石灰和熟石灰的性质实验
了解生石灰和熟石灰的性质
1、用坩埚钳夹持石灰石放在酒精喷灯外焰上加热后放在石棉网上,观察
2、将燃烧后的石灰石投入装有冷水的烧杯中,观察
3、静置后,取上层清液置于两支试管中,向一支试管中加入2滴酚酞试液,向另一支试管中的液体吹气
燃烧后的物质容易被捏碎
溶解,烧杯内的水沸腾
加入酚酞的试管溶液变红
另一支试管变浑浊
碳酸钙===氧化钙+二氧化碳
氧化钙+水===氢氧化钙
放出大量的热
物质在水中的分散现象
通过实验得出溶液的概念
高锰酸钾、食盐、蔗糖晶体、泥土、水、食用油、小烧杯、玻璃棒
1取少量高锰酸钾加入到水中,搅拌
少量食盐加入到水中,搅拌
取少量蔗糖晶体放入盛有水的小烧杯中,搅拌,
取少量泥土加入小烧杯中,加入适量的水,搅拌,静置
取1-2滴食用油加入水中振荡后静置
紫红色透明液体不分层
无色透明液体不分层
无色液体不分层
变浑浊,静置分层,下层为泥土
变浑浊,静置分层,上层为油,下层为水
结论:
物质以细小的固体颗粒分散在水中,则形成悬浊液;
物质以小液滴分散在水中,则形成乳浊液;
物质以分子或离子的形式均匀分散到另一种物质中形成均一、稳定的混合物叫做溶液。
乳化现象
通过实验了解乳化现象
试管、滴管、橡皮塞
在试管中加入5ml,用滴管向试管中加入1—2滴食用油和数滴洗洁精,用橡皮塞塞紧试管,振荡片刻,静置,观察实验现象
振荡后,油以很小的液滴形式均匀悬浮在水中形成乳浊液
洗洁精能够将不相溶的水和油以小液滴形式形成稳定的乳浊液