中考化学聚焦热点题型科学探究题1Word格式文档下载.docx
《中考化学聚焦热点题型科学探究题1Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《中考化学聚焦热点题型科学探究题1Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
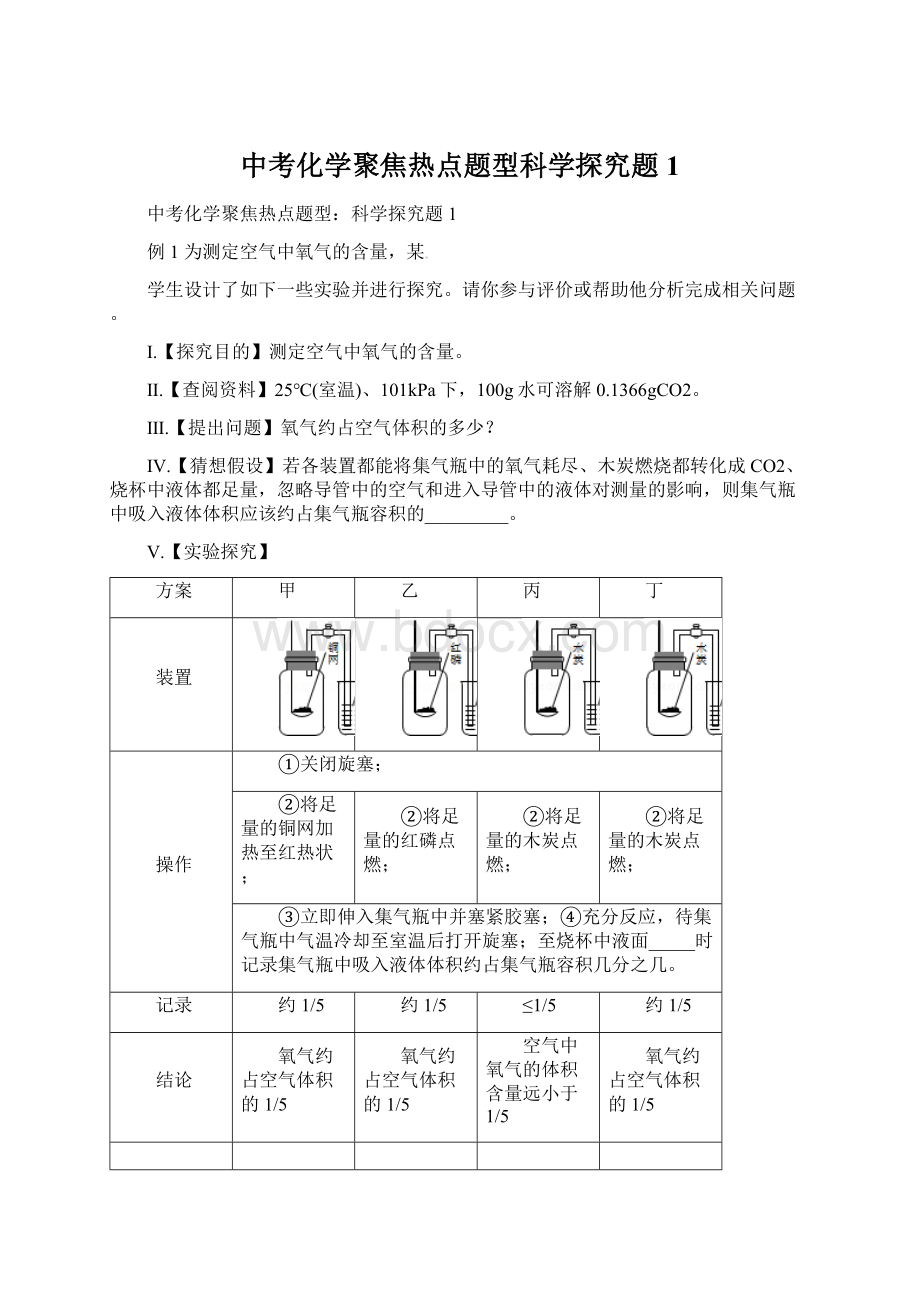
记录
约1/5
≤1/5
结论
氧气约占空气体积的1/5
空气中氧气的体积含量远小于1/5
Ⅵ.【反思交流】
(1)当集气瓶中气温未冷却至室温即记录集气瓶中吸入液体体积约占集气瓶容积的体积分数为a,当集气瓶中气温冷却至室温后再记录集气瓶中吸入液体体积约占集气瓶容积的体积分数为b,则a_________b(填“>”或“<”或“=”)。
(2)丁方案所测数据与猜想假设数据基本吻合的原因是_________(用化学方程式表示)。
(3)丙方案所测数据远小于1/5的主要原因是_________。
(4)以乙方案为例,试分析在测定过程中,对测定结果带来误差的因素可能有__________________(任答两点)。
解析由空气中氧气的含量可知,若各装置都能将集气瓶中的氧气耗尽、木炭燃烧都转化成CO2、烧杯中液体都足量,忽略导管中的空气和进入导管中的液体对测量的影响,则集气瓶中吸入液体体积应该约占集气瓶容积的1/5。
当瓶内的压强不再改变,不再吸入液体,烧杯中液面保持不变,
这时便可读数。
(1)当瓶内的压强偏高时,进入的液体偏少,所以a<b;
(2)由于二氧化碳能被氢氧化钠溶液吸收,瓶内的压强减小;
(3)丙方案所测数据远小于1/5的主要原因是CO2气体在水中的溶解度不大;
(4)在测定过程中,对测定结果带来误差的因素可能有:
装置气密性差、集气瓶中气温未恢复至室温就读数、可燃物红磷、木炭的量偏少等。
答案1/5保持不变
(1)<
(2)2NaOH+CO2=Na2CO3+H2O;
(3)CO2气体在水中的溶解度不大(4)装置气密性差、集气瓶中气温未恢复至室温就读数等
例2某兴趣小组同学为了探究干电池中物质的成分,将电池剖开时闻到异味且发现有黑色物质。
【提出问题】为什么有异味?
黑色物质的成分是什么?
【网络搜索】干电池的成分有二氧化锰、铁粉及铵盐等物质。
【实验设计】同学们分别设计实验进行探究。
实验Ⅰ:
小婧取适量黑色物质与___________混合置于研钵内研磨,嗅到氨味,再用湿润的石蕊试纸检测,试纸变蓝,证明黑色物质中含有铵盐。
实验Ⅱ:
小清用一种物理方法发现黑色物质中不含铁扮。
他采用的方法是_________。
实验Ⅲ:
小明将黑色物质加入适量的水中搅拌,静置后过滤,取滤渣进行实验。
实验步骤
实验现象
实验结论
①取适量黑色滤渣装入试管中,再加入过氧化氢溶液
_______________
有气体生成
②立即向试管中_______________
木条复燃
该气体是氧气
上述实验中产生氧气的化学方程式为_______________,据此小明认为黑色物质中一定含有二氧化锰。
【交流讨论】大家对小明的结论提出了质疑。
(1)小莹认为若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和__________在反应前后都没有发生变化;
(2)小仪认为除了小莹考虑的因素外,另一个原因是氧化铜等黑色物质对过氧化氢分解也有催化作用。
【结论与反思】
(1)干电池中一定含有铵盐,可能含有二氧化锰,一定不含有铁粉。
(2)面对网络信息,我们要去伪存真,不应盲从。
解析铵盐与碱混合会放出氨气,所以取适量黑色物质与熟石灰混合置于研钵内研磨,嗅到氨味,再用湿润的石蕊试纸检测,试纸变蓝,证明黑色物质中含有铵盐;
铁能被磁铁吸引,所以用物理方法发现黑色物质中不含铁扮,他采用的方法是用磁铁吸引;
二氧化锰和过氧化氢溶液混合会生成氧气,氧气具有助燃性,能使带火星的木条复燃;
二氧化锰能加快过氧化氢溶液分解生成氧气的速率,而本身的质量和化学性质不变,所以若要证明黑色物质中一定含有二氧化锰,必须验证二氧化锰的质量和化学性质。
答案氢氧化钙用磁铁吸引产生大量气泡伸入带火星的小木条2H2O2
2H2O+O2↑化学性质
二、中考化学推断题
2.A、B、C、D、E是初中化学常见的物质,其中物质B是重要的调味品,物质B、E、D中含有相同的非金属元素,物质A、B、C含有相同的金属元素,物质A、E属于盐,物质D属于酸,且物质A和D不能发生反应,用“一”表示物质之间能发生化学反应,用“→”表示一种物质能转化为另一种物质。
请回答下列问题:
(1)写出下列物质的化学式:
A_____,C_____,D_____,E_____;
(2)E→D反应的化学方程式为_____;
(3)A与E反应的实验现象为_____。
【答案】Na2SO4NaOHHClBaCl2BaCl2+H2SO4=BaSO4↓+2HCl溶液中产生白色沉淀
【解析】
【分析】
A、B、C、D、E是初中化学常见的物质,物质B是重要的调味品,所以B是氯化钠,物质B、E、D中含有相同的非金属元素,物质A、B、C含有相同的金属元素,物质A、E属于盐,物质D属于酸,且物质A和D不能发生反应,所以D是盐酸,E会转化成盐酸,会与A反应,所以A是E是氯化钡,A是硫酸钠,氯化钠会转化成C,C和硫酸钠可以相互转化,所以C是氢氧化钠,经过验证,推导正确。
【详解】
(1)经推导可得A是Na2SO4,C是NaOH,D是HCl,E是BaCl2;
(2)E→D的反应是氯化钡和硫酸反应生成硫酸钡沉淀和盐酸,化学方程式为:
BaCl2+H2SO4=BaSO4↓+2HCl;
(3)A与E的反应是氯化钡和硫酸钠反应生成硫酸钡沉淀和氯化钠,实验现象为:
溶液中产生白色沉淀。
【点睛】
本题为具有一定开放性的推断类问题,完成此题,关键是根据题目叙述找准解题的突破口,直接得出有关物质的化学式,并大胆进行假设,减少符合条件的物质范围,使思考简化,然后得出其他物质的化学式,带入验证即可。
3.A、B、C、D均含同一种元素,它们的转化关系如图。
A是白色难溶固体,相对分子质量为100,金属元素质量分数为40%;
C常作干燥剂;
D属于碱。
(“→”表示一种物质转化为另一种物质,部分反应条件、反应物及生成物已略去)请回答下列问题:
(1)A的一种用途是_____;
(2)B的化学式为_____;
(3)由C转化为D的化学方程式为_____;
(4)A、B之间的相互转化反应所属基本反应类型为_____。
【答案】补钙剂CaCl2CaO+H2O=Ca(OH)2复分解反应
A、B、C、D均含同一种元素,A是白色难溶固体,相对分子质量为100,金属元素质量分数为40%,所以A是碳酸钙,C常作干燥剂,所以C是氧化钙,D属于碱,氧化钙会生成D,所以D是氢氧化钙,氧化钙生成的B可以和碳酸钙互相转化,所以B是氯化钙。
(1)A是白色难溶固体,相对分子质量为100,金属元素质量分数为40%,所以A是碳酸钙,故A的一种用途是补钙剂。
(2)氧化钙会生成D,所以D是氢氧化钙,氧化钙生成的B可以和碳酸钙互相转化,所以B是氯化钙,故B的化学式为
。
(3)由C转化为D的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:
(4)A是碳酸钙,B是氯化钙,A、B之间的相互转化反应是碳酸钙和稀盐酸反应,所属基本反应类型为:
复分解反应。
A是白色难溶固体,相对分子质量为100,金属元素质量分数为40%,所以A是碳酸钙,C常作干燥剂,所以C是氧化钙。
4.五种物质之间的转化关系如图所示,回答下列有关问题:
(1)③反应的基本类型是_____。
(2)完成①转化中,可在Na2CO3溶液中加入的物质类别是_____(选填序号,A.氧化物B.酸C.碱D.盐)。
(3)写出转化中属于中和反应的化学方程式_____。
(4)⑧反应时一定发生的现象是_____;
若④反应出现蓝色沉淀,则反应的化学方程式是_____;
(5)①~⑧能够逆向转化的有_____(填序号)。
【答案】复分解反应BDNaOH+HNO3=NaNO3+H2O产生白色沉淀CuCl2+2NaOH=Cu(OH)2↓+2NaCl②⑤
(1)碳酸钠能与硫酸反应生成硫酸钠、二氧化碳和水,该反应是由两种化合物相互交换成分生成了两种新的化合物,属于复分解反应;
故填:
复分解反应;
(2)碳酸钠能与盐酸(属于酸)反应生成氯化钠、水和二氧化碳;
碳酸钠能与氯化钙(属于盐)反应生成氯化钠和碳酸钙白色沉淀;
BD;
(3)中和反应是指酸与碱作用生成盐和水的反应,即氢氧化钠与硝酸反应生成硝酸钠和水;
NaOH+HNO3=NaNO3+H2O;
(4)硫酸钠能与硝酸钡反应生成硫酸钡白色沉淀和硝酸钠,所以会观察到有白色沉淀产生;
氢氧化钠能与氯化铜反应生成氢氧化铜蓝色沉淀和氯化钠;
产生白色沉淀;
CuCl2+2NaOH=Cu(OH)2↓+2NaCl;
(5)碳酸钠能与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠;
硫酸钠能与氢氧化钡反应生成硫酸钡白色沉淀和氢氧化钠;
②⑤。
5.图中A~H是初中化学常见的物质,且分别由一种或两种元素组成。
D中两种元素的质量比为4︰1,固态E可用于人工降雨,F为磁铁矿的主要成分。
图中“—”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。
(1)写出化学式:
E_______。
(2)写出化学方程式:
C→B_______________,F与H_____________,A与D________。
【答案】CO22H2+O2
2H2O2C+Fe3O4
3Fe+2CO2↑CuO+2HCl=CuCl2+2H2O
根据题目中的信息,题中所有的物质都是由一种或两种元素组成的,固态E可用于人工降雨,可知固态E是干冰,则E为:
CO2,F为磁铁矿的主要成分,则K是Fe3O4,D是CuO,A和CuO能反应,且A能转化为CO2,所以A是HCl,HCl、Fe3O4能转化为B,B能和CO2反应,因此B是H2O。
C能和Fe3O4反应,能生成H2O,因此C是H2。
D、E、F都能和H反应,因此H是C,故G是Fe。
(1)由分析知,E的化学式为:
CO2;
(2)C转化为B,即氢气在氧气中燃烧生成水,C→B的方程式为:
2H2+O2
2H2O;
F与H是碳将四氧化三铁还原生成铁和二氧化碳,反应方程式为:
2C+Fe3O4
3Fe+2CO2↑;
A与D是氧化铜和盐酸反应生氯化铜和水,方程式为:
CuO+2HCl=CuCl2+2H2O;
解题的关键是根据物质的性质推断出各物质。
6.如图中表示中学几种常见的物质在一定条件下可以转化,A是石灰石的主要成分,E、G为黑色的粉末,C为无色液体,H为紫红色固体。
(部分条件省略)
C_____B_____G_____。
(2)CO2通入D澄清溶液的化学反应方程式是_____。
【答案】H2OCaOCuOCO2+Ca(OH)2═CaCO3↓+H2O
A是石灰石的主要成分,所以A是碳酸钙,碳酸钙高温会生成氧化钙和二氧化碳,所以B是氧化钙,C为无色液体,可以和氧化钙反应产生D,所以C是水,D是氢氧化钙,氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,E、G为黑色的粉末,E和二氧化碳反应产生F,F和G反应产生二氧化碳和H,H为紫红色固体,所以E是碳,F是一氧化碳,一氧化碳和氧化铜反应产生铜和二氧化碳,所以H为铜,G是氧化铜。
(1)A是石灰石的主要成分,所以A是碳酸钙,碳酸钙高温会生成氧化钙和二氧化碳,所以B是氧化钙,C为无色液体,可以和氧化钙反应产生D,所以C是水,化学式为
;
B是氧化钙,化学式为
,G是
(2)CO2通入D澄清溶液的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式是:
A是石灰石的主要成分,所以A是碳酸钙,碳酸钙高温会生成氧化钙和二氧化碳,所以B是氧化钙,C为无色液体,可以和氧化钙反应产生D,所以C是水,D是氢氧化钙,E、G为黑色的粉末,E和二氧化碳反应产生F,F和G反应产生二氧化碳和H,H为紫红色固体,所以E是碳,F是一氧化碳。
7.如图是初中化学中常见化合物间的转化关系,其中A在常温下是液体,F是人体胃液中助消化的酸,E常用来改良酸性土壤,A和B在不同的条件下会发生不同的化学反应。
图中“—”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。
(1)写出物质的化学式:
A_____,B_____。
(2)B和G之间发生反应的化学方程式为_____。
(3)G和F之间的反应属于基本反应类型中的_____反应。
(4)C物质的一种用途是_____。
【答案】H2OCO2CO2+2NaOH=Na2CO3+H2O复分解建筑材料(或补钙剂等)
A在常温下是液体,则A可能是水;
F是人体胃液中助消化的酸,则F是盐酸;
再由A(水)和B在不同的条件下会发生不同的化学反应”,可知B为二氧化碳,因为二氧化碳能与水反应生成碳酸,另外,二氧化碳和水在植物光合作用下能反应转化成葡萄糖和氧气;
由于A(水)还能和D反应,则D为氧化钙;
又D能转化为E,且E能和F盐酸反应,则E为氢氧化钙,符合E常用来改良酸性土壤的说法;
再结合图示可知,G能分别与B二氧化碳、F盐酸反应,则G为碱液(如氢氧化钠);
由于C能转化生成D(氧化钙)或A(水)或B(二氧化碳),故C为碳酸钙,带入框图,推断合理。
(1)由分析知AB是水和二氧化碳,化学式为:
H
2
O、CO2;
E是氢氧化钙,F是盐酸,盐酸能与氢氧化钙反应生成氯化钙和水,反应的方程式为:
Ca(OH)2+2HCl=CaCl2+2H2O;
(2)B是二氧化碳,G是氢氧化钠,两者反应的方程式为:
CO2+2NaOH═Na2CO3+H2O;
(3)G是氢氧化钠,F是盐酸,该反应的基本类型属于复分解反应;
(4)C是碳酸钙,可以用作建筑材料。
8.A、B、C、D、E是常见的不同类别的物质,它们之间的转化及反应关系如图所示(部分反应物、生成物及反应条件未标出,“→”表示转化关系,“一”表示相互能反应)。
人体缺乏A元素会引起贫血,B溶液呈蓝色且可用于配制波尔多液,B和D含有相同的阴离子。
(1)C应是化合物中的_____类;
E的化学式是_____。
(2)A与B溶液反应后,溶液的质量_____(填“增大”“减小”或“不变”)。
(3)C﹣D反应的化学方程式可能是_____。
【答案】碱H2O减小2NaOH+H2SO4=Na2SO4+2H2O
根据题目给出的流程图和信息:
A、B、C、D、E是常见的不同类别的物质,人体缺乏A元素会引起贫血,因此A是铁;
B溶液呈蓝色且可用于配制波尔多液,因此B是硫酸铜;
B和D含有相同的阴离子,因此D是硫酸;
硫酸铜和氢氧化钠反应生成氢氧化铜蓝色沉淀和氢氧化钠,因此C是氢氧化钠。
硫酸和氢氧化钠都能转化成E,因此E是水。
(1)氢氧化钠属于碱,因此C是碱类;
故答案为:
碱;
H2O;
(2)A是铁,B是硫酸铜,铁和硫酸铜反应生成硫酸亚铁和铜,铁的相对原子质量小于铜,因此溶液的质量减小;
减小;
(3)氢氧化钠和硫酸反应生成硫酸钠和水,配平即可;
2NaOH+H2SO4=Na2SO4+2H2O。
在书写中和反应的化学方程式时要注意水分子前的系数。
9.甲、乙、丙、丁是常见的化合物,它们有如图所示转化关系(部分物质已略去),甲是实验室常用燃料,其相对分子质量为46的有机物;
乙是最常见的溶剂;
丁是白色难溶固体,可做补钙剂。
则甲的化学式为_____;
反应③的化学方程式为_____;
试剂A中溶质在生产或生活中的一种用途是_____。
【答案】C2H5OHCaCO3+2HCl=CaCl2+H2O+CO2↑改良酸性土壤
甲、乙、丙、丁是常见的化合物,甲是实验室常用燃料,相对分子质量为46的有机物,所以甲是酒精,酒精和氧气在点燃的条件下生成水和二氧化碳,乙是最常见的溶剂,所以乙是水,丙是二氧化碳,丁是白色难溶固体,可做补钙剂,所以丁是碳酸钙,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,A是氢氧化钙,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以B是盐酸。
将猜想代入框图进行检验,猜想成立。
根据以上分析可知:
甲是酒精,化学式为:
C2H5OH,反应③是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑,试剂A中溶质在生产或生活中的一种用途是:
改良酸性土壤。
在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
10.A﹣E是初中常见物质,有如图所示的关系,其中A是单质,B是生活中常用的调味品,C是红色固体,E俗称小苏打.图中“﹣”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.(部分反应物、生成物及反应条件略去).回答下列问题:
(1)写出B物质的化学式:
B______.
(2)分别写出C与D、D与E反应的化学方程式______________________、_____________________。
(3)由C转化为A的原理在工业上常用于____。
【答案】NaClFe2O3+6HCl=2FeCl3+3H2ONaHCO3+HCl=NaCl+H2O+CO2↑炼铁
B是生活中常用的调味品,故B是氯化钠,E俗称小苏打,E是碳酸氢钠,D能与碳酸氢钠反应,能生成氯化钠,故D是稀盐酸,C是红色固体,能生成单质A,且能与稀盐酸反应,故C是氧化铁,A是铁,经检验,推理合理。
(1)由分析可知,B是氯化钠,化学式为:
NaCl。
(2)氧化铁与稀盐酸反应生成氯化铁和水,反应的方程式为:
Fe2O3+6HCl=2FeCl3+3H2O;
稀盐酸与碳酸氢钠反应生成氯化钠、二氧化碳和水,反应方程式为:
NaHCO3+HCl=NaCl+H2O+CO2↑
(3)氧化铁转化为铁工业上长用于炼铁。