化学方程式的简单计算教案Word文档下载推荐.docx
《化学方程式的简单计算教案Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《化学方程式的简单计算教案Word文档下载推荐.docx(14页珍藏版)》请在冰豆网上搜索。
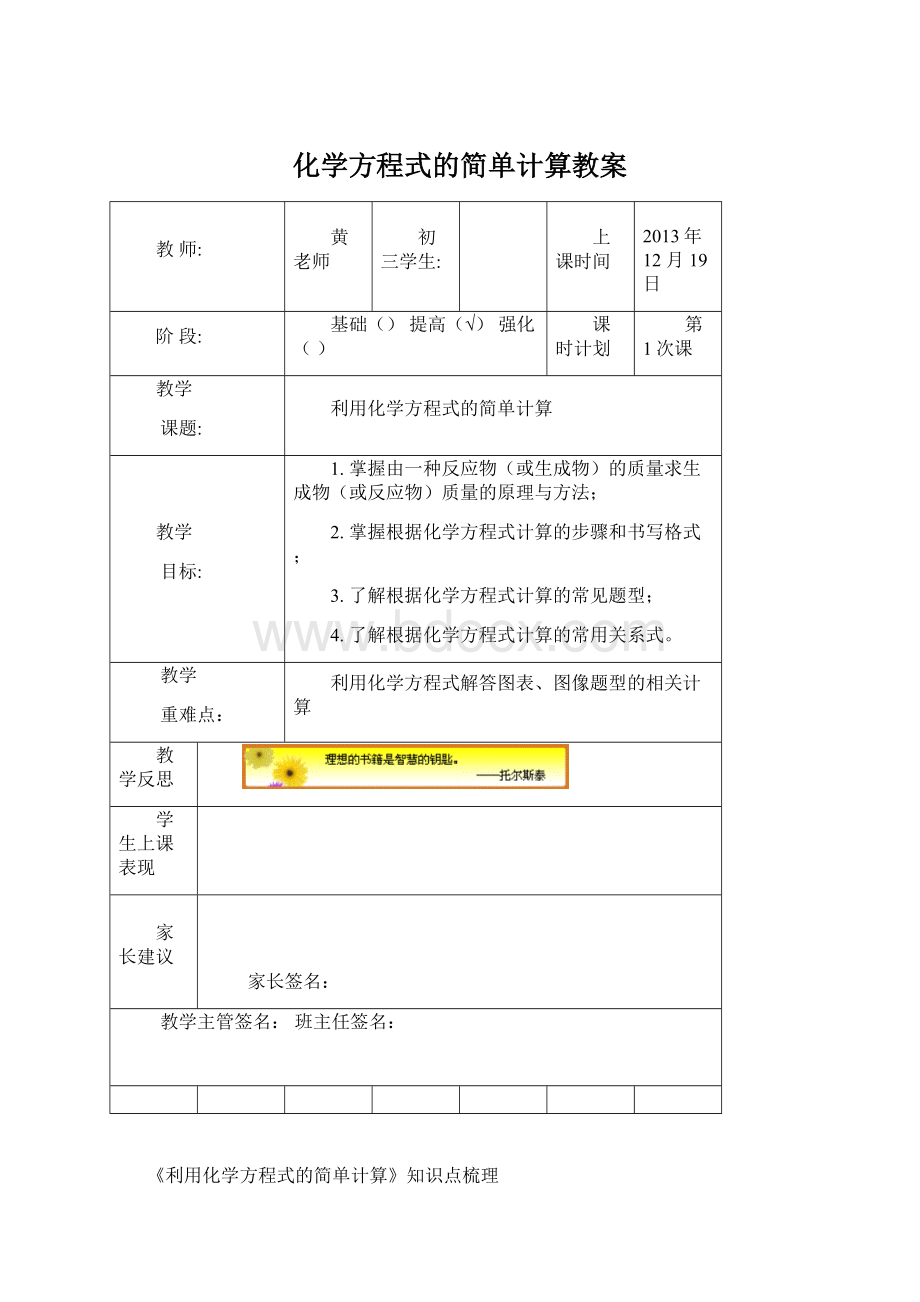
解:
设可生成氧化镁的质量为X
(1)设未知数…………设
(2)写出化学方程式……方
4880(3)写出有关物质的式量、
3gX已知量和未知量……关
(4)列比例式,求解……比
………………………算
=5g(5)简明地写出答案……答
答:
3克镁在氧气中充分燃烧可生成氧化镁5克。
(3)根据化学方程式计算应该注意的事项
①正确书写化学方程式,准确列出有关反应物或生成物的质量比;
②列式时,各物质的质量单位必须统一,对应关系要正确;
③反应物、生成物都必须是纯净物,如果是混合物,应该将不纯物的质量按题意转化为纯净物的质量;
④解题的过程要完整,规范
⑤设未知数是要指明物理量,不要带单位。
⑥.相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。
⑦.计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
【小试牛刀】取氯酸钾和二氧化锰的混合物15.5克,放入一大试管中加热,反应完全后冷却到反应前温度,称残余固体质量为10.7克。
求生成氧气多少克?
生成氯化钾多少克?
知识点2:
常见的计算类型:
(1)利用化学方程式的简单计算;
(2)涉及到气体体积的计算
(3)有关含杂质物质的化学方程式的计算;
(4)质量守恒定律结合化学方程式的综合计算。
(5)表格式的有关化学方程式的计算
(6)图像式的有关化学方程式的计算
有关计算公式:
①纯净物的质量=不纯物的质量×
纯净物的质量分数=不纯物的质量×
(1-杂质的质量分数)
②不纯物总质量中含有纯净物的质量分数(纯度):
③一定体积的气体换算成一定质量的气体:
气体的体积=气体的质量/气体的密度。
解题思路:
①审题:
认真阅读题目,反复推敲关键字句,准确理解题意。
②析题:
运用所学知识剖析题目,理清层次,挖掘隐含信息,排除干扰条件,分析已知和待求。
明确物质间关系,寻找解题突破口。
③解题:
解题时要做到思路清楚,方法正确,步骤清晰(设未知、写化学方程式、找关系量、列比例式、求未知、写答案),计算准确,书写规范。
④验题:
检查所用条件是否符合题意,是否全部解出所求问题,单位是否统一,计算是否正确等。
例2:
在一个密闭容器内有四种物质A、B、C、D,在高温条件下发生反应,一段时间后测得反应前后各物质质量如下表所示,如果A的相对分子质量为2N,D的相对分子质量为3N,则该反应的化学反应方程式中A与D的化学计量数之比为
A
B
C
D
反应前质量(g)
8
10
1
15
反应后质量(g)
未测
24
2
6
A.1:
1B、1:
2C、1:
3D、2:
3
【解析】本题是根据化学方程式进行简单计算的综合题,首先要根据表中内容判断反应物是什么和生成物是什么,然后根据质量关系来判断A与D的化学计量数之比。
根据表中数据可知,B和C为生成物,而D为反应物,再根据质量守恒定律可知A减少的质量为6g,故A也为反应物,写出化学反应方程式为:
xA+yD=mB+nC,最后根据A与D的质量关系计算它们的化学计量数之比)
【答案】A
【小试牛刀】为了测定实验室中氯酸钾样品的纯度,某学习小组取2.5g该样品与0.5g二氧化锰混合,加热该混合物t1时间后(假设杂质不参加反应),冷却,称量剩余固体的质量,重复以上操作,依次称得加热t1、t2、t3、t4时间后剩余固体的质量,记录数据如下表:
加热时间
t1
t2
t3
t4
剩余固体质量/g
2.48
2.34
2.04
请仔细分析实验数据,回答下列问题:
(1)在________时间后,该样品中的氯酸钾已经完全反应
(2)完全反应后产生氧气的质量
(3)该样品中氯酸钾的质量分数
例3:
下图是实验室用高锰酸钾制取氧气随时间的变化关系图,与该反应事实相吻合的是()
【小试牛刀】一定量的木炭与过量的氧气在密闭容器内加热使其充分反应,下图中能正确反映容器内有关的量随时间变化关系的图像是()
【总结】化学方程要配平,需将纯量代方程;
关系式对关系量,计算单位不能忘;
关系量间成比例,解设比答需完整。
【及时检测】
1.制取71克五氧化二磷,需要磷_______克,需要烧氧气_______克(
)
A.30克30克
B.30克40克
C.31克40克
D.40克31克
2.在2X+Y2=2Z的反应中,X的相对原子质量为24,Y2的相对分子质量为32,Z的相对分子质量为()
A.32B.40C.56D.64
3.相同质量的下列物质在氧气中完全燃烧,消耗氧气最多的是()
A.PB.SC.CD.H2
4.将25gA与5gB发生反应,所得混合物中含有10A,11gC,还有另外一种物质D。
A、B、C、D相对质量分别为30、20、44、18,则它们之间反应的化学方程式正确的是()
A.A+B=C+DB.2A+B=2C+DC.2A+B=C+2DD.A+2B=2C+D
5.一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表。
下列说法中正确的是( )
A.X=7g B.在该反应中,丙物质一定做催化剂
C.该反应是分解反应 D.在该反应的化学方程式中,丙、丁的化学计量数之比为1∶l
物质
甲
乙
丙
丁
反应前质量
8g
35g
5g
反应后质量
2g
X
42g
6.镁带在耐高温的密闭容器(内含空气)内加热,容器内有关的量随时间变化的图像正确的是( )
7.镁在空气中燃烧,生成氧化镁,其固体质量变化
可用图表示,则(80-48)克表示的质量为:
()
A.生成物MgO的质量
B.参加反应O2的质量
C.参加反应的镁的质量
D.生成物MgO与参加反应的O2的质量和
8.下图为某反应的微观模拟示意图。
从图中
获得的有关信息不正确的是()
A.分子是化学变化中的最小粒子
B.化学反应前后原子的数目没有增减
C.该化学反应属于分解反应
D.分子间存在一定的间隔
9.将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
下列判断正确的是()
丙醇
氧气
水
二氧化碳
反应前质量/g
6.0
12.8
反应后质量/g
7.2
8.8
a
A.表中a的值为2.8B.X一定是该反应的催化剂
C.表中a的值为2.4D.若起始时氧气的质量是14.4g,则无X生成
10.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质
Y
Z
Q
反应前质量/g
84
5
反应后质量/g
待测
14
试推断该密闭容器发生的化学反应基本类型为()
A.分解反应B.化合反应C.置换反应D.以上三种反应均有可能
11、根据已知填空
化学方程式
C+O2
CO2
各物质质量比
12()44
已知所求
6g()g()g
12.电解水的化学方程式为____________________;
填写下表
反应物
生成物
H2O
O2
质量比
18克
2克
8克
64克
由上表可知:
在化学反应中:
(1)任何一个化学反应都遵循__________________。
(2)不管反应物和生成物质量是多少,各物质的质量比__________(填相同或不同)。
13.凯尔将6g镁分别与不同质量的氧气反应,试将生成氧化镁的质量填入下表,并回答:
氧气质量(g)
生成氧化镁质量(g)
4
12
(1)当第一次与2g氧气反应时,为什么不能生成8gMgO?
_______________________________
(2)从第二次以后,为什么不断增加氧气的质量,生成MgO的质量却不增加?
___________________________________
14.下面是某位同学做的一道计算题,请指出他的错误:
题目:
3.25gZn和足量的盐酸反应制取H2,问可制得H2的质量是多少?
设可得H2的质量为xg。
Zn+HCl=ZnCl+H2↑
651
3.25gx
65∶1=x∶3.25gx=
可制得H2211.25g。
(1);
(2);
(3);
(4)。
15.加热122.5g氯酸钾使之完全分解,可生成氧气多少克?
16.为了测定实验室中高锰酸钾样品的纯度(杂质不参加反应),取16g该样品加热,完全反应后,得到1.6g氧气,求样品中高锰酸钾的质量分数。
17.把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示:
第一次
第二次
第三次
O2质量/g
SO2质量/g
(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是。
(2)请你通过计算求出:
第二次实验生成二氧化硫多少克?
(3)在表中填写第三次实验生成二氧化硫的质量。
18.由干燥的氯酸钾和二氧化锰组成的固体混合物的质量为30g,把该固体混合物放入大试管中加热,完全反应后,冷却到反应前的温度,称得试管中固体物质的质量为20.4g.
(1)此反应的化学方程式为。
(2)制得氧气的质量是。
(3)原固体混合物中二氧化锰的质量是。
【作业】
1.在化学反应X+Y====Z中,3gX和足量Y充分反应后生成8gZ,则参加反应的Y的质量为()
A.2.5gB.3gC.5gD.6g
2.在2A+B==2C反应中,已知A的相对分子质量为24,C的相对分子质量为40,则B的相对分子质量为()
A.16gB.32gC.16D.32
3.A、B、C三种物质各15g,它们化合时只能生成30g新物质D。
若增加10gA,则反应停止后,原反应物中只余C。
根据上述条件推断下列说法中正确的是
A.第一次反应停止后,B剩余9gB.第二次反应后,D的质量为50g
C.反应中A和B的质量比是3∶2D.反应中A和C的质量比是5∶2
4.在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
下列说法正确的是(
B
111
A.该闭容器中发生的化学变化属于分解反应
B.密闭容器中发生的化学变化属于化合反应
C.该反应中A、B、C、D四种物质(参加反应或生成)的质量比为26∶9∶111∶80
D.反应后密闭容器中A的质量为22g
5.(2008南京市)在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9∶22.若2.6gA与B完全反应后.生成8.8gD。
则在此反应中B与D的质量比为()
A.4∶9B.8∶1C.10∶11D.31∶44
6.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:
下列说法错误的是
20
22
11
28
A该反应是分解反应B甲可能是该反应的催化剂
C乙、丙变化的质量比为9:
8D反应后甲的质量为0g
7.在反应X+Y=R+2M中,当1.6gX与Y完全反应,生成4.4gR,且反应生成的R和M的质量之比为11:
9,则在此反应中Y和M的质量之比是()
A.23:
9B.16:
9C.32:
9D.46:
9
8.在反应2A+B=3C+D中,A和B的相对分子质量之比为5:
1,已知20gA与一定量B恰好完全反应,生成5gD,则在此此反应中B和C的质量比为()
A.4:
19B.3:
5C.1:
3D.2:
17
9.在一个密闭容器中,甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质的质量如下表:
58
27
19
则该密闭容器中发生的化学反应类型为()
A.分解反应B.化合反应C.置换反应D.复分解反应
10.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表,下列说法中不正确的是()
25
21
9
A.该反应为分解反应B.该反应遵守质量守恒定律C.X中未测值为零D.若Q为氧气,则该反应为氧化反应
11.在一个密闭容器中有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
40
23
下列说法正确的是()
A.该反应一定是置换反应B.Y、Q的相对分子质量之比一定为11:
C.参加反应的X、Z的质量比为1:
4D.反应后X的质量为0
12.在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:
则下列表述正确的是()
A.未测值为3gB.丙一定是催化剂
C.乙全部参与了反应D.甲与乙反应的质量比为14:
13.密闭容器内有A、B、C、D四种物质,在一定条件下完全反应,测得反应前后各物质的质量如下:
下列说法正确的是()
前/g
19.7
8.7
31.6
0.4
后/g
17.4
3.6
A.物质C一定是化合物,物质D可能是单质
B.反应后密闭容器中A的质量为19.7g
C.反应过程中,物质B与物质C的相对分子质量比为87:
36
D.若物质A与物质C的相对分子质量之比为197:
158,则化学方程式中A与C的化学计量之比为1:
14.电解10克水,能得到氢气_______克,氧气_______克。
15.现有25gKClO3与MnO2的混合物充分反应后,剩余15.4g,求混合物中二氧化锰的质量和质量分数各是多少.
16.实验室要制取4.8克氧气,至少需分解多少克高锰酸钾?
17..中国登山协会为纪念我国首次攀登珠穆朗玛峰成功50周年再次组织攀登,阿旺扎西等一行登山运动员于2003年5月21日13:
40成功登顶。
在登山过程中,人均携带10Kg的氧气,若实验室用高锰酸钾为原料,制取相同质量的氧气,需多少千克的高锰酸钾?
18..已知,火箭升空至少要携带100kg的液氢,充分燃烧才能获得足够的量。
你会在火箭助燃仓中填充多少千克的液氧来满足这些液氢的完全燃烧?
19..高温煅烧碳酸钙生成氧化钙和二氧化碳;
如果要制
得生石灰56克,则需要多少克碳酸钙,同时可生成多
少克二氧化碳?
二氧化碳的体积是多少?
(已知:
二氧化碳的密度为2克/升)
20.已知:
化学反应2A+3B=2C+2D
①已知4gA与9gB恰好完全反应,生成5gC,则生成D的质量为;
A与C的质量比为。
②已知A和B参加反应的质量比4:
9,共生成130g物质,则参加反应的A的质量为。
③已知:
B、C、D的相对分子质量依次为30、25、40,则Mr(A)=。
④已知:
4gA与9gB恰好完全反应,生成5gC,Mr(A)=20,则Mr(D)=。