高一化学第三章之必做好题四Word格式.docx
《高一化学第三章之必做好题四Word格式.docx》由会员分享,可在线阅读,更多相关《高一化学第三章之必做好题四Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
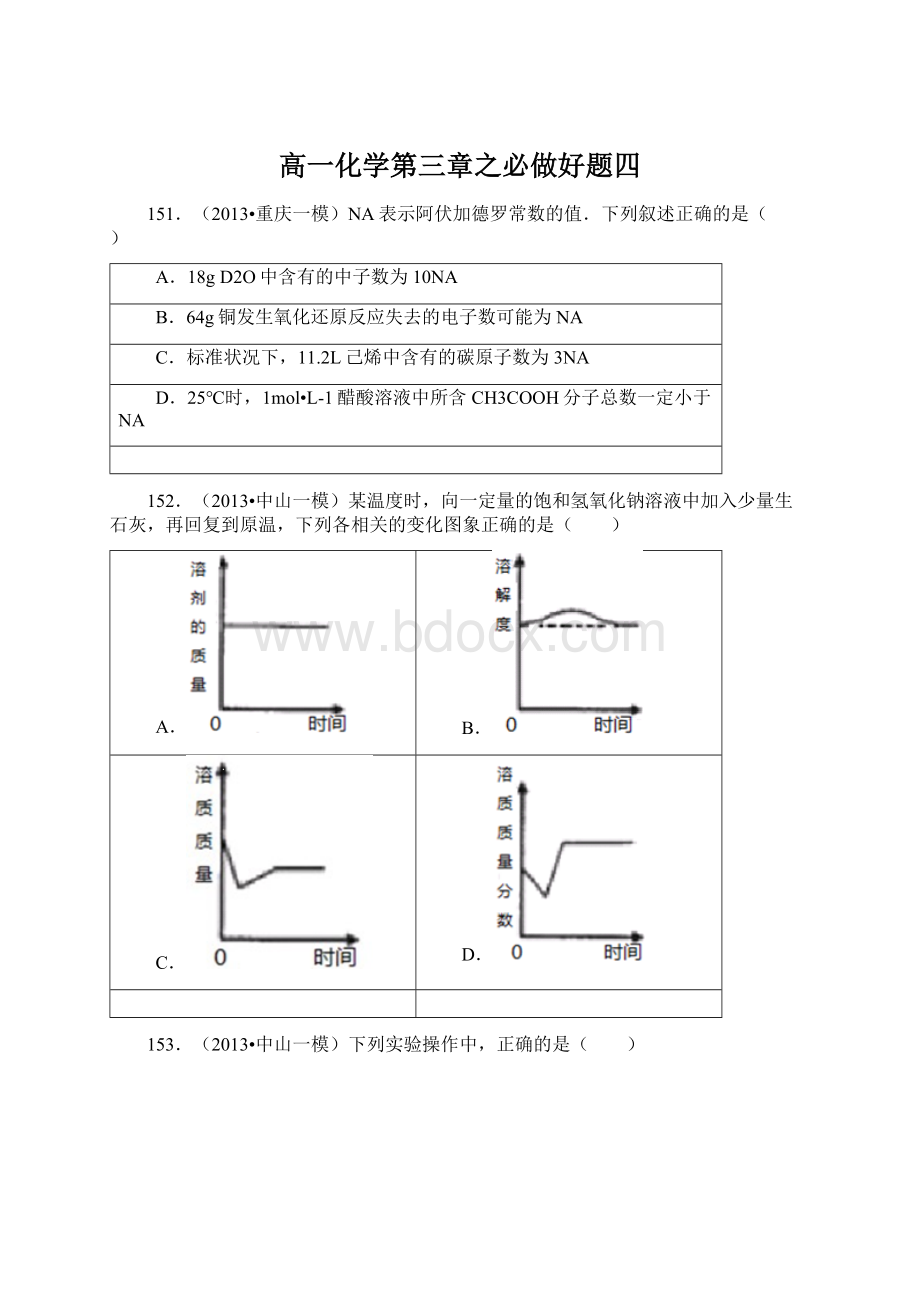
B.22.4L2H2O中所含的中子数为10NA
C.100mL
1mol•L-1AlCl3溶液中含的阳离子数大于0.1NA
D.78g的Na2O2含阴离子2NA
157.(2013•闸北区二模)FeS2在空气中充分燃烧的化学方程式为4FeS2+11O2
高温
2Fe2O3+8SO2,若a
g
FeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为( )
A.120N/a
B.120a/11N
C.11a/120N
D.120N/11a
158.(2013•闸北区二模)对下列装置,不添加其他仪器无法检查气密性的是( )
159.(2013•闸北区二模)下列实验用酸性KMnO4溶液不能达到预期目的是( )
A.鉴别SO2和CO2
B.检验硫酸铁溶液中是否有硫酸亚铁
C.鉴别苯和对二甲苯
D.检验CH2=C(CH3)CHO中含碳碳双键
160.(2013•闸北区二模)如图装置可用于收集气体并验证其化学性质,
气体
试剂
现象
结论
A
NO
紫色石蕊试液
溶液变红
NO与水反应生成硝酸
B
Cl2
NaBr溶液
溶液呈橙黄色
氯的非金属性大于溴
C
SO2
酸性KMnO4溶液
溶液褪色
SO2有漂白性
D
NH3
MgCl2溶液
产生白色沉淀
NH3有碱性
下列对应关系完全正确的是( )
A.A
B.B
C.C
D.D
161.(2013•枣庄一模)下列关于实验操作的叙述正确的是( )
A.用四氣化碳萃取溴水中的溴时,将溴的四氣化碳溶液从分液漏斗下口放出
B.用氢氧化钠溶液滴定盐酸的实验中,可通过旋转玻璃活塞调节滴定速率
C.在配制一定物质的量浓度溶液的实验中,若定容时加水超过刻度线应立即用滴管吸
出少量水
D.用玻璃棒蘸取溶液滴到放在洁净表面皿上用蒸锻水润湿的pH试纸上,测溶液的PH
162.(2013•烟台一模)下列实验操作能使实验结果偏低的是( )
A.用蒸馏水润湿的pH试纸所测定的某酸溶液的pH
B.用容量瓶配制溶液,定容后摇匀液面下降,再加蒸馏水至刻度线所配制的溶液浓度
C.用仰视量筒刻度量取的一定量浓硫酸所配制的0.1mol•L-1H2SO4溶液的浓度
D.用待测液润洗的锥形瓶进行中和滴定所测定的待测液浓度
163.(2013•烟台模拟)下列叙述中正确的是( )
A.1L1.0mol•L-1的盐酸中含有6.02×
1023个HCl分子
B.1L1.0mol•L-1的FeCl3溶液中Fe3+所带电荷总数为3×
6.02×
1023个
C.Na2O2与水反应转移6.02×
1023个电子时,生成11.2LO2(标准状况)
D.配制1L0.10mol•L-1硫酸铜溶液,可将25.0gCuSO4•5H2O溶于1.0L水中
164.(2013•烟台模拟)仅用下表提供的仪器(夹持仪器和试剂任选)不能实现相应实验目的是( )
选项
实验目的
仪器
除去氢氧化铝胶体中的泥沙
漏斗(带滤纸)、烧杯、玻璃棒
从食盐水中获得NaCl晶体
坩埚、玻璃棒、酒精灯、泥三角
用0.1000mol•L-1的盐酸测定未
知浓度的NaOH溶液浓度
碱式滴定管、酸式滴定管、锥形瓶、胶头滴管、烧杯
用MnO2和浓盐酸制取干燥、纯
净的Cl2
圆底烧瓶、分液漏斗、酒精灯、洗气瓶、集气瓶、导管、石棉网
165.(2013•烟台模拟)下列与实验有关的叙述不正确的是( )
A.液溴保存时应加少量水并盛放在用玻璃塞塞紧的试剂瓶中
B.某气体通入品红溶液褪色,加热溶液又变红,该气体为SO2
C.配制硫酸亚铁溶液,可将绿矾晶体溶于蒸馏水并加入一定量的稀硫酸和铁屑
D.某溶液中加盐酸产生使澄清石灰水变浑浊的无色气体,则该溶液一定含CO2+3知
166.(2013•徐州三模)设NA为阿伏加德罗常数的值.下列说法正确的是( )
mol金刚石中含有的共价键数目为2NA
B.标准状况下,11.2
L甲醛中含有的氧原子数目为NA
C.1
0.1
mol•L-1
CH3COONa溶液中含有的阴离子总数为0.1NA
D.0.1
Na2O2与足量水完全反应时,转移的电子数目为0.2NA
167.(2013•无锡一模)设NA为阿伏加德罗常数的值,下列说法正确的是( )
mol•L-1的氨水中含有的NH3分子数为0.1NA
L的CCl4中含有的CCl键数为0.4NA
C.常温常压下,3.0
g葡萄糖和冰醋酸的混合物中含有的原子总数为0.4NA
D.标准状况下,Na2O2与足量CO2反应生成2.24
O2,转移电子数为0.4NA
168.(2013•无锡二模)设NA为阿伏加德罗常数的值.下列说法一定正确的是( )
A.25℃,pH=13的NaOH溶液中含有OH-为0.1
B.1
mol•L-1CuSO4溶液中含有Cu2+为0.1
C.2.24LN2和NH3混合气体中原子间含有的共用电子对数目为0.3NA
D.2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA
169.(2013•潍坊一模)以NA表示阿伏加德罗常数,下列说法正确的是( )
A.常温常压下,46gN02与N204的混合气体中含有的原子数为3NA
B.15.6
Na2O2与过量CO2反应时,转移的电子数为O.4NA
C.常温常压下,11.2L
二氧化硫中所含的氧原子数等于NA
D.1L
1
的Na2CO3溶液中含有NA个CO32-
170.(2013•潍坊模拟)下列实验能达到预期目的是( )
A.将含有SO2的CO2气体通过足量的饱和Na2CO3溶液以除去SO2
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜和镁的金属活动性强弱
C.称取19.0g氯化亚锡(SnCl2),用100mL蒸馏水溶解,配制1.0mol/L
SnCl2溶液
D.测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱
171.(2013•天河区一模)一定条件下,仅由氯化钠的水溶液肯定不能制得的是( )
A.NaOH
B.H2
C.HCl
D.Na2SO4
172.(2013•天河区一模)正确的实验操作对实验结果、人身安全非常重要.下列实验操作正确的是( )
液体加热
检查装置气密性
倾倒液体
浓硫酸稀释
173.(2013•天河区一模)下列说法错误的是( )
A.通过过滤的方法可以将硬水软化
B.保持水的化学性质的最小粒子是水分子
C.墙内开花,墙外香,说明分子是不断运动的
D.可以用含小苏打的发酵粉焙制糕点
174.(2013•天河区一模)下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
物质
所含杂质
除去杂质的方法
CO2
O2
通过灼热的铜网
KOH溶液
K2CO3
加入足量稀盐酸至不再产生气泡
NaCl
CaCO3
溶解、过滤、蒸发
H2
H2O
通过浓H2SO4
175.(2013•泰州二模)设NA为阿伏加德罗常数的值.下列叙述错误的是( )
A.常温常压下,0.17g
NH3中含有的共用电子对数为0.1NA
B.常温常压下,1
pH=1的稀H2SO4中含有的氢离子数为0.1NA
C.标准状况下,2.24
Cl2与足量稀NaOH反应转移电子数为0.1NA
D.10
g由CaCO3与KHCO3组成的混合物中含有的碳原子数为0.1NA
176.(2013•泰安三模)下列有关物质除杂的方法中可行的是( )
A.除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤
B.除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液
C.已知:
Ksp(CuS)<Ksp(FeS),可加入过量的难溶电解质FeS,使水中少量的Cu2+转化成硫化物沉淀而除去
D.向含有少量的FeBr2的FeCl2溶液中,加入适量氯水,再加CC14萃取分液,以除去FeC12溶液中的FeBr2
177.(2013•松江区二模)如图所示实验装置测定气体摩尔体积,相关叙述正确的是( )
A.用CCl4代替水,测得氢气的体积更准确
B.量气管压入漏斗的水过多而溢出,会导致测定失败
C.必须待体系温度降低到0℃时才可进行读数
D.上提水准管,量气管液面高度不断改变,说明装置漏气
178.(2013•松江区二模)利用下列各组物质制备和收集少量相应气体,能采用如图实验装置的是( )
A.浓氨水与固体CaO
B.FeS与稀硫酸
C.稀硝酸与铜片
D.电石与水
179.(2013•深圳一模)NA代表阿伏加德罗常数.下列叙述正确的是( )
A.标准状况下,22.4L己烷中C-C共价键数目为5NA
B.0.1mol•L-1AlCl3溶液中含有氯离子数为0.3NA
C.1molFe在1molCl2中充分燃烧,转移电子数为3NA
D.20g重水(
2
1
H2O)所含的电子数为10NA
180.(2013•深圳一模)下列实验方法正确的是( )
A.除去NaCl溶液中的Cl2,可加入酒精后分液
B.滴定管用蒸馏水洗净后,直接装入标准浓度的溶液滴定
C.用排水法收集稀HNO3和Cu反应产生的NO气体
D.用KSCN溶液和氯水鉴别FeCl3溶液中是否含有FeCl2
181.(2013•深圳二模)用NA表示阿伏加德罗常数,下列说法正确的是( )
A.常温常压下,4.4g
CO2和4.4g
N2O的原子总数都是0.3NA
B.次氯酸光照分解产生22.4mL气体(标准状况下),转移电子数为0.002NA
C.常温下,4.6g乙醇含有C-H键总数为0.6
D.0.2
mol•L-1FeCl3溶液中含有Cl-总数为0.6NA
182.(2013•深圳二模)下列实验正确的是( )
A.用量筒量取15.50mL
0.100
mol•L-1盐酸
B.用无水酒精萃取碘水中的碘
C.用过量浓氨水洗涤试管内的银镜
D.做H2还原CuO实验时,要先通氢气,验纯后再加热
183.(2013•绍兴一模)下列有关说法正确的是( )
A.食醋中总酸含量测定实验中,盛放NaOH溶液的滴定管排除气泡的方法是直接放液
B.用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在有机溶剂中的溶解能力较Cu2+小
C.在分液漏斗的检漏操作时,先向分液漏斗中加少量水,检查旋塞芯处是否漏水,然后将漏斗倒转过来,检查玻璃塞是否漏水,待确认不漏水后方可使用
D.中和滴定实验中,如用于盛放待测溶液的锥形瓶洗净后未干燥,会影响测定结果
184.(2013•汕头一模)下列有关说法正确的是( )
A.7.45g
NaClO中含有6.02×
1022个NaClO分子
B.1.00molNaClO中所有ClO-的电子总数为26×
1023
2
mol/L明矾经水解可得到氢氧化铝胶体粒子数目为2×
D.将2.00mol明矾完全溶于1.00
L水中,得到溶液的物质的量浓度为2
mol/L
185.(2013•汕头一模)下列实验方法正确的是( )
A.用无水乙醇提取碘水中的碘单质
B.加入稀HNO3和BaCl2溶液产生白色沉淀的溶液中一定含SO42-
C.可用FeCl3溶液一次性鉴别CCl4、苯酚溶液、NaI溶液和NaCl溶液
D.玻璃棒在配制0.1mol/L
NaCl溶液与粗盐提纯的实验中所起的作用相同
显示解析试题篮
186.(2013•日照一模)用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.常温常压下,46gNO2含有3NA个原子
B.7.8gNa2O2中含有的阴离子数目为0.2NA
C.室温时,1LpH=2的NH4Cl溶液中水电离出H+的数目为10-12NA
D.过氧化氢分解制得标准状况下1.12LO2,转移的电子数目为0.2NA
187.(2013•日照二模)用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A.2.24L
CH4气体中含有的电子数为NA
B.25℃时,1.0L
pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA
C.0.1NA个氯气份了溶于水形成1L溶液,所得溶液中c(C1-)=0.1mol•L-1
D.1molCH3COONa和少量CH3COOH溶于水形成的中性溶液中,CH3COO-数目为NA
188.(2013•青岛二模)下列说法不正确的是(设NA表示阿伏加德罗常数的值)( )
A.可用盐析法分离NaCl溶液和淀粉胶体
B.天然油脂的分子中含有酯基,属于酯类
C.T℃时,1L
pH=6的纯水中,含有的OH-数目为l×
10-6NA
D.12.0
gNaHSO4固体中含有的阳离子数目为0.1
189.(2013•青岛二模)下列有关实验基本操作的说法错误的是( )
A.存放新制氯水时,使用带玻璃塞的棕色玻璃瓶
B.配制一定物质的量浓度的溶液时,若开始容量瓶中有少量蒸馏水,对浓度无影响
C.酸碱中和滴定实验中用到的玻璃仪器仅有酸式滴定管、碱式滴定管和烧杯
D.进行蒸发操作时,不能使混合物中的水分完全蒸干
190.(2013•普陀区二模)室温时在实验室里将1.12L
H2S(g)通入1L某浓度的烧碱溶液中,恰好完全反应,测得溶液的pH=10(体积变化忽略不计),正确的推断是(NA代表阿伏加德罗常数)( )
A.硫化氢的分子数目约为0.05NA个
B.原烧碱溶液中约含溶质微粒0.1NA个
C.反应后溶液中约含OH-
1×
10-4NA个
D.反应后溶液中约含S2-
0.05NA个
191.(2013•普陀区二模)实验成功离不开正确的操作及数据记录.实验操作、记录正确的是( )
A.滴定管装液前只需水洗、润洗
B.在通风橱中取用溴
C.用pH试纸测得某氯水的pH为2
D.用100
mL量筒取70.5
mL蒸馏水
192.(2013•普陀区二模)用如图装置不能完成气体制取任务的是( )
A.过氧化钠和水反应制取氧气
B.生石灰和浓氨水反应制取氨气
C.二氧化锰和浓盐酸反应制取氯气
D.碳化钙和饱和食盐水反应制取乙炔
193.(2013•浦东新区一模)在反应3Cl2+8NH3→6NH4Cl+N2中,设阿伏加德罗常数为NA.则下列说法正确的是( )
A.若有0.3
Cl2参加反应,转移的电子数为0.6NA
B.若生成2.24
L氮气,转移的电子数为0.6NA
C.若有1.2NA个电子发生转移,则被氧化的氨气的质量是27.2
g
D.若生成1
mol的氯化铵转移电子数是n个,则NA=
n
194.(2013•浦东新区一模)用下列实验分离装置进行相应实验,能达到实验目的是( )
A.用图Ⅰ所示装置除去CO2中含有的少量HCl
B.用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图Ⅲ所示装置分离NaCl和Na2SO4的混合溶液
D.用图Ⅳ所示装置分离CCl4萃取碘水后已分层的有机层和水层
195.(2013•浦东新区三模)将a
g二氧化锰粉末加入b
mol/L的浓盐酸c
L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.可以收集到氯气
22.4b
2NA
L
B.反应后溶液中的Cl-数目为:
2aNA
87
C.NA可表示为:
87d
2a
D.反应后溶液中的H+数目为:
bc-2d
196.(2013•浦东新区三模)在中学化学实验室经常用到下列实验装置,其中不可用于物质分离的装置是( )
197.(2013•浦东新区三模)下述有关实验操作正确的是( )
A.溴苯中混有溴:
加入碘化钾溶液后分液
B.除去SO2中的少量CO2:
通过盛有饱和Na2CO3溶液的洗气瓶
C.用玻璃棒在过滤器上搅拌以加速AgCl沉淀的洗涤
D.中和滴定实验中,锥形瓶用蒸馏水洗净后未干燥,不影响测定结果
198.(2013•浦东新区二模)将a
g铝粉加入过量NaOH溶液中充分反应后,铝粉完全溶解,并收集到标准状况下b
L氢气,所得溶液中共有c个溶质离子,反应中转移电子d个.则阿伏加德罗常数(NA)可表示为( )
A.
27c
B.
16.8c
b
C.
9d
a
D.
22.4d
199.(2013•浦东新区二模)有机物的除杂方法中正确的是(括号中的是杂质)( )
A.乙酸(乙醛):
加入新制的氢氧化铜,加热
B.苯(苯酚):
加入溴水,过滤
C.溴乙烷(溴单质):
加入热氢氧化钠溶液洗涤,分液
D.乙酸乙酯(乙酸):
加入饱和碳酸钠溶液洗涤,分液
200.(2013•浦东新区二模)如图是制取和收集某气体的实验装置,该装置可用于( )
A.用浓硫酸和氯化钠反应制取HCl
B.用浓氨水和生石灰反应制取NH3
C.用双氧水与二氧化锰反应制取O2
D.用饱和食盐水和电石反应制取C2H2