高三化学下学期第三次质量检测试题高新部Word文件下载.docx
《高三化学下学期第三次质量检测试题高新部Word文件下载.docx》由会员分享,可在线阅读,更多相关《高三化学下学期第三次质量检测试题高新部Word文件下载.docx(21页珍藏版)》请在冰豆网上搜索。
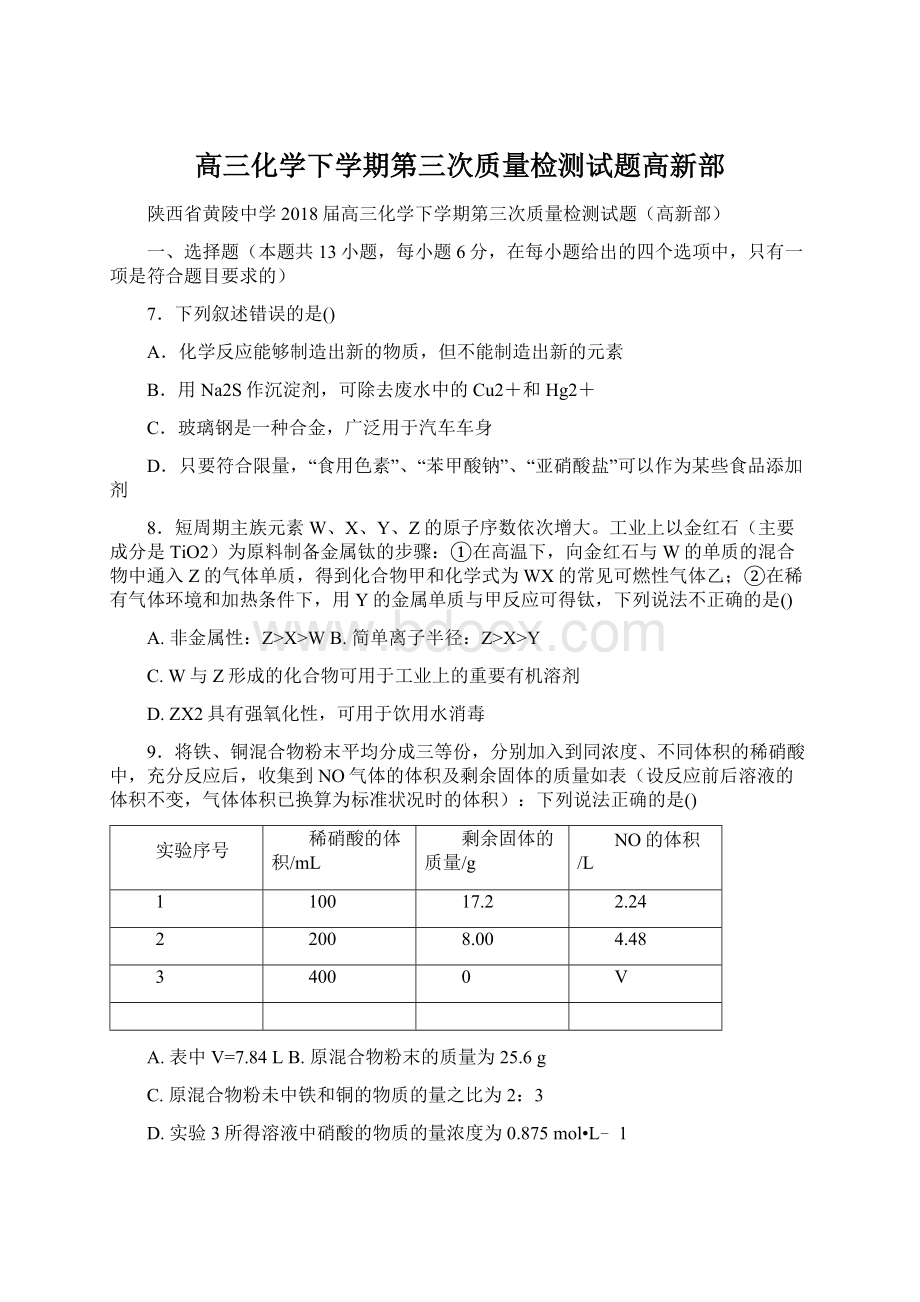
D.实验3所得溶液中硝酸的物质的量浓度为0.875mol•L﹣1
10.我国研究锂硫电池获得突破,电池的总反应是16Li+S8
8Li2S,充放电曲线如图所示,下列说法不正确的是()
A.充电时,电能转化为化学能
B.放电时,锂离子向正极移动
C.放电时,1molLi2S6转化为Li2S4得到2mole-
D.充电时,阳极总电极反应式是8S2--16e-=S8
11.a、b、c、d为原子序数依次增大的四种短周期主族元素。
a的最外层电子数是内层电子数的3倍,b的M层上有1个电子,a与c同主族。
下列说法不正确的是
A.原子半径:
b>
c>
dB.简单阴离子还原性:
d>
c
C.气态氢化物稳定性:
a>
cD.a、b可形成既含离子键又含共价键的离子化合物
12.液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点,一种以肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH作为电解质,
下列关于该燃料电池的叙述不正确的是
A.电流从右侧电极经过负载后流向左侧电极
B.负极发生的电极反应式为N2H4+4OH﹣﹣4e﹣=N2+4H2O
C.该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
D.该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
13.常温下,用0.2000mol/L的MOH溶液滴定10mL同浓度的一元弱酸HA,滴定过程溶液pH随MOH溶液V的变化曲线如图所示(忽略中和热效应),下列说法不正确的是
A.HA溶液加水稀释后,溶液中
的值减小
B.当V1=10时,MOH一定是弱碱
C.当V1=10时,溶液中水的电离程度最大
D.当V1>10时,溶液中离子浓度关系一定是c(M+)>c(A-)>c(OH-)>c(H+)
26.(14分)前两年华北地区频繁出现的雾霾天气引起了人们的高度重视,化学反应原理可用于治理环境污染,请回答以下问题。
(1)一定条件下,可用CO处理燃煤烟气生成液态硫,实现硫的回收。
①已知:
2CO(g)+O2(g)=2CO2(g)ΔH=−566kJ·
mol‾1
S(l)+O2(g)=SO2(g)ΔH=−296kJ·
则用CO处理燃煤烟气的热化学方程式是。
②在一定温度下,向2L密闭容器中充入2molCO、1molSO2发生上述反应,达到化学平衡时SO2的转化率为90%,则该温度下该反应的平衡常数K=。
(2)SNCR─SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:
已知该方法中主要反应的热化学方程式:
4NH3(g)+4NO(g)+O2(g)
4N2(g)+6H2O(g)ΔH=−1646kJ·
mol‾1,在一定温度下的密闭恒压的容器中,能表示上述反应达到化学平衡状态的是(填字母)。
a.4υ逆(N2)=υ正(O2)
b.混合气体的密度保持不变
c.c(N2)∶c(H2O)∶c(NH3)=4∶6∶4
d.单位时间内断裂4molN─H键的同时断裂4molN≡N键
(3)如图所示,反应温度会直接影响SNCR技术的脱硝效率。
①SNCR技术脱硝的温度选择925℃的理由是。
②SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是;
但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是。
(4)一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示:
①中间室的Cl‾移向(填“左室”或“右室”),处理后的含硝酸根废水的pH(填“增大”或“减小”);
②若图中有机废水中的有机物用C6H12O6表示,请写出左室发生反应的电极反应式:
。
27.(15分)三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂,实验室制取POCl3并测定产品含量的实验过程如下:
I.制备POCl3采用氧气氧化液态的PCl3法。
实验装置(加热及夹持装置省略)及相关信息如下。
物质
熔点/℃
沸点/℃
相对分子质量
其他
PCl3
-112.0
76.0
137.5
均为无色液体,遇水均剧烈
水解为含氧酸和氯化氢,两者互溶
POCl3
2.0
106.0
153.5
(1)仪器a的名称为_______________________________;
(2)装置C中生成POCl3的化学方程式为________________________________;
(3)实验中需控制通入O2的速率,对此采取的操作是_____________________;
(4)装置B的作用除观察O2的流速之外,还有___________________________________;
(5)反应温度应控制在60~65℃,原因是__________________________________;
Ⅱ.测定POCl3产品含量的实验步骤:
①实验I结束后,待三颈烧瓶中液体冷却到室温,准确称取16.725gPOCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液;
②取10.00mL溶液于锥形瓶中,加入10.00mL3.5mol/LAgNO3标准溶液(Ag++Cl-=AgCl↓);
③加入少量硝基苯(硝基苯密度比水大,且难溶于水);
④以硫酸铁溶液为指示剂,用0.2mol/LKSCN溶液滴定过量的AgNO3溶液(Ag++SCN-=AgSCN↓),到达终点时共用去10.00mLKSCN溶液。
(6)达到终点时的现象是_________________________________________;
(7)测得产品中n(POCl3)=___________________________;
(8)已知Ksp(AgCl)>
Ksp(AgSCN),据此判断,若取消步骤③,滴定结果将_______。
(填“偏高”“偏低”或“不变”)
28.(14分)NH3作为一种重要化工原料,被大量应用于工业生产,与其性质有关的催化剂研究曾被列入国家863计划。
(1)催化剂常具有较强的选择性,即专一性。
已知:
反应Ⅰ:
4NH3(g)+5O2(g)4NO(g)+6H2O(g)ΔH=-905.0kJ·
mol-1
反应Ⅱ:
4NH3(g)+3O2(g)2N2(g)+6H2O(g)ΔH=-1266.6kJ·
写出NO分解生成N2与O2的热化学方程式______________________________________。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应Ⅰ,测得不同时间NH3和O2的浓度如下表:
时间(min)
5
10
15
20
25
c(NH3)/(mol·
L-1)
1.00
0.36
0.12
0.08
0.072
c(O2)/(mol·
L-1)
2.00
1.20
0.90
0.85
0.84
则下列有关叙述中正确的是________。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内
=1时,说明反应已达平衡
D.前10分钟内的平均速率v(NO)=0.088mol·
L-1·
min-1
(3)氨催化氧化时会发生上述两个竞争反应Ⅰ、Ⅱ。
为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,测得有关物质的量关系如下图:
①该催化剂在低温时选择反应____(填“Ⅰ”或“Ⅱ”)。
②520℃时,4NH3+3O2
2N2+6H2O的平衡常数K=__________(不要求得出计算结果,只需列出数字计算式)。
③C点比B点所产生的NO的物质的量少的主要原因________。
(4)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的Cu2+。
25℃时,K1(H2S)=1.3×
10-7,K2(H2S)=7.1×
10-15,Ksp(CuS)=8.5×
10-45。
在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。
则0.1mol·
L-1氢硫酸的pH≈______(取近似整数)。
29.(8分)
分析下面与酶有关的曲线,回答下列问题:
(1)酶的作用机理可以用甲图纵坐标中段来表示。
如果将酶催化改为无机催化剂催化该反应,则b在纵轴上将______(填“上移”或“下移”)。
(2)乙图中160min时,生成物的量不再增加的原因是___________________。
(3)联系所学内容,分析丙图曲线:
①对于曲线abc,若x轴表示pH,则曲线上b点的生物学意义是________________________。
②对于曲线abd,若x轴表示反应物浓度,则y轴可表示_____________。
曲线bd不再增加的原因是_____________。
30.(10分)
血液在血管内不断地循环流动,具有运输能力,还具有维持内环境稳态、参与体液调节、防御和保护等作用。
请回答下列问题:
(1)各种营养物质和激素都是通过血液运输的,请比较饭后4小时肝细胞周围的毛细血管动脉端和静脉端中血糖浓度的高低:
(2)正常人肌肉在剧烈运动时产生的乳酸进入血液,血浆要依靠等无机盐离子的调节,使血浆的PH维持在7.35~7.45。
(3)人进食后的一段时间,在胃酸的作用下,分泌促胰液素进入血液,随血液循环导致。
(4)研究表明,人体血液中含有的生长素来源于消化道,请给出合理的解释:
31.(9分)我国第三个国家级湿地公园的建设流程如下:
退田还湖、水道清淤→清理地基,铺设减渗层→回填富含有机物的土壤和砂石(土壤取自原湿地生态系统的河底)→栽培本土水生及湿生植物,如芦苇、蒲草等,并注水→引入鲤鱼、草鱼等水生生物。
据此回答下列问题:
(1)上述流程涉及的生态系统的组成成分有生产者、消费者、______________。
(2)该湿地生物群落的演替类型属于_____演替,物种丰富度的变化趋势是____。
可见,人类活动往往会使群落演替按照不同于自然演替的______和______进行。
(3)此湿地生态系统岸边到湖中央的不同区域分布着不同的动物,这体现出群落的______结构。
其中阅海园区有鸟类107种,鸣翠湖园区有鸟类97种,这体现出生物多样性中的______多样性。
(4)湿地在改善水质、蓄洪防旱、调节气候等方面具有重要作用,这体现了生物多样性的_______价值。
32.(12分)下图是两个家族两种不同单基因遗传病的系谱图,图1中3号和4号为双胞胎,图2中4号不含致病基因。
回答下列问题:
(1)在图1中若3号、4号为异卵双生,则二者基因型相同的概率为_____。
若3号、4号为同卵双生,则二者性状差异来自_____________。
(2)图2中该病的遗传方式为______________遗传,理由是_____________。
若8号与10号近亲婚配,生了一个男孩,则该男孩患病的概率为。
(3)若图2中8号到了婚育年龄,从优生的角度考虑,你对她有哪些建议?
__________________________________________。
(二)选考题:
共45分。
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
如果多做,则每学科按所做的第一题计分。
33.【物理——选修3-3】
(15分)
(1)(5分)下列说法不正确的是(填正确答案标号。
选对1个得2分,选对2个得4分,选对3个得5分;
每选错1个扣3分,最低得分为0分)
A.竖直玻璃管里的水银面不是平面,而是“上凸”的,这是表面张力所致
B.相对湿度是空气里水蒸气的压强与大气压强的比值
C.物理性质表现为各向同性的固体一定是非晶体
D.压缩气体需要用力,这是气体分子间有斥力的表现
E.气缸里一定质量的理想气体发生等压膨胀时,单位时间碰撞器壁单位面积的气体分子数一定减少
(2)(10分)如图,体积为V、内壁光滑的圆柱形导热气缸顶部有一质量和厚度均可忽略的活塞;
气缸内密封有温度为2.4T0、压强为1.2P0的理想气体。
P0和T0分别为大气的压强和温度。
气体内能U与温度T的关系为U=aT,a为正的常量;
容器内气体的所有变化过程都是缓慢的.求:
①气缸内气体与大气达到平衡时的体积V1;
②在活塞下降过程中,气缸内气体放出的热量Q.
34.【物理——选修3—4】
(1)(5分)一列简谐横波沿x轴传播。
t=0时的波形如图所示,质点A与质点B相距
lm,A点速度沿y轴正方向;
t=0.02s时,质点A第一次到达正向最大位移处。
由此可知()(填正确答案标号。
选对一个得2分,选对两个得4分,选对三个得5分,每选错一个扣3分,最低得分为0分)
A.此波沿x轴正方向传播
B.此波的传播速度为25m/s
C.从t=0时起,经过0.04s,质点A沿波传播方向迁移了1m
D.在t=0.04s时,质点B处在平衡位置,速度沿y轴正方向
E此列波不能和频率为50Hz的横波发生干涉现象
(2)(10分)高速公路上的标志牌都用“回归反射膜”制成,夜间行车时,它能把车灯射出的光逆向返回。
这种“回归反射膜”是用球体反射元件制成的。
如图所示,透明介质球的球心位于O点,半径为R,光线DC平行于直径AOB射到介质球的C点,DC与AB的距离H=
若DC光线经折射进入介质球,在介质球内经一次反射,再经折射后射出的光线与人射光线CD平行。
试作出光路图,并计算出介质球的折射率。
35.【选修3——物质的结构与性质】
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的价电子排布式为_________。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。
电负性:
C___Ti(填“>
”或“<
“,下同);
第一电离能:
N____O,原因是_________。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3)。
FeTiO3与80%的硫酸反应可生成TiOSO4。
SO42-的空间构型为________形,其中硫原子的杂化方式为_______,写出与SO42-互为等电子体的一种分子的化学式:
________。
(4)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图1,Ti位于立方体的体心。
该晶体中,Ca2+的配位数为______。
(5)Fe能形成多种氧化物,其中FeO晶胞结构如图2。
FeO晶胞边长为428pm则FeO晶体的密度为___________g/cm3(阿伏伽德罗常数的值用NA表示,1pm=10-12m,写出计算式即可)。
36.【选修5——有机化学基础】
从薄荷油中得到一种烃A(C10H16),与A相关反应如下:
(1)B所含官能团的名称为_____________。
(2)含两个-COOCH3基团的C的同分异构体共有___种(不考虑手性异构),其中核磁共振氢谱显示2个吸收峰的异构体结构简式为________。
(3)D→E的反应类型为_________。
(4)G为含六元环的化合物,写出其结构简式________。
(5)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂名称为____。
(6)写出E→F的化学反应方程式:
________________。
(7)参照上述合成路线,设计由苯为原料(无机试剂任选)合成己二酸的合成路线。
37.[生物——选修1:
生物技术实践](15分)
木聚糖酶可以将半纤维素(一种多糖)转化为单细胞蛋白和其他有用物质。
有些嗜热菌能产生耐热木聚糖酶,在食品工业上具有较高的潜在应用价值。
现欲从温泉中分离能分解半纤维素的嗜热菌,并从中筛选木聚糖酶高产菌株,获得耐热木聚糖酶。
(1)实验中,接种环使用前后都在酒精灯上灼烧,其目的是___________________________。
(2)取适量体积的样品涂布在富含__________且其为唯一碳源的固体培养基上,置于恒温培养箱中培养,菌落长出后,挑取单个菌落并进行一系列操作,然后在培养基上用_____________法接种培养,进行菌株的________________。
最后将得到的菌株接种到__________(填“固体”或“液体”)培养基中富集。
(3)将富集后的菌株接种于固体培养基上,待菌落长出后用0.1%的__________染色1h,再用1mol/L的NaCl溶液脱色。
菌落周围会出现__________,筛选___________________的菌落即为木聚糖酶高产菌株。
38.[生物——选修3:
现代生物科技专题](15分)
Ⅱ型糖尿病病因复杂,多数是胰岛素拮抗引起机体对胰岛素的敏感性降低,而胰岛素单克隆抗体可用于快速检测血清胰岛素的含量。
请回答下列有关胰岛素单克隆抗体制备的问题:
(1)首先需要将人胰岛素注射到健康成熟小鼠体内,其目的是获取__________________细胞;
再将该细胞与______________相融合,以制取杂交瘤细胞;
其中诱导融合的常用生物诱导因素是________________。
(2)细胞融合实验完成后,融合体系中除含有未融合的细胞和杂交瘤细胞外,可能还有______________________________________________等两两融合的细胞。
细胞融合过程体现了细胞膜具有___________的特性。
(3)为检验得到的杂交瘤细胞能否分泌胰岛素抗体,可用___________与从杂交瘤细胞培养液中提取的抗体杂交。
在体外条件下,当培养的小鼠杂交瘤细胞达到一定密度时,需进行___________培养以得到更多数量的细胞。
(4)细胞融合技术的优点是_________________________________。
生物
1—6DAACCC
(1)ab(2分)上移(1分)
(2)底物已被完全消耗掉(2分)
(3)①在最适pH下,酶的催化效率最高(1分)
②酶促反应速率(1分)酶浓度的限制(1分)
30.(10分,每空2分)
(1)血糖浓度动脉端小于静脉端
(2)HCO3-、HPO42-(答出前者就可得2分)
(3)小肠黏膜胰腺(胰液)分泌量增加
(4)人体的消化道中没有分解生长素的酶
31.(9分每空1分)
(1)分解者、非生物的物质和能量(2分)
(2)次生增大速度方向
(3)水平物种(4)间接
32.(12分每空2分)
(1)5/9环境因素
(2)伴X染色体隐性该病为隐性遗传病,4号不含致病基因而7号患病,因此致病基因不可能位于常染色体上而是位于X染色体上 1/4
(3)与不患病的男性结婚,生育女孩
37.
(1)杀灭所有微生物及其孢子、防止细菌等的污染
(2)半纤维素平板划线法或稀释涂布平板分离纯化液体
(3)刚果红溶液透明圈透明圈(直径)大
38.
(1)能分泌抗人胰岛素抗体的B小鼠骨髓瘤细胞灭活的病毒
(2)B细胞相互融合形成的细胞、骨髓瘤细胞相互融合形成的细胞流动性
(3)人胰岛素传代
(4)突破了有性杂交的局限,使远缘杂交成为可能
物理14.C15.C16.A17.A18.B19.AC20.BC
21.ABD
22.
(1).1.075
(2).D(3).AD
23.
(1)3.0V或3V
(2)G如图所示
(3)
24解析:
设小球A下滑到水平轨道上时的速度大小为v1,平台水平速度大小为v,
由动量守恒定律有0=mAv1-Mv
由能量守恒定律有mAgh=
mAv12+
Mv2
联立解得v1=2m/s,v=1m/s
小球A、B碰后运动方向相反,设小球A、B的速度大小分别为v1′和v2。
由于碰后小球A被弹回,且恰好追不上平台,则此时小球A的速度等于平台的速度,有v1′=1m/s
由动量守恒定律得mAv1=-mAv1′+mBv2
由能量守恒定律有
mAv12=
mAv1′2+
mBv22
联立解得mB=3kg。
答案:
3kg
25解析:
(1)由题意可知,粒子做匀速圆周运动的半径为r1,有:
r1=
洛伦兹力提供向心力,有:
qv0B=m
解得:
v0=
(2)洛伦兹力提供向心力,又有:
qvB=m
r2=
粒子做匀速圆周运动的周期为T,有:
T=
则相遇时间为:
t=
=
T
在这段时间内粒子转动的圆心角为θ,有:
θ=
×
360°
=150°
如图所示,相遇点的纵坐标绝对值为:
r2sin30°
小球抛出点的纵坐标为:
y=
g
2-
(3)相遇时间t′=
T,
由对称性可知相遇点在第二个周期运动的最低点
设粒子运动到最低点时,离x轴的距离为ym,水平速度为vx
由动能定理,有:
qEym=
mvx2
联立解得:
ym=
故小球抛出点的纵坐标为:
(1)
(2)
(3)
33.【物理——选修3-3】
(15分)
(1)BCD(5分)
(2)
【解答】解:
(1)在气体由压强P=1.2P0到P0时,V不变,温度由2.4T0变为T1,
由查理定律得
……………………………1分
得:
T1=2T0……………………………1分
在气体温度由T1变为T0的过程中,体积由V减小到V1,气