动物生物化学习题集二文档格式.docx
《动物生物化学习题集二文档格式.docx》由会员分享,可在线阅读,更多相关《动物生物化学习题集二文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
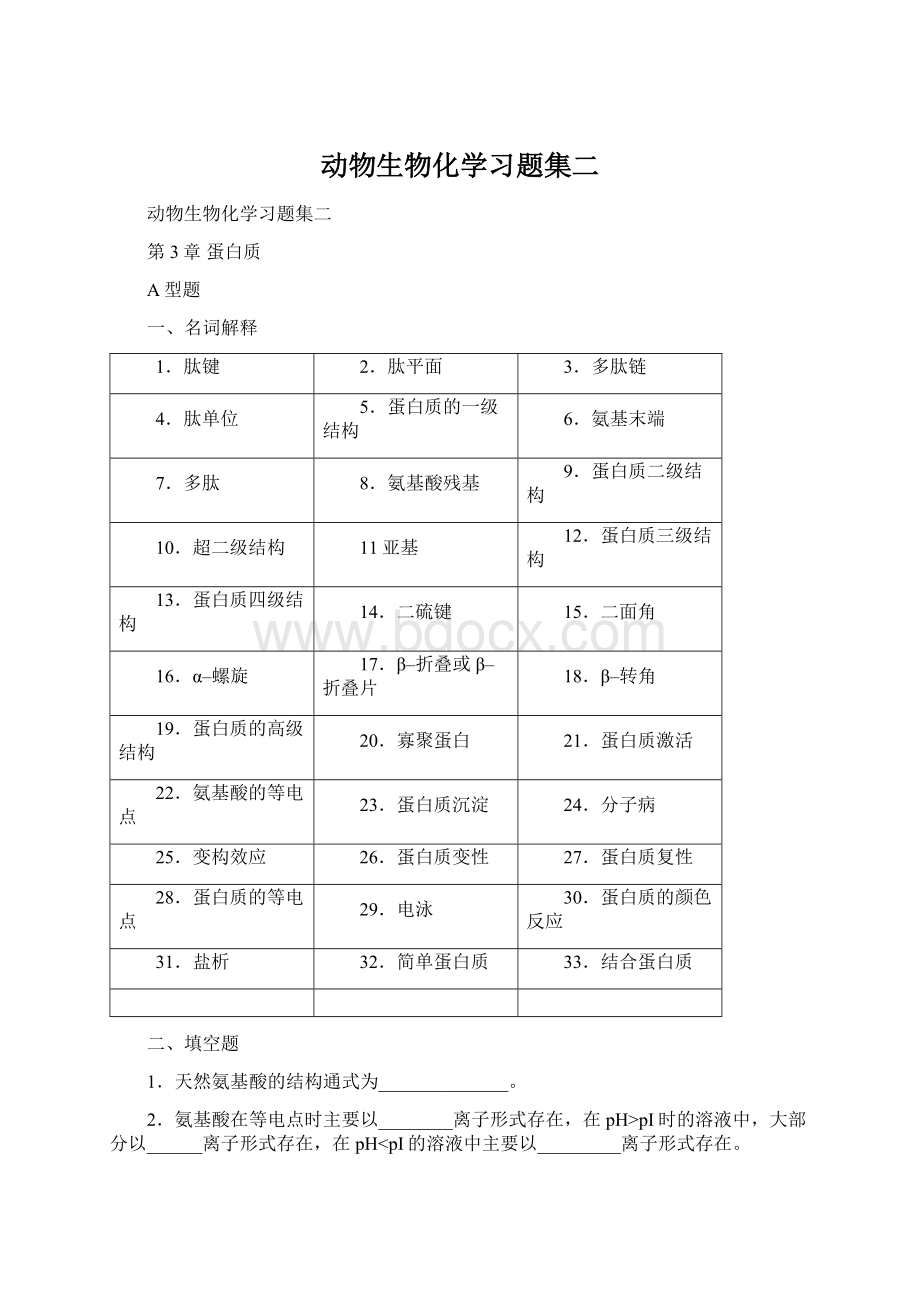
6.在一定的实验条件下,___________是氨基酸的特征常数。
7.在常见的20种氨基酸中,结构最简单的氨基酸是________。
8.蛋白质中氮元素的含量比较恒定,平均值为_______。
9.蛋白质中不完整的氨基酸被称为________。
10.维系蛋白质二级结构的最主要的力是________。
11.α–螺旋中相邻螺圈之间形成链内氢键,氢键取向几乎与________平行。
氢键是由每个氨基酸的______与前面隔三个氨基酸的_________形成的,它允许所有的_______都参与氢键的形成。
12.参与维持蛋白质构象的作用力有_____、_____、________、_______、_______、和_______。
13.蛋白质之所以出现丰富的构象,是因为主肽链的________和_______键能进行转动。
14.蛋白质主链构象的结构单元包括________、_________、________、_______。
15.维系蛋白质四级结构的作用力是_______、_______、_______和_______,其中最主要的是_________。
16.变性蛋白质的主要的特征是________丧失。
17.蛋白质变性的实质是_________________。
18.血红蛋白与氧结合呈现_____效应,这是通过血红蛋白的__________作用来实现的。
19.在胰岛素分子中始终保持不变的氨基酸残基称为_______________。
20.没有活性的胰岛素前体称为________________。
21.血红蛋白分子是由两个______亚基和两个______亚基组成的四聚体。
在血红素中央的________是氧结合的部位,且每一个_________可以结合一个氧分子。
22.医学通常用75%的洒精来消毒手术部位,主要是应用_________的这一特性。
23.常用的测定蛋白质分子量的方法有________、________和_________三种。
24.蛋白质溶液是亲水胶体,它具有一般胶体的性质,如:
_________、________、_______和__________。
25.破坏蛋白质胶体溶液稳定因素的因素有___________、_________、_________、__________和_______________。
26.蛋白质沉淀作用的实质是______________。
27.蛋白质分子在直流电场中的迁移速率的大小与蛋白质分子本身的________、__________和________有关。
28.根据分子对称性的不同,可将蛋白质分为_________和___________两大类。
29.根据化学组成的不同可将蛋白质分为_________和_____________两大类。
30.结合蛋白的非蛋白质部分通常称为______________。
三、简答题
1.α–螺旋的特征是什么?
如何以通式表示α–螺旋?
2.蛋白质β–折叠二级结构的主要特点是什么?
3.参与维持蛋白质空间结构的化学键有哪些?
有何作用?
4.胰岛素原与胰岛素在一级结构上有什么差异?
胰岛素原是如何被激活的?
5.血红蛋白的氧结合曲线为什么是S形的?
有何生理意义?
6.为什么用电泳法能将不同蛋白质的混合物分离出来?
7.蛋白质为什么能在水溶液中稳定存在?
8.蛋白质分子为何具有紫外吸收特性?
四、论述题
1.用实例说明多肽一级结构与功能之间的关系?
2.什么是蛋白质变性?
有哪些因素可使之变性?
变性蛋白质有什么变化?
用哪些方法可以检测蛋白质是否变性?
3.蛋白质有哪些重要的理化性质?
其分离提纯的一般步骤是什么?
如何测定蛋白质分子量?
4.用实例说明蛋白质的一级结构。
B型题
1.如何测定蛋白质的一级结构?
2.如何鉴定蛋白质发生了变性?
第4章核酸化学
A型题
1.自我复制
2.转录
3.翻译
4.磷酸二酯键
5.核酸的一级结构
6.DNA二级结构
7.碱基互补规律
8.稀有碱基
9.遗传密码
10.“发卡”结构
11.沉降系数
12.复性
1.核苷酸除去磷酸基后称为。
2.RNA常见的碱基是、、和。
3.体内的嘌呤碱主要有和;
嘧啶碱主要有、和。
4.DNA双螺旋结构模型是于年提出来的。
5.DNA双螺旋的两股链的顺序是、的关系。
6.双螺旋DNA的熔解温度Tm与、和有关。
7.DNA的稀盐溶液加热至某个特定浓度,可引起理化性质发生很大的变化,如
和,这种现象叫做,其原因是由于。
8.DNA双螺旋直径为nm,双螺旋每隔nm转一圈约相当于个碱基对,糖和磷酸位于双螺旋的侧,碱基位于侧。
9.DNA二级结构的重要特点是形成结构,此结构的外部结构是由
和形成,而结构的内部是由通过相连而成的。
10.DNA的双螺旋中,A、T之间有个键,而G、C之间有个键。
11.RNA分子指导蛋白质合成,RNA分子用作蛋白质合成中活化氨基酸的载体。
12.tRNA的二级结构是型,三级结构是型。
13.因为核酸分子中含有嘌呤碱和,二者两种物质又均具有,故使核酸对的波长有紫外吸收作用。
14.tRNA的三叶草结构中,氨基酸臂的功能是,反密码子环的功能是。
15.tRNA的氨基酸臂中的最后3个碱基是,反密码子环最中间有3个单核苷酸组成,tRNA不同也不同。
1.简述DNA碱基当量定律。
2.什么是DNA热变性?
DNA热变性后有何特点?
Tm值表示什么?
3.简述DNA碱基组成特点。
4.简述核酸的概念、分类、特点及功能。
5.DNA与RNA的一级结构有何异同?
6.简述核酸的逐步水解过程。
1.说明DNA双螺旋的结构特点。
2.简述RNA的种类及作用。
3.DNA都有那些物理化学性质?
1.试述tRNA二级结构的结构特征。
2.为什么大多数核酸酶受金属螯合剂EDTA的抑制?
3.真核细胞染色体DNA很长,它是如何存在于细胞核内的?
第7章酶与维生素
一、名词解释
1.酶
2.全酶
3.辅酶
4.酶的专一性
5.酶活性中性
6.必需基团
7.酶原
8.酶原激活
9.诱导契合学说
10.底物
11.变构酶
12.活化能
13.酶活力
14.激活剂
15.变构效应
16.混合级反应
17.Km
18.酶的最适pH
19.酶的最适温度
20.竞争性抑制作用
21.调节酶
22.变构效应
23.正协同效应
24.效应物(子)
25.变构激活剂
26.共价修饰调节
27.同工酶
28.酶工程
29.固定化酶
30.多酶复合体
1.酶的化学本质是或。
2.酶分子中能直接与底物分子结合,并催化底物化学反应的部位,称为酶的
或。
3.酶活性部位是由和组成的。
前者决定专一性,后者决定专一性。
4.酶对的严格选择性称为酶的专一性,一般可分为、
和。
5.L–精氨酸酶只作用于L–精氨酸,而对D–精氨酸无作用,因为此酶具有
专一性。
6.酶根据其分子特点可分为、、三类。
7.按照化学组成,酶可分为和。
8.单纯酶的活性仅仅决定于它的,结合酶的活性除了需要以外,还需要,前者称为,后者称为。
9.提高酶催化效率的五大主要因素是、、
、、和。
10.共价催化又可分为和。
11.大多数酶的催化机理可分为和两类。
12.、和都是酶结合底物的重要化学键。
13.测酶活力的主要原则是在特定、和条件下测定其体系内产物的生成量或底物的消耗量。
14.测定酶活力,实际上就是测定,酶促反应速度越快,酶活力就越。
15.酶活力单位是衡量酶的单位。
为了统一酶活力的计算标准,1961年,国际生物化学协会酶学委员会对酶活力单位作了下列规定:
在指定的反应条件下,
内,将的底物转化为产物所需要的酶量,定为一个国际单位。
上述指定的反应条件是:
,,。
16.酶反应速度有二种表示方式:
17.为了排除干扰,酶活力应该用来表示。
就是指:
底物开始反应之后,很短一段时间内的反应速度。
反应时间一般采用。
18.酶制剂的酶含量及纯度常用表示。
比活力较大的酶制剂,其酶含量及纯度较。
19.抑制剂并不改变一个酶反应的Vmax。
20.预使酶促反应速度达到最大反应的90%,此时底物浓度应是此酶Km值的
倍。
21.如果一个酶对A、B、C三种底物的米氏常数分别为Kma、Kmb、Kmc,且Kma>
Kmb>
Kmc,则此酶的最适底物是,与酶亲和力最小的底物是。
22.影响酶反应速度的因素有:
、、、
、、等。
23.动物体内各种酶的最适温度一般在,大多数酶的最适pH一般为。
24.同工酶是一类相同、不同的一类酶。
25.根据调节物分子的不同,别构效应分为和。
根据调节酶反应速度对[S]敏感性不同分为和。
26.酶活性的调控可以通过两种方式来完成,第一种是,已存在于细胞的酶,可以通过酶的改变或等方式来改变其活性,第二种是,通过改变酶的
的速度,来改变,从而改变酶活性。
27.对代谢途径的反应速度起调节作用的酶称为,它包括、以及等。
28.酶工程分为和两大类,前者又称为,是酶学与化学工程技术相结合的产物,后者又称为,是酶学与DNA重组技术为主的现代分子生物学技术相结合的产物。
29.固定化酶就是指:
。
30.常用的制备固定化酶的方法有、、和等方法。
31.国际酶学委员会根据酶催化的反应类型,将酶分成、、、、、六大类。
1.试述使用酶作催化剂的优缺点?
2.在全酶分子中金属离子有何作用?
3.试述辅基与辅酶有何异同?
4.举出三种维生素,说明其辅酶形式和在酶促反应中的主要作用?
5.举例说明酶原激活的机理?
6.解释磺胺类药物的抑菌机理、有机磷农药的杀虫机理?
7.试说明可逆性抑制与不可逆性抑制的不同之处?
8.简单说明竞争性抑制与非竞争性抑制的不同特征?
9.如何进行酶活力的测定?
10.说明酶活性部位的组成,位置和基团构成。
11.什么是米氏常数?
其意义是什么?
怎样能够求出米氏常数?
12.什么是单纯酶和结合酶?
它们的区别和联系是什么?
1.什么是变构酶,变构调节有何生理意义?
2.说明影响酶促反应速度的主要因素?
一、简答题
1.简述化学酶工程与生物酶工程所研究的主要内容?
2.酶的变构调节和共价修饰调节有何异同?
第8章糖代谢
1.血糖
2.糖酵解
3.三羧酸循环
4.丙酮酸脱氢酶复合体
5.α–酮戊二酸脱氢酶复合体
6.磷酸戊糖途径
7.葡萄糖异生作用
8.糖原
9.糖原合成作用
10.酶促酶级联式机制
11.糖原的分解
12.有氧氧化
1.糖在动物体内主要作为和。
2.单胃杂食动物体内糖的主要来源是由,而反刍动物,糖源是,它被瘤胃中的微生物发酵,分解为、和等低级脂肪酸后被吸收。
3.由生成的反应是糖酵解途径中唯一的脱氢反应,反应脱下的氢被递氢体接受。
4.糖酵解途径的关键酶有、和。
5.糖酵解途径的反应全部在细胞的进行。
6.1摩尔葡萄糖经糖酵解途径可产生摩尔ATP。
7.糖酵解途径中1,6–二磷酸果糖在醛缩酶催化下裂解为2分子三碳单位即和。
8.丙酮酸脱氢酶复合体包括、及三种酶和种辅助因子。
9.1mol乙酰辅酶A和1mol草酰乙酸经三羧酸循环后,最终可产生molATP和mol草酰乙酸。
10.Krebs循环的关键酶包括、和。
11.一次TCA循环可有次脱氢反应、次底物磷酸化和
次脱羧反应。
12.磷酸戊糖途径的重要产物是和。
13.磷酸戊糖途径从开始,反应可分为和两个分支。
14.磷酸戊糖途径通过将和核苷酸代谢联系起来。
15.磷酸戊糖途径的产物之一NADPH主要在还原性的生物合成中作供体。
16.非氧化性分支即5–磷酸核糖经过一系列的分子重排生成6–磷酸果糖和。
17.磷酸戊糖途径的产物之一5–磷酸核糖主要用于合成和。
18.葡萄糖异生作用主要在中进行。
29.、和是体内糖异生的主要非糖前体物质。
20.葡萄糖异生途径的“能障”实际上是糖酵解中三个酶催化的反应;
这三种酶是、、和。
21.丙酮酸羧化酶位于内,它的辅基是。
22.异生途径绕过“能障”的反应由、、和催化。
23.糖原中的葡萄糖残基以相连形成直链,以相连形成分枝。
24.糖原合成的关键酶是;
糖原分解的关键酶是。
25.葡萄糖参与合成糖原的活性形式是。
26.调节糖原代谢的激素主要有、和。
27.浓度为的Ca2+恰可引起肌肉收缩。
28.肌肉不能直接补充血糖的主要原因是缺乏。
29.糖原分解需要、和这三种酶共同发挥作用。
三、简答题
1.试述血糖的来源和去路。
2.简述糖酵解途径的生理意义。
3.在糖酵解过程中,NAD+的再生是怎样实现的?
4.简述柠檬酸循环的生理意义。
5.简述磷酸戊糖途径的生理意义。
6.简述糖异生的生理意义。
7.简述糖原合成的过程(结合反应的关键酶)。
8.简述糖原分解的过程(结合反应的关键酶)。
9.以磷酸化酶的调节为例,说明酶的级联机制。
1.写出糖的酵解途径(文字标出)及相关酶类。
2.写出柠檬酸循环的反应途径(文字标出)及相关酶类。
3.计算一摩尔葡萄糖经糖的有氧氧化可生成多少摩尔ATP?
4.试述机体是怎样进行糖原代谢的整体调节的?
5.简述体内的各种糖代谢途径是怎样联系起来的,连接产物如何起的作用。
1.试述机体是怎样利用磷酸戊糖途径对NADPH、5–磷酸核糖和ATP的需要进行调控的。
2.为什么说丙酮酸羧化酶是联系糖异生和柠檬酸循环的一个重要酶?
3.为什么肝脏中糖原浓度最高?
4.肌糖原和肝糖原分解产物的代谢去向有何不同?
第8章脂类代谢
1.脂类
2.类脂
3.必需脂肪酸
4.脂肪动员
5.脂肪酸的β–氧化
6.酮体
7.血浆脂蛋白
8.酮症
9.酸中毒
1.人体不能合成而需要由食物提供的必需脂肪酸有、和。
2.脂肪酸的β–氧化在线粒体内的反应包括、、和
四个步骤。
脂酰CoA经一次β–氧化可生成一分子和。
3.脂肪酸的β–氧化的限速酶是。
4.一分子16碳长链脂酰CoA可经次β–氧化生成个乙酰CoA。
5.酮体合成的酶系存在于,氧化利用的酶系存在于。
6.酮体生成过程中的限速酶为。
7.限制脂肪酸生物合成速度的反应是由催化的。
8.高等动物合成甘油三酯所需要的前体是和。
9.脂肪酸合成过程中,超过16碳的脂肪酸主要通过和亚细胞器的酶系参与延长碳链。
10.乙酰CoA羧化酶的辅酶是,催化反应的产物是。
11.血浆中脂肪酸的唯一来源是。
12.血浆中的游离脂肪酸浓度不仅取决于的动员程度,也取决于肝脏摄入
的速度。
13.动脉粥样硬化可能是由于过多的引起的。
14.胆固醇生物合成的原料是,合成胆固醇的限速酶是。
15.脂肪消化产物在十二指肠下段或空肠上段被吸收后,与磷脂、载脂蛋白等组成
经淋巴进入血液循环。
16.游离脂肪酸不溶于水,需与结合后由血液运至全身。
17.血浆脂蛋白根据其密度由小到大分为、、、
四类。
18.血浆的水平与心血管病的发生呈反相关。
19.受体基因缺陷是引起家族性高胆固醇血症的重要原因。
1.简述脂类的生理功能。
2.简述酮体的生理意义。
3.简述脂肪组织中脂肪的合成与分解的调节。
4.简述肌肉组织利用脂肪酸以节约糖的机制。
5.简述肝脏对于脂肪代谢的调节作用。
6.血浆脂蛋白有哪两种分类?
各种血浆脂蛋白的功能有什么特点?
7.胆固醇在动物体内有哪些生物转变?
8.试说明脂肪分解产生的甘油的代谢去向。
9.说明反刍动物丙酸代谢的意义。
1.简述脂肪酸β–氧化的具体过程。
2.试计算1摩尔18碳饱和脂肪酸通过β–氧化彻底氧化分解为H2O和CO2时可产生多少摩尔ATP。
3.写出酮体生成与利用的的反应过程,说明引起动物发生酮病的机制。
4.以14碳脂肪酸为例,写出它的合成过程。
5.用文字简要描述脑磷脂和卵磷脂的合成过程。
1.为什么摄入过量的糖容易长胖?
2.乙酰CoA可进入哪些代谢途径?
请列出。
3.动物机体如何调节胆固醇的合成?
4.脂类代谢紊乱有那些常见情况,其发生机理各是怎样?
第9章生物氧化
1.呼吸链
2.磷氧比值
3.底物水平磷酸化
4.氧化磷酸化
5.生物氧化
6.铁硫中心
1.ATP由和反应形成,这个过程称为,其需要食物分子分解释放的来推动。
在体内分为和两种。
2.代谢物在细胞内的氧化与在体外燃烧的主要区别是、、和。
3.真核细胞生物氧化是在进行的,原核细胞生物氧化是在进行的。
4.生物氧化是通过代谢物反应实现的,生物氧化产生的H2O是通过
形成的。
5.生物界普遍存在的典型的生物氧化体系是由、和三部分形成的。
6.典型的呼吸链包括和两种,这是根据接受代谢物脱下的氢的不同而区别的。
7.填写电子传递链的阻断抑制剂:
NAD→FMN→CoQ→Cytb→Cytc1→Cytc→Cytaa3→O2
()()()
8.氧化磷酸化生成ATP的偶联部位是,和。
9.每对电子从FADH2转移到必然释放出2个H+进入线粒体内。
10.NADH呼吸链中氧化磷酸化发生的部位是在;
;
。
11.用特殊的抑制剂可将呼吸链分成许多单个反应,这是一种研究氧化磷酸化中间步骤的有效方法,常用的抑制剂及作用如下:
鱼藤酮抑制电子由向的传递。
抗霉素A抑制电子由向的传递。
氰化物、CO抑制电子由向的传递。
12.黄嘌呤氧化酶以为辅基,并含有和,属于金属黄素蛋白酶。
13.单加氧酶也称为或,分布在细胞的上。
1.在体内ATP有哪些生理作用?
2.生物体内有哪些重要的高能化合物?
3.何谓呼吸链?
4.常见的呼吸链电子传递抑制剂有哪些?
它们的作用机制是什么?
5.何谓氧化磷酸化作用?
NADH呼吸链中有几个氧化磷酸化偶联部位?
6.分别写出NADH和FADH2电子传递链的过程及其关键酶。
1.何谓解偶联作用?
如何证明2,4–二硝基苯酚是典型的解偶联剂?
2.为什么CO和氰化物有剧毒?
第11章蛋白质的分解代谢
1.氮平衡
2.蛋白质的最低需要量
3.蛋白质的生理价值
4.必需氨基酸
5.非必需氨基酸
6.蛋白质的互补作用
7.氨基酸代谢池
8.转氨基作用
9.联合脱氨基作用
10.嘌呤核苷酸循环
11.内源性氨基酸
12.外源性氨基酸
13.血氨
14.生糖氨基酸
15.生糖兼生酮氨基酸
16.生酮氨基酸
17.一碳单位
18.甲硫氨酸循环
1.正常成年动物的蛋白质代谢情况是属于平衡,即=。
2.蛋白质的生理价值主要取决于的数量、种类及比例。
3.营养充足的婴儿、孕妇、恢复期病人,常保持。
4.蛋白质的生理价值=。
5.由糖代谢的中间产物合成的氨基酸属于。
6.直接生成游离氨的脱氨方式有和。
7.转氨酶的辅酶称,它与底物脱下的氨基结合可转为。
8.L–谷氨酸脱氢酶的辅酶是________或________,和是此酶的别构抑制剂。
9.嘌呤核苷酸中最终将NH3释放出的化合物称,催化此反应的酶是。
10.丙氨酸经转氨基作用可产生游离氨和,后者可进入途径进一步代谢。
11.NH3有剧毒,不能在体内积累,它主要以形式进行转运。
12.是清除氨的主要器官,它可通过将NH3和CO2合成无毒的,而禽类则合成的是。
13.合成一分子尿素需消耗分子的高能键。
14.转运氨并降低其毒性的氨基酸是和。
15.生酮氨基酸经代谢后可产生,它是合成酮体的原料。
16.合成黑色素的主要原料是或。
17.儿茶酚胺包括、、和三种物质。
18.dTMP只能由甲基化产生。
19.催化氧化型硫氧还原蛋白还原的酶是,此酶的辅酶是。
20.催化dUMP转变为dTMP的酶是,此酶的辅酶是,它转运给dUMP生成dTMP。
1.简述蛋白质在动物体内有何生物学功能。
2.试述动物体内氨的来源、转运和去路。
3.试说明氨基酸脱氨基后生成的α–酮酸的代谢去向。
4.氨基酸的代谢去向有哪些?
5.简述天冬氨酸在尿素循环中的作用。
6.举出三种氨基酸脱羧基作用的产物,说明其生理功能?
7.说明谷胱甘肽的分子组成及有何生理机能?
1.写出鸟氨酸循环过程,说明尿素分子中C、N原子的来源?
2.试述一碳基团的来源和转变?
3.综述糖、脂类、氨基酸和核苷酸代谢的相互联系和相互影响?
B型