最新高一化学上学期第一次质量检测试题1Word文档下载推荐.docx
《最新高一化学上学期第一次质量检测试题1Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《最新高一化学上学期第一次质量检测试题1Word文档下载推荐.docx(9页珍藏版)》请在冰豆网上搜索。
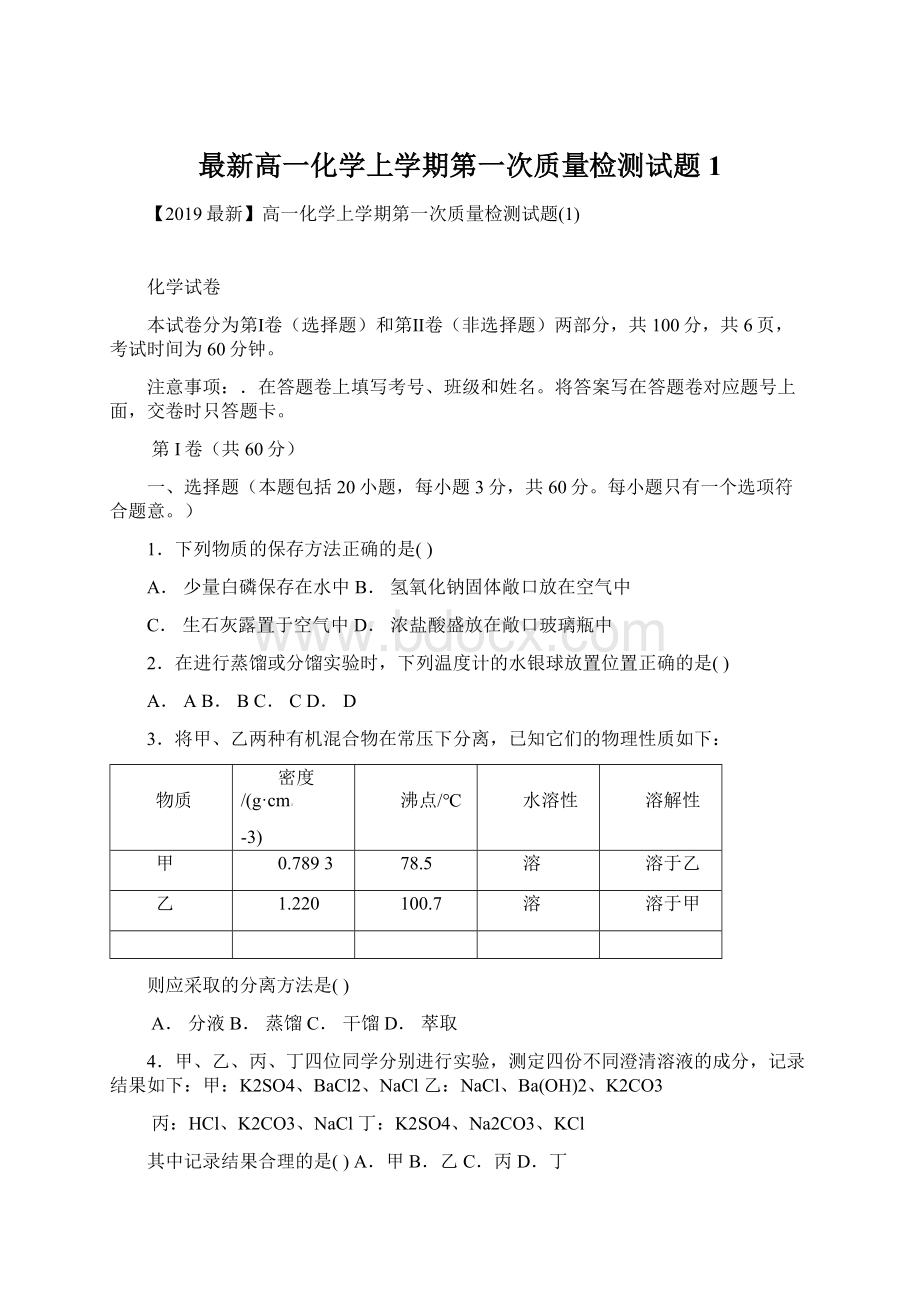
78.5
溶
溶于乙
乙
1.220
100.7
溶于甲
则应采取的分离方法是()
A.分液B.蒸馏C.干馏D.萃取
4.甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录结果如下:
甲:
K2SO4、BaCl2、NaCl乙:
NaCl、Ba(OH)2、K2CO3
丙:
HCl、K2CO3、NaCl丁:
K2SO4、Na2CO3、KCl
其中记录结果合理的是()A.甲B.乙C.丙D.丁
5.过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2溶液;
④滴入稀盐酸至无气泡产生;
⑤过滤。
正确的操作顺序是(
)
A.③②①⑤④B.①②③⑤④C.②③①④⑤D.③⑤②①④
6.在某无色透明酸性溶液中,能共存的离子组是()
A.NH4+、NO3-、Al3+、Cl-B.Na+、Fe2+、K+、NO3-
C.MnO4-、K+、SO42-、Na+D.K+、SO42-、HCO3-、Na+
7.下列化学实验操作或事故处理方法正确的是(
A.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸
B.给试管里的液体加热,液体的体积一般不超过试管容积的
C.酒精着火时可用水扑灭
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
8.下列物质中导电性最差的是()
A.熔融状态的KOHB.石墨棒
C.固态KClD.稀H2SO4
9.实验室进行NaCl溶液蒸发时,一般有以下操作过程:
①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干,其中正确的操作顺序是( )
A.①②③④B.①②③④⑤C.②③①④⑤D.②①③④⑤
10.下列制取蒸馏水的实验装置与操作的说法中,不正确的是()
A.温度计的水银球应插入蒸馏烧瓶中的自来水中
B.冷凝管中的水流方向是从下口进入,上口排出
C.实验中需要在蒸馏烧瓶中加入几粒碎瓷片,防止出现暴沸现象
D.加热蒸馏烧瓶必须垫石棉网
11.下列反应中,不属于离子反应的是()
A.H2和O2的反应B.铁与CuSO4溶液的反应
C.Ba(OH)2溶液和H2SO4溶液的反应D.Zn和稀H2SO4反应
12.如果你家里的食用花生油混有水份,你将采用下列何种方法分离()
A.过滤B.蒸馏C.分液D.萃取
13.铁、稀盐酸、澄清石灰水、氯化铜溶液是常见的物质,四种物质间的反应关系如图所示。
图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是()
A.OH-+HCl===H2O+Cl-
B.Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C.Fe+Cu2+===Cu+Fe2+
D.Fe+2H+===Fe3++H2↑
14.某同学欲配制含有大量下列各离子的溶液,其中能实现的是()
A.K+、H+、SO42-、OH-
B.Na+、Ca2+、CO32-、NO3-
C.Na+、H+、CL-、CO32-
D.Na+、Cu2+、CL-、SO42-
15.下列状态的物质,既能导电又属于电解质的是()
A.MgCl2晶体B.NaCl溶液
C.液态氯化氢D.熔融的KOH
16.三组混合液:
①植物油和水,②丙酮和水(二者互溶),③碘化钠和单质碘的混合水溶液。
分离它们的正确方法依次是()
A.分液 萃取 蒸馏B.萃取 蒸馏 分液
C.分液 蒸馏 萃取D.蒸馏 萃取 分液
17.下列叙述中不正确的是()
A.在熔融状态下和溶解于水时均不导电的化合物,叫做非电解质
B.电解质、非电解质都对化合物而言,单质不在此范畴
C.在水中的电解质一定都导电性很强
D.水是极弱的电解质
18.古代常用如图所示装置来炼丹、熬烧酒、制花露水等。
南宋张世南《游宦纪闻》记载了民间制取花露水的方法:
“锡为小甑,实花一重,香骨一重,常使花多于香。
窍甑之傍,以泄汗液,以器贮之。
”该装置利用的实验操作方法是()
A.蒸馏B.过滤
C.萃取D.升华
19.在用CCl4萃取碘水中的碘单质时,必须使用到的玻璃仪器是()
20.下表中所列出的物质,属于贴错了包装标签的是()
选项
A
B
C
D
物质的化学式
HNO3(浓)
CCl4
P4
KClO3
危险警告标识
第II卷(共40分)
三、填空题(本题包括4小题,共40分)
21.(6分)下列物质:
①Fe②CO2③NaCl溶液④Cu(OH)2⑤熔融的MgCl2⑥NH4Cl溶液
⑦盐酸⑧C2H5OH(酒精)(用序号作答).
其中属于电解质的有________,属于非电解质的有________,能导电的有________.
22.(8分)写出下列各组反应中的离子方程式。
A.盐酸分别与NaOH溶液、Cu(OH)2反应:
________________________________________________________________________
________________________________________________________________________;
B.硫酸分别与NaOH溶液、Ba(OH)2溶液反应:
C.硝酸分别与Na2CO3溶液、K2CO3溶液反应:
D.锌分别与稀盐酸、稀硫酸反应:
________________________________________________________________________。
23.(10分)除去下列物质中混有的少量杂质(杂质不要求回收),把适当的试剂、操作方法的序号写在相应的括号内。
a.加适量盐酸、过滤b.加适量水、过滤、蒸发c.加适量水、过滤d.加热(高温或灼烧)e.加适量盐酸、蒸发f.冷却热的饱和溶液、过滤
(1)碳酸钙中混有少量的碳酸钠________
(2)氯化钾粉末中混有碳酸钾________
(3)氧化钙中混有少量的碳酸钙________
(4)二氧化锰中混有少量的炭粉________
(5)硝酸钾中混有少量的食盐________
24.(16分)今有A、B、C、D、E、F六种装置,如图所示。
(胶塞、导管可自由选用)
(1)写出①~④的仪器名称:
①__________,②__________,③________,④________。
(2)实验室制取并收集氧气时应选择________和________相连接,制取并收集氢气时应选择________和________相连接。
(3)做木炭还原氧化铜并检验生成气体的实验,应选择________和________相连接,检验气体时观察到的实验现象是________。
(4)制取氢气并做还原氧化铜的实验,应选择________和________装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,其原因是_________________________________________________
参考答案
1.A
【解析】A、白磷易自燃,应隔绝空气,所以储存在水中,以防自燃,A正确;
B、固体氢氧化钠易潮解,故应密封保存,B错误;
C、生石灰能吸收水,应密封保存,C错误;
D、浓盐酸具有较强的挥发性,所以应密封保存在细口瓶中,D错误,答案选A。
点睛:
此题是药品储存的有关考查题,解题的关键是了解所储存物质的特性,属基础性知识考查题。
解答时还需要注意试剂瓶和瓶塞的选择。
2.C
【解析】蒸馏时温度计测量气体的温度,因此温度计的水银球通常放置在蒸馏烧瓶的支管口处。
答案选C。
3.B
【解析】由表中信息可知甲、乙互溶且均易溶于水,但甲、乙的沸点不同,故应采取蒸馏的方法进行分离。
答案选B。
4.D
【解析】甲会形成BaSO4沉淀而不能共存;
乙会形成BaCO3沉淀而不能共存;
丙会产生CO2气体而不能共存。
5.A
【解析】
Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后加入盐酸酸化。
但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必需放在氯化钡的后面,而氢氧化钠可以随意调整,所以正确的操作顺序是③②①⑤④,答案选A。
6.A
7.A
A、不慎将浓碱溶液沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸,A正确;
B、给试管里的液体加热,液体的体积一般不超过试管容积的1/3,B错误;
C、酒精着火时不能用水扑灭,应该用沙子扑灭,C错误;
D、量筒不能用来稀释溶液或溶解固体,稀释浓硫酸应该在烧杯中进行,D错误,答案选A。
8.C
【解析】石墨棒能导电;
熔融电解质、电解质溶液因有能够自由移动的离子,能导电;
固体KCl含有钾离子和氯离子但不能自由移动,不导电。
9.B
【解析】试题分析:
实验室进行NaCl溶液蒸发时,正确的操作过程为:
①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干,选B。
考点:
考查化学实验基本操作
10.A
蒸馏时温度计的水银球应位于支管口附近,A项错误。
11.A
【解析】氢气和氧气反应过程中没有离子参加或生成,故不属于离子反应,A项符合题意。
12.C
【解析】花生油难溶于水,花生油与水混合分层,所以用分液法分离花生油和水的混合物,故C正确。
13.C
【解析】A中盐酸是强酸,在溶液中应拆成离子形式,正确的离子方程式为H++OH-===H2O;
B中澄清石灰水中Ca(OH)2应拆成离子形式,正确的离子方程式为2OH-+Cu2+===Cu(OH)2↓;
C中铁能置换出氯化铜中的铜,原子守恒,电荷也守恒,正确;
D中铁与稀盐酸反应生成
Fe2+,正确的离子方程式为Fe+2H+===Fe2++H2↑。
故正确答案为C。
14.D
试题分析:
A中氢离子和OH-不能大量共存;
B中生成碳酸钙白色沉淀;
C中生成CO2和水,所以正确的答案选D。
考查离子共存的正误判断
点评:
本题是基础性知识的考查,也是高考中的常见题型,难度不大。
本题有利于培养学生灵活运用知识的能力,有利于调动学生的学习积极性。
15.D
【解析】MgCl2晶体是电解质但无自由移动的离子,不导电;
NaCl溶液是混合物,非电解质溶液;
HCl液态时不导电。
16.C
【解析】①植物油和水不互溶,已分层可直接分液;
②丙酮和水互溶,但沸点相差较大,可用蒸馏;
③碘化钠易溶于水,单质碘更易溶于有机溶剂,所以可用萃取的方法,故选项C正确。
17.C
【解析】在水中的电解质也有强弱之分,部分难溶于水的强电解质也不导电。
18.A
题干中描述的制取花露水的方法实际上和现代蒸馏的方法是一样的,“窍甑之傍,以泄汗液,以器贮之”。
说的就是冷凝液体的过程,故本题选A。
19.C
【解析】在用CCl4萃取碘水中的碘单质时,必须使用到的玻璃仪器是分液漏斗和烧杯,答案选C。
20.B
【解析】四氯化碳不具有可燃性,故选B。
21.④⑤②⑧①③⑤⑥⑦
【分析】
在水溶液里或熔融状态下导电的化合物是电解质,包括:
酸、碱、盐、金属氧化物、水;
在水溶液和熔融状态下都不导电的化合物是非电解质,包括大多是有机物、非金属氧化物、氨气,单质和混合物,不是化合物,既不是电解质也不是非电解质。
存在自由移动的电子或离子的物质能够导电。
【详解】
①Fe是单质,既不是电解质,也不是非电解质,存在自由移动的电子,能够导电;
②CO2是非金属氧化物,属于非电解质,不能导电;
③NaCl溶液,属于混合物,既不是电解质,也不是非电解质,存在自由移动的离子,能够导电;
④Cu(OH)2是碱,属于电解质,不溶于水,不能导电;
⑤熔融的MgCl2是盐,属于电解质,存在自由移动的离子,能够导电;
⑥NH4Cl溶液,属于混合物,既不是电解质,也不是非电解质,存在自由移动的离子,能够导电;
⑦盐酸属于混合物,既不是电解质,也不是非电解质,存在自由移动的离子,能够导电;
⑧C2H5OH(酒精)水溶液和熔融状态下都不导电的化合物,属于非电解质,不能导电;
所以属于电解质的有:
④⑤;
属于非电解质的有:
②⑧;
能导电的有:
①③⑤⑥⑦,故答案为:
①③⑤⑥⑦。
【点睛】
本题考查了电解质和非电解质的判断,明确二者的概念和区别是解本题关键,注意单质和混合物既不是电解质也不是非电解质,盐酸为易错点。
本题的另一个易错点为导电的物质,要注意常见的导电物质有:
金属单质、电解质溶液、熔融状态的离子化合物和石墨。
22.A.H++OH-===H2O,Cu(OH)2+2H+===Cu2++2H2O
B.H++OH-===H2O,2H++2OH-+Ba2++SO42-===BaSO4↓+2H2O
C.CO32-+2H+===CO2↑+H2O
D.Zn+2H+===Zn2++H2↑
【解析】根据离子方程式的书写步骤,逐一写出离子方程式。
23.:
(1)c
(2)e(3)d(4)d(5)f
【解析】:
(1)中利用CaCO3不溶于水,Na2CO3易溶于水,加水,过滤干燥即可除杂。
(2)中KCl和K2CO3均易溶于水,故不能用过滤法分离;
可用盐酸反应后,再将溶液蒸发即得到氯化钾晶体。
(3)中利用高温分解法,使CaCO3分解除去并生成CaO。
(4)中二者均不溶于水,可利用炭粉易燃方法,选用d。
(5)中利用二者溶解度随温度变化的差异,采用结晶法分离除杂。
24.
(1)①铁架台②试管③烧杯④酒精灯
(2)AEBF
(3)AC有白色沉淀生成
(4)BD防止生成的铜再和氧气反应
(2)中制取氧气,可以采用加热高锰酸钾的方法,氧气的密度比空气重,可以选用向上排空气法收集,故选用的仪器为A和E;
实验室中制取氢气采用Zn和稀H2SO4反应,H2的密度小于空气的密度,可以采用向下排空气法进行收集,故选B和F。
(3)木炭还原氧化铜需要加热,生成物为CO2,检验生成物的方法是将CO2通入澄清的石灰水中,现象为澄清的石灰水变浑浊。
故装置选用A和C
(4)H2还原CuO需要将导管通入试管底部,故选B和D,为了防止生成的Cu被空气中的O2氧化,需要在反应结束时先停止加热,带试管冷却后在停止通氢气。