初三化学 化学质量守恒定律的专项 培优练习题及答案Word文件下载.docx
《初三化学 化学质量守恒定律的专项 培优练习题及答案Word文件下载.docx》由会员分享,可在线阅读,更多相关《初三化学 化学质量守恒定律的专项 培优练习题及答案Word文件下载.docx(20页珍藏版)》请在冰豆网上搜索。
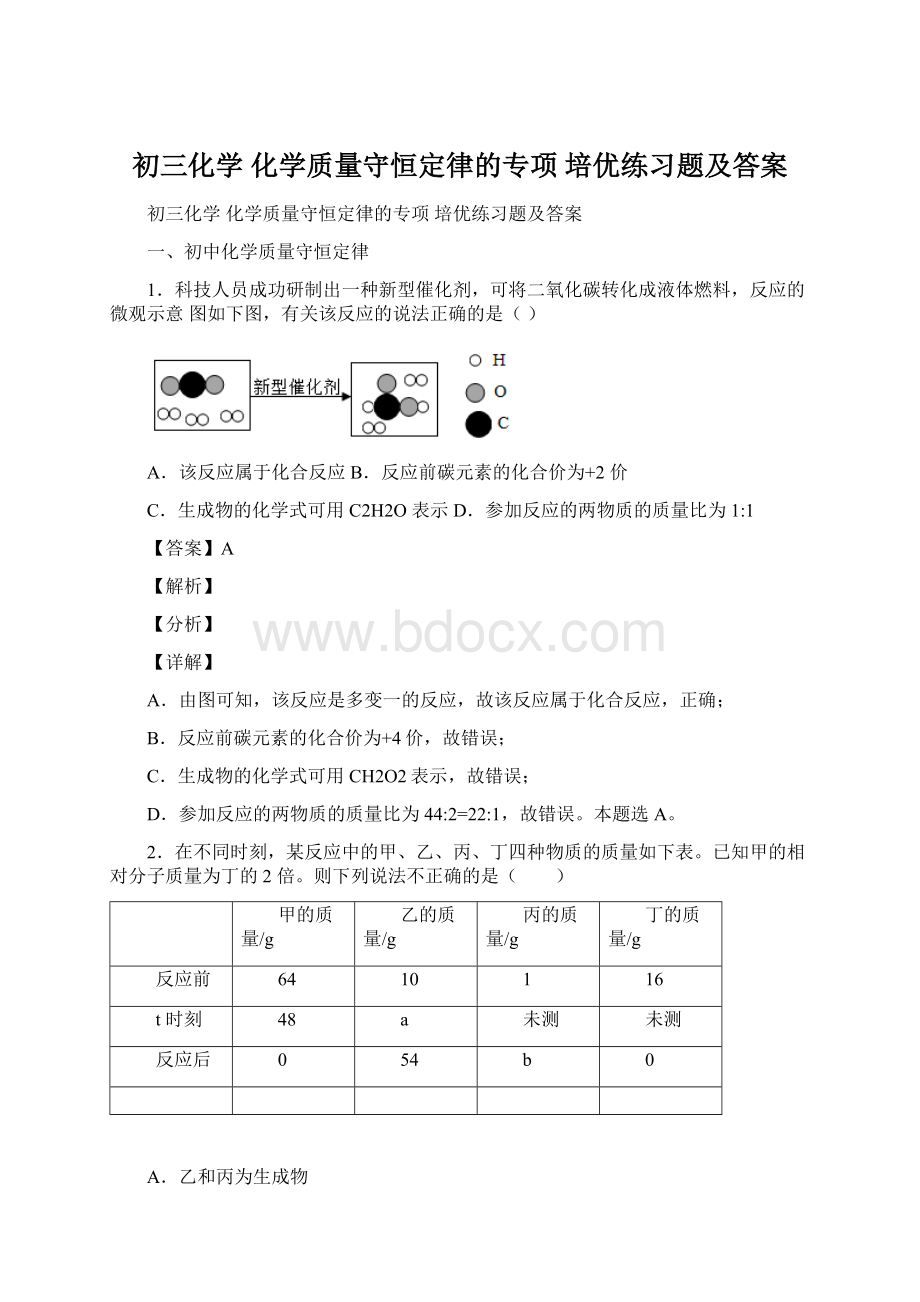
B、设t时刻生成乙的质量为x
x=11g
a=10g+11g=21g,故B正确;
C、根据A中计算结果可知b=37,故C正确;
D、设丁的相对分子质量为m,则甲的相对分子质量为2m,该反应的化学方程式可表示为:
a:
b=2:
1,故D错误。
故选:
D。
3.如图是某汽车尾气净化装置中发生反应的微观示意图。
下列说法正确的是( )
A.该反应中,Z是由Y分解生成的
B.一个Y和W分子中均有11个电子
C.参加反应的X与生成的Z的质量比为9:
7
D.化学反应前后,催化剂的质量和性质一定不变
【答案】C
由反应的微观示意图可以看出,反应物是NH3和NO两种分子,生成物是N2和H2O两种分子,所以化学反应方程式为:
6NO+4NH3
5N2+6H2O。
A、由微粒的构成可知,X、Y都含有氮原子,不能确定Z是由Y分解生成的,故A不正确;
B、由微粒的构成可知,Y和W分子分别是氨分子和水分子,一个Y和W分子中均有10个电子,故B不正确;
C、参加反应的X与生成的Z的质量比为(30×
6)(28×
5)=9:
7,故C正确;
D、化学反应前后,催化剂的质量和化学性质一定不变,故D不正确。
故选C。
【点睛】
根据质量守恒定律,反应前后原子个数不变。
4.下列化学用语书写正确的是
A.3个硝酸根离子:
3NO3-B.2个铝原子:
Al2
C.五氧化二磷分子:
O2P5D.标出氯化镁中氯元素的化合价:
A.由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。
表示多个该离子,就在离子符号前加相应的数字,3个硝酸根离子:
3NO3-,此选项正确;
B.由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,2个铝原子:
2Al,此选项错误;
C.五氧化二磷属于氧化物,氧化物的化学式中,氧元素符号在后,由分子构成的物质,化学式可表示一个该分子,故五氧化二磷分子:
P2O5,此选项错误;
D.化合价标在元素符号的正上方,氯化镁中氯元素的化合价为-1,
,此选项错误。
故选A。
5.自来水消毒过程中常发生下列转化:
A.反应前后分子不可分
B.转化①是化合反应
C.转化②中丙和丁的分子个数之比为1:
D.转化①、②中氯元素的化合价都发生变化
A、由图示可知,一个氯气分子和一个水分子反应生成一个氯化氢分子和一个次氯酸分子。
两个次氯酸分子反应生成两个氯化氢分子和一个氧分子。
化学方程式为:
转化①H2O+Cl2=HCl+HClO;
转化②2HClO
2HCl+O2↑。
由微粒的变化可知,应前后分子发生了变化,分子可再分,错误;
B、由转化①H2O+Cl2=HCl+HClO可知,生成物是两种,不是化合反应,错误;
C、转化②2HClO
2HCl+O2↑中丙和丁的分子个数之比为2:
1,错误;
D、转化①中氯元素的化合价由0变为+1,②中氯元素的化合价由+1,变为-1,都发生改变,正确。
故选D。
点睛:
化学变化的实质是反应物的分子分成原子,原子重新组合成新的分子,反应前后元素种类不变,原子的种类不变、数目、质量都不变;
物质的种类、分子的种类一定发生变化。
6.某化学反应的微观示意图如图所示,则下列说法正确的是()
A.反应前后分子种类、数目均不变
B.该反应属于置换反应
C.该反应中,反应物的质量比是1:
D.该反应的生成物均为氧化物
由反应的微观示意图可知,该反应的化学方程式为CH4+2O2点燃2H2O+CO2。
A、由反应的微观示意图可知,反应前后分子种类该变、数目不变,错误;
B、由反应的微观示意图可知,生成物中没有单质,不属于置换反应,错误;
C、由反应的化学方程式可知,该反应中,反应物的质量比是(12+1×
4):
(2×
16×
2)=1:
4,错误;
D、由反应的化学方程式可知,该反应的生成物是H2O和CO2,均为氧化物,正确。
7.在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
关于此反应的认识不正确的是( )
物质
W
G
H
P
反应前质量/g
18
32
反应后质量/g
待测
26
12
A.物质H一定是该反应的催化剂
B.该反应一定是化合反应
C.在反应物和生成物中,G、P的质量比为5:
4
D.待测值为13
根据质量守恒定律计算出“待测”的值,再根据化学反应后,质量增加的物质是生成物,质量减少的物质是反应物。
A、物质H的质量在反应前后不变,可能是该反应的催化剂,也可能没有参加反应,故A不正确;
B、W、P质量都减少,是反应物,G增加,是生成物,反应物是两种,生成物是一种,H的质量在反应前后不变,属于化合反应而不是分解反应,故B正确;
C、反应中G、P的质量比为25g:
20g=5:
4,故C正确;
D、根据质量守恒定律,反应前后物质的总质量不变,所以18+1+2+32=待测+26+2+12,因此待测=13g,反应后物质待测值W的质量为:
18g﹣5g=13g,故D正确。
在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和。
8.合成尿素的化学方程式为:
CO2+2X
CO(NH2)2+H2O,X的化学式为( )
A.NH3B.N2H4C.HNO3D.NH3•H2O
由质量守恒定律:
反应前后,原子种类、数目均不变。
反应前后,原子种类、数目均不变,由反应的化学方程式
,反应前碳、氢、氧、氮原子个数分别为1、0、2、0,反应后的生成物中碳、氢、氧、氮原子个数分别为1、6、2、2,根据反应前后原子种类、数目不变,则2X分子中含有2个氮原子和6个氢原子,则每个X分子由1个氮原子和3个氢原子构成,则物质X的化学式为
。
9.冰晶石(Cryolite),一种矿物,化学式为NanAlF6,常用在电解铝工业作助熔剂。
已知冰晶石中F显-1价,则n的值为()
A.1B.2C.3D.4
根据化合物中元素的化合价的代数和为零,则(+1)n+(+3)+(-1)×
6=0,则n=3,故选C。
10.A、B、C三种物质各15g,它们化合时只能生成30g新物质D.若增加10gA,则反应停止后,原反应物中只剩余C.根据上述条件推断,下列说法正确的是()
A.第一次反应停止后,B剩余9g
B.第二次反应后,D的质量为60g
C.反应中A和B的质量比是3:
D.反应中A和C的质量比是5:
由题意可知,第一次A全部反应,B、C有剩余;
若增加10gA,25gA时,与15gB也会恰好反应,只剩余C;
设:
第一次反应停止后,参加反应的B的质量为x,第二次反应后,D的质量为y
A+B+C→D
15gx30g
25g15gy
x=9g,因此剩余B是6g;
y=50g
根据质量守恒定律:
第一次参加反应的C的质量=30g﹣15g﹣9g=6g,因此反应中A和C的质量比=15g:
6g=5:
2故选D
11.金属单质M与非金属单质硫发生如下反应为2M+S
M2S。
甲、乙二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同。
充分反应后,实验数据记录如下表,则M的相对原子质量是
M的质量/
S的质量/g
M2S的质量/g
甲
6.0
2.5
7.5
乙
7.0
1.5
A.64B.56C.39D.23
由题中实验数据可知,甲中硫过量、乙中M过量,6.0gM和1.5g硫完全反应,所以根据反应方程式
2M:
32=6g:
1.5g
M=64
则M的相对原子质量是64,故选A。
12.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中正确的是( )
c
d
反应前的质量(g)
8.4
3.2
4.0
2.8
反应后的质量(g)
X
1.6
8.8
A.反应中a和b的质量比为2:
B.d一定是催化剂
C.上表中X=3.2
D.该反应是分解反应
A、X=8.4+3.2+4.0﹣1.6﹣8.8=5.2,反应中a和b的质量比为:
(8.4﹣5.2):
(3.2﹣1.6)=2:
1,该选项说法正确;
B、d反应前后质量不变,可能是催化剂,也可能既不是催化剂也不是反应物和生成物,该选项说法不正确;
C、X=5.2,该选项说法不正确;
D、反应后a、b质量减小,都是反应物,c质量增大,是生成物,该反应是化合反应,该选项说法不正确。
A。
13.在一个密闭容器内,有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量见下表
物质
A
B
C
D
6
111
待测
15
84
依据上表判断,下列说法正确的是()
A.该反应是化合反应B.待测值为22
C.生成A和B的质量比为22:
9D.D物质是该反应的反应物
由表中数据分析可知,反应前后,B的质量增加了9g,是生成物,生成B的质量为9g;
C的质量减少,是反应物,减少的质量是111g;
同理可以确定D是生成物,生成D的质量为80g;
由质量守恒定律,A应是生成物,且生成的质量为111g-9g-80g=22g,反应后丁的质量为4g+22g=26g。
A、由以上分析可知该反应是一种物质反应生成三种物质,所以属于分解反应,错误;
B、反应后密闭容器中A的质量为26g,错误;
C、生成A和B的质量比=22g:
9g=22:
9,正确;
D、D物质是该反应的生成物,错误。
故选C。
本题考查了质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律,在化学反应中质量增加的是生成物,质量减少的是反应物。
14.一定条件下,某装置中发生了化学反应,测得反应前后各物质的质量变化如下表所示。
下列说法中,正确的是()
丙
丁
反应前的质量/g
60
反应后的质量/g
33
x
24
3
A.x的值等于0.5
B.丙和丁的质量变化比为8:
C.乙一定是催化剂
D.该反应是化合反应
【答案】B
由表中数据分析可知,反应前后甲的质量减少了60g﹣33g=27g,故是反应物,参加反应的质量为27g;
同理可以确定丙是生成物,生成的质量为24g﹣0g=24g;
丁是生成物,生成的质量为3g﹣0g=3g;
由质量守恒定律,乙的质量不变,可能作该反应的催化剂,也可能没有参加反应。
A、乙的质量不变,x的值等于1.5,故选项说法错误;
B、丙和丁的质量变化比为24g:
3g=8:
1,故选项说法正确;
C、乙的质量不变,可能作该反应的催化剂,也可能没有参加反,故选项说法错误;
D、该反应的反应物为甲,生成物是丙和丁,符合“一变多”的形式,属于分解反应,故选项说法错误。
故选B。
15.在化学反应2A+B2=2AB中,A与B2反应的质量关系如图所示,现将6gA和8gB2充分反应,则生成AB的质量是
A.12gB.11gC.9gD.14g
由两者反应时的质量关系可知,两者反应的质量比是1:
1,则可判断6gA和8gB2充分反应时B2会剩余2g,根据质量守恒定律可知生成的AB会是12g。
16.在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如下图所示。
图中a、b、c、d分别表示相应物质的质量分数。
下列数据正确的是
A.a=56%B.b=6%C.c=17%D.d=8%
对比图1、图2和图3得,反应后甲和乙质量减少了,丙质量增加了,丁反应前后质量没有变化,则甲+乙
丙。
A、甲由70→42,减少了28,图2应减少14,a=70%-14%=56%;
B、乙由14%→11%,减少了3%,图3应减少6%,b=14%-6%=8%;
C、丙由6%→40%,增加了34,图2应增加17,c=6%+17%=23%;
D、对比图1和图3得,丁反应前后质量分数没有改变,d=10%。
17.2018年10月28日,我国首艘国产航母第三次试海成功。
用到的金属钛主要通过下列反应制得:
①2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,②TiCl4+2Mg═Ti+2MgCl2.则X的化学式为()
A.FeCl3B.FeCl2C.Fe2O3D.FeO
由2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO可知,反应前铁原子是2个,反应后应该是2个,包含在2X中,反应前后钛原子都是2个,碳原子都是6个,氧原子都是6个,反应前氯原子是14个,反应后应该是14个,其中6个包含在2X中,因此X的化学式是FeCl3。
18.煤的气化是提高煤的利用率、减少环境污染的有效措施。
煤的气化过程中发生了化学反应C+H2O(气)
H2+CO,反应前后,发生了变化的是
A.元素的种类B.分子的种类C.原子的数目D.物质的总质量
试题分析:
在化学反应中元素的种类、原子的数目和物质的总质量都不发生改变,分子的种类发生了变化.
考点:
化学变化的实质;
点评:
参加反应的各种物质的质量总和等于反应后各种物质的质量总和,理解质量守恒定律的特征和本质是解题的关键.
19.珍惜生命,远离毒品,每年6月26日是国际禁毒日,毒品冰毒的化学式为C10H15N,下列关于冰毒的说法正确的是( )
A.该物质中碳、氢、氮元素的质量比为10:
15:
B.该物质是由碳、氢、氮三种元素组成的化合物
C.该物质由10个碳原子、15个氢原子和1个氮原子构成
D.该物质充分燃烧只生成二氧化碳和水
A、冰毒中的C、H、N元素的质量比=(12×
10):
(1×
15):
14=120:
15:
14,错误;
B、根据冰毒的化学式可知,冰毒有C、H、N三种元素组成的化合物,正确;
C、根据冰毒的化学式可知,一个冰毒分子由10个碳原子、15个氢原子、1个氮原子构成,错误;
D、根据冰毒的化学式以及质量守恒定律可知,该物质充分燃烧除额生成二氧化碳和水,还应生成含有氮元素的物质,错误。
20.我国古代典籍中有“银针验毒”的记载,其反应原理之一是4Ag+2H2S+O2=2X+2H2O。
下列有关该反应的说法不正确的是
A.X的化学式是Ag2SB.H2S中S元素为-2价
C.反应前后元素的种类不变D.H2S是无毒的
A、由质量守恒定律:
反应前后,原子种类、数目均不变,由反应的化学方程式4Ag+2H2S+O2═2X+2H2O,反应前银、氢、硫、氧原子个数分别为4、4、2、2,反应后的生成物中银、氢、硫、氧原子个数分别为0、4、0、2;
根据反应前后原子种类、数目不变,则2X分子中含有4个银原子和2个原子,则每个X分子由2个银原子和1个硫原子构成,则物质X的化学式为Ag2S,故A说法正确;
B、H2S中H显+1价,故S元素为-2价,故B说法正确;
C、由质量守恒定律可知,反应前后元素的种类不变,故C说法正确;
D、在反应4Ag+2H2S+O2═2Ag2S+2H2O中,能用银检验的有毒物质就是H2S,故D说法错误。
21.下图为甲烷与水反应得到水煤气的反应微观示意图:
下列有关说法错误的是:
A.该反应前后存在元素化合价的变化
B.反应物的分子个数比为1:
C.反应前后分子的种类发生了改变
D.四种物质中有三种氧化物
【解析】由图示可知,该反应的反应物是甲烷和水,生成物是一氧化碳和氢气,反应的化学方程式为:
CH4+H2O
CO+3H2;
A.反应前在甲烷中碳元素的化合价是-4,反应后在一氧化碳中碳元素的化合价是+2,发生了改变,故A正确;
B.由上述方程式可知,反应物的分子个数比为1:
1,故B正确;
C.由微粒的变化可知,反应前后分子的种类发生了改变,故C正确;
D.由反应的方程式可知,四种物质中有CO、H2O两种氧化物,故D不正确;
22.甲和乙在一定条件下反应生成丙和丁。
结合微观示意图分析,下列结论正确的是
A.丙的相对分子质量为32gB.丙中C、H、O元素的质量比为3:
1:
C.生成的丙和丁的分子个数比为2:
1D.该反应为置换反应
A、相对分子质量不能带g,故错误;
B、丙物质中碳、氢、氧元素的质量比为12:
4:
16=3:
4,故正确;
C、该反应的化学方程式为CO2+3H2
CH3OH+H2O,故生成的丙和丁的分子个数比为1:
1,故错误;
D、该反应的生成物中没有单质,故不可能是置换反应,故错误。
23.如图为某反应的微观示意图,其中“
”和“
”表示不同元素的原子。
下列说法正确的是()
A.反应前后原子数目发生改变
B.反应前后分子种类没有改变
C.该反应属于化合反应
D.参加反应的两种分子个数比为1∶2
A、由反应的微观示意图可知,反应前后原子种类、数目没有发生改变,选项A错误;
B、图中可知,反应前后分子种类发生了改变,选项B错误;
C、该反应由两种物质生成了一种物质,符合化合反应的特征,属于化合反应,选项C正确;
D、图中可知,参加反应的两种分子个数比为1∶1,选项D错误。
24.在一密闭容器内有M、N、Q、R四种物质,在一定条件下充分反应,反应前后各物质质量如表,则下列说法正确的是( )
M
N
Q
R
反应前质量(g)
5
反应后质量(g)
11
85
A.该反应属于化合反应
B.待测物质N的质量为22g
C.该反应属于分解反应
D.反应中M、N、Q、R四种物质质量比为9:
37:
80:
根据化学反应前后物质的总重量不变,可得;
2+15+5+111=11+待测+85+0,故待测=37g,所以反应后密闭容器中N的质量为37g;
根据各物质反应前后质量的增减,即反应后质量增加的为生成物,反应后质量减少的为反应物,可知M、N、Q是生成物,R是反应物;
故该反应为R→M+N+Q是分解反应;
该反应中四种物质(参加反应或生成)的质量比为(11-2):
(37-15):
(85-5):
(111-0)=9:
22:
111,故D答案是错误的。
先利用质量守恒定律,计算出待测物质的质量,然后根据反应前后物质质量的增或减判断反应的反应物与生成物判断反应,此为解决该类问题的一般方法。
25.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如表:
反应前的质量(g)
56
下列说法不正确的是( )
A.x为64B.参加反应的乙的质量为18g
C.参加反应的甲物质的质量为46gD.丙物质一定作催化剂
根据质量守恒定律可知:
反应前各物质的质量总和=反应后生成各物质的质量总和,所以X=56+18+2+0-10-0-2=64;
根据反应中反应物质量会减少,生成物质量会增加,可以判断反应物为:
甲、乙,而生成物为丁,丙质量不变,可能做催化剂
A、X=56+18+2+0-10-0-2=64,正确;
B、参加反应的乙的质量为18g,正确;
C、参加反应的甲物质的质量为56g-10g-46g,正确;
D、丙质量不变,可能做催化剂,错误。
26.如图是甲、乙、丙三种物质转化的微观示意图,其中
和
分别表示两种质子数不同的原子.下说法正确的是( )
A.反应前后分子数没有改变
B.甲、乙、丙均属于化合物
D.甲的相对分子质量等于乙、丙的相对分子质量之和
A、由反应前后微粒的变化可知,每两个甲分子反应后生成了一个乙分子和两个丙分子,分子数发生了改变,故A不正确;
B、由物质的微观构成示意图可知,乙是由同种的原子构成的同种的分子构成的物质,属于单质,故B不正确;
C、由三种物质转化的微观示意图可知,该反应由一种物质生成了两种物质,属于分解反应,故C正确;
D、由质量守恒定律可知,参加反应的甲的质量等于生成的乙、丙的质量之和,故D不正确。
27.下图为某化学反应的微观模拟示意图,下列说法中,不正确的是
A.该反应不属于置换反应
B.图示中x的数值为3
C.反应前后氢元素的化合价发生了改变
D.反应中甲、丙两物质的质量比为2:
由图,结合质量守恒定律,该反应的方程式为CH4+H2O==CO+3H2。
A、置换反应为一种单质和一种化合物生成另一种单质和化合物的反应,而该反应为2种化合物生成一种单质和一种化合物的反应,不属于置换,正确;