化学高考评价标准Word格式文档下载.docx
《化学高考评价标准Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《化学高考评价标准Word格式文档下载.docx(9页珍藏版)》请在冰豆网上搜索。
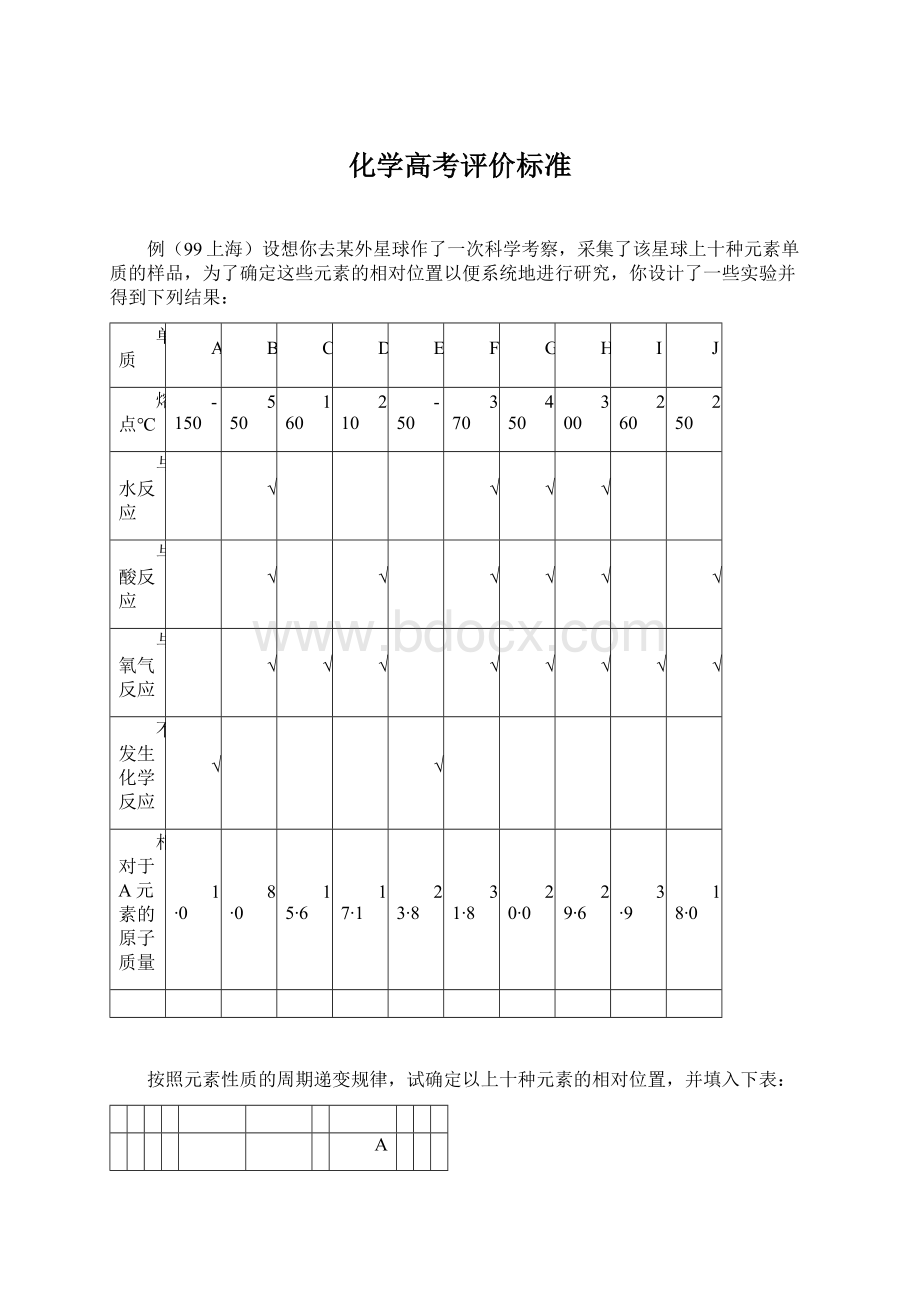
370
450
300
260
250
与水反应
√
与酸反应
与氧气反应
不发生化学反应
相对于A元素的原子质量
1∙0
8∙0
15∙6
17∙1
23∙8
31∙8
20∙0
29∙6
3∙9
18∙0
按照元素性质的周期递变规律,试确定以上十种元素的相对位置,并填入下表:
A
(06江苏)写出NaClO的溶液与SO2反应的离子方程式:
ClO-+SO2+2OH-=H2O+Cl-+SO42-。
NaClO与NH3反应生成化合物J,J由两种元素组成,其相对分子质量为32,J的化学式:
N2H4。
例(06四川-12)(4)已知尿素的结构简式为H2N-
-NH2,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
答:
①H-
-NH-NH2;
②NH4N=C=O
(07北京)某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
实验步骤
实验现象
将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中。
产生气泡,析出疏松的红色固体,溶液逐渐变为无色。
反应结束后分离出溶液备用
红色固体用蒸馏水洗涤后,置于潮湿空气中。
一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。
持续电解,在阴极附近的溶液中还可以观察到的现象是白色沉淀生成,后沉淀逐渐溶解至消失
解释此现象的离子方程式是Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O。
(08北京)由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去):
(5)另取原样品,加入足量稀硫酸充分反应。
若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中的物质用化学式表示)__CuO、C;
Fe2O3、CuO、C、___Fe2O3、Fe、CuO、C、_____________________________。
07江苏-12
花青苷是引起花果呈现颜色的一种花色素,广泛存在于植物中。
它的主要结构在不同pH条件下有以下存在形式:
下列有关花青苷说法不正确的是(B)
A.花青苷可作为一种酸碱指示剂
B.I和Ⅱ中均含有二个苯环
C.I和Ⅱ中除了葡萄糖基外,所有碳原子可能共平面
D.I和Ⅱ均能与FeCl3溶液发生显色反应
(05全国I)
某酒精厂由于管理不善,酒精滴漏到某种化学品上而酿成火灾。
该化学品可能是
AKMnO4BNaCl
C(NH4)2SO4DCH3COOH
(09宁夏)
下列化合物中既能使溴的四氯化碳溶液褪色,又能在光照下与溴发生取代反应的是
A.甲苯B.乙醇C.丙烯D.乙烯
(06广东-10)下列物质性质的变化规律,与共价键的键能大小有关的是
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.HF、HCl、HBr、HI的热稳定性依次减弱
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
钠与水的反应
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中
配制一定浓度的氯化钾溶液1000mL
准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶解,振荡摇匀,定容
排除碱式滴定管尖嘴部分的气泡
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出
取出分液漏斗中所需的上层液体
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
(07江苏)
阿伏加德罗常数约为6.02×
1023mol-1,下列叙述正确的是
A.2.24LCO2中含有的原子数为0.3×
6.02×
1023
B.0.1L3mol·
L-1的NH4NO3溶液中含有的NH4+数目为0.3×
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3×
*D.4.5SiO2晶体中含有的硅氧键数目为0.3×
(07广东)下列实验操作完全正确的是(C)
(05全国II)下图中的实验装置可用于制取乙炔。
请填空:
(1)图中,A管的作用是:
调节水面高度以控制反应的发生和停止;
制取乙炔的化学方程式是
(06上海)
在标准状况下,向100mL氢硫酸溶液中通人二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为
A0.5mol/LB0.05mol/L
C1mol/LD0.1mol/L
(05上海)某些废旧塑料可采用下列方法处理:
将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如右
图。
加热聚丙烯废塑料得到的产物如下表:
产物
氢气
甲烷
乙烯
丙烯
苯
甲苯
碳
质量分数(%)
12
24
16
20
10
6
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物
电石
乙炔
聚乙炔
写出反应②、③的化学方程式
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有种。
(3)锥形瓶C中观察到的现象。
经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为。
(4)写出C中逸出的气体在工业上的两种用途、。
(2009北京)
28-②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解),该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果:
铵盐质量为10.00g和20.00g时,浓硫酸增加的质量相同;
铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;
铵盐质量为40.00g时,浓硫酸的质量不变。
计算:
该铵盐中氮元素的质量分数是%;
若铵盐质量为l5.00g,浓硫酸增加的质量为。
(计算结果保留两位小数)
14.562,31g
25。
C时,若体积为Va、pH=a的某一元酸与体积为Vb,pH=b的某一元强碱混合,恰好中和,且已知Va<
Vb,a=0.5b。
请填写下列空白:
(1)a值可否等于3(填“可”或“否”)其理由是
(2)a值可否等于5(填“可”或“否”)其理由是
(3)a的取值范围是
(05北京)某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·
6H2O晶体。
(图中夹持及尾气处理装置均已略去)
(1)装置B中发生反应的化学方程式是。
(2)装置E中的现象是黑色固体变红,右端管壁有水珠
(08北京)一定温度下,将1molN2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。
温度由T1继续升高到T2的过程中,气体逐渐变为无色。
若保持T2,增大压强,气体逐渐变为红棕色。
气体的物质的量n随温度T变化的关系如图所示。
①温度在T1-T2之间,反应的化学方程式是
_________2NO2===2NO+O2________________。
_2NO2===N2+2O2_____
(08宁夏)为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案二:
将
g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.02000 mol·
L-1的KMnO4溶液滴定,达到终点时消耗了25.00 mLKMnO4溶液。
(4)若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析。
方案二 (填“准确”“不准确”“不一定准确”),理由是 ;
方案二不准确,如果铁片中存在与稀硫酸反应而溶解的其他金属,生成的金属离子在酸性溶液中能被高锰酸钾氧化,会导致结果偏高;
如果存在与稀硫酸反应而溶解的铁的氧化物,生成的Fe3+离子在酸性溶液中不能被高锰酸钾氧化,会导致结果偏低
06全国I(标准答案与评分细则)
在呼吸面具和潜水艇中可用过氧化纳作为供氧剂。
请选用适当的化学试剂和实验用品、用上图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(4)试管F中收集满气体后,下一步实验操作是:
把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气。
(09全国I)
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是
A.Ba2+、NO3-、NH4+、Cl-
B.Ca2+、HCO3-、NH4+、AlO2-
C.K+、Ba2+、Cl-、HSO3-
D.Mg2+、NH4+、SO42-、K+
(08全国I)
在溶液中加入中量Na2O2后仍能大量共存的离子组是(B)
A.NH+4、Ba2+、Cl-、NO-3
B.K+、AlO-2、Cl-、SO42-
C.Ca2+、Mg2+、NO-3、HCO-3
D.Na+、Cl-、CO2-3、SO2-3