化学68单元Word格式文档下载.docx
《化学68单元Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《化学68单元Word格式文档下载.docx(11页珍藏版)》请在冰豆网上搜索。
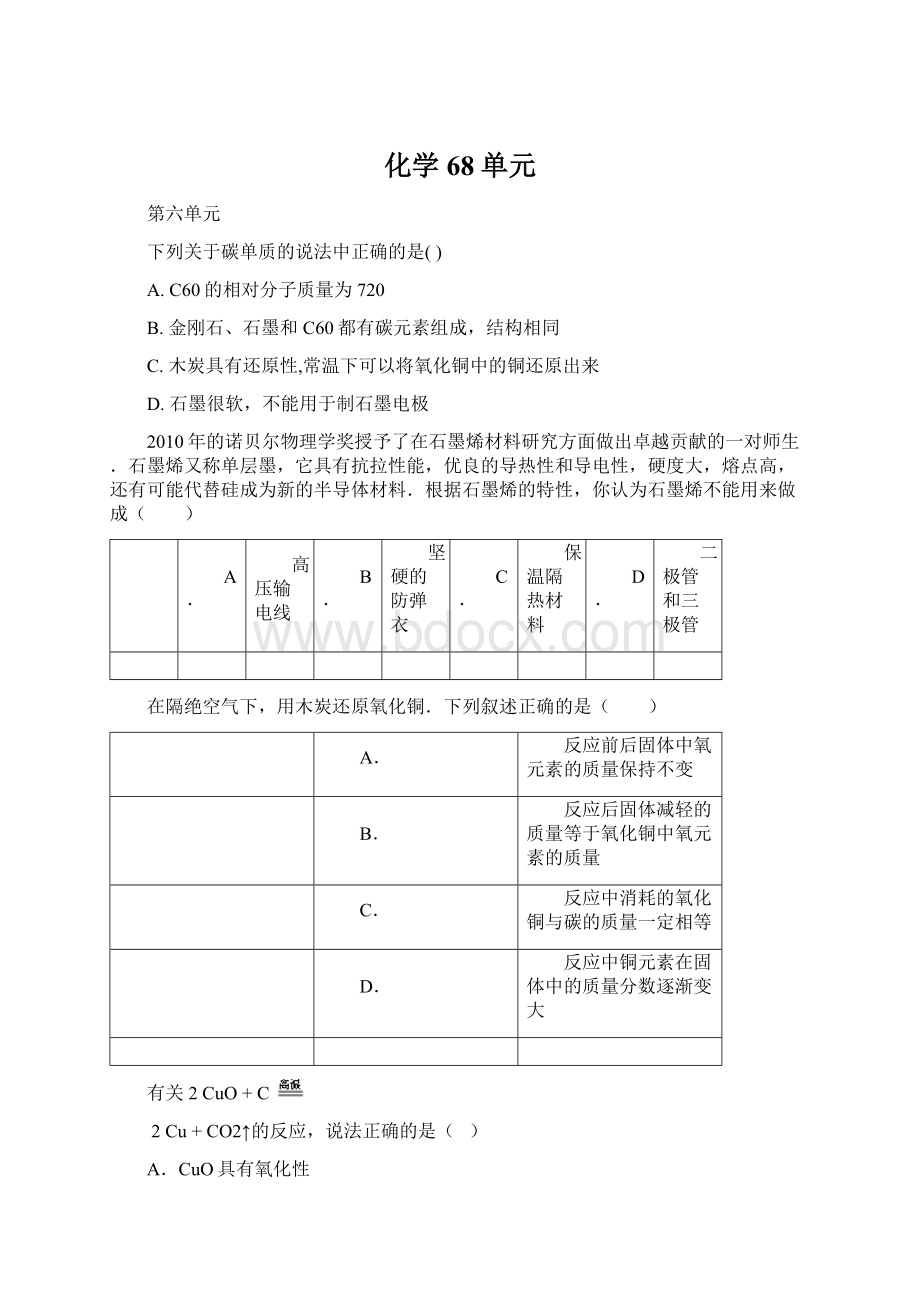
B.C发生了还原反应
C.反应前后氧元素的化合价没有改变
D.反应前后固体质量不变
木炭和二氧化锰的颜色都是黑色,我们可以用方法来区分它们,所使用的方法是
(填“物理方法”或“化学方法”)。
除去氧化铜中的炭粉的最好方法是( )
隔绝空气加热混合物
在空气中加热混合物
在氧气流中加热混合物
在二氧化碳流中加热混合物
已知在一定条件下14g碳与20g氧气恰好完全反应,则反应的产物是()
A.只有COB.既有CO,又有CO2
C.只有CO2D.无法确定
右图是木炭与氧化铜的实验,大试管中的反应体现了碳的性.
(1)酒精灯加灯罩的目的;
(2)刚开始预热,试管②中立即产生气泡,但澄清石灰水不变浑浊,原因是________;
(3)判断反应发生的现象是,实验中产生的气体可能是:
、、
(4)是否可以不待试管冷却就把试管里的粉末倒在纸上?
原因是
下图为初中化学常见气体的发生与收集装置.有关这些装置的说法不正确的是( )
装置I可作为固体加热制取气体的发生装置
装置Ⅱ中长颈漏斗可以用分液漏斗、医用注射器代替
装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体
装置Ⅴ可以用于收集H2、O2,也可以用于实验室收集CO2
如图装置可用来收集气体,试回答下列问题.
(1)若用向上排空气法收集氧气,则氧气应从导管口 通入,空气从导管口 排出.若收集氢气(氢气的密度比空气小),则氢气应从导 通入,空气从管口 排出.如要检验是否已收集满了氧气,可将带火星的木条放在 处.
(2)若用排水法收集氧气,瓶内装满水,气体从 端通入.若装置中储存了氧气,现要用水将装置中的氧气排出进行实验,水应从 端通入.
取四朵用石蕊试液染成紫色的干燥纸花进行如下操作,能观察到纸花变红的是:
用
Y
形管或
形导管完成以下实验。
(1)图
9
中
形管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的现象:
________________________,用分子的观点解释这一现象:
________________________。
(2)图
10
形导管平放于桌面,实验中可观察到的现象;
________________________,用化学方程式解释结论:
________________________;
若把
形导管固定在铁架台上(如图
11),a
管位于上方,
b
管位于下方,两石蕊试纸均湿润,可观察到
管中试纸变色比
a
管明显,原因:
从能量变化角度看,“放出大量的热”是能转化为热能和。
如图是用一氧化碳还原氧化铜的实验装置图。
(1)实验时,要先通入一氧化碳,过一会儿再给氧化铜加热,其原因是
。
(2)根据实验事实填写下列空白:
观察到的现象
发生反应的化学方程式
A处
B处
C处
C处设置一个点燃的酒精灯的目的是
有一混合气体的成分中可能含有水蒸气、一氧化碳、二氧化碳,某同学设计了如下的实验装置探究混合气体的成分.请根据要求回答下列问题:
(1)实验中,证明混合气体中有水蒸气的现象是白色固体变为蓝色;
若B中澄清石灰水出现________现象,则证明混合气体中有二氧化碳,证明混合气体中有一氧化碳的现象是________或________.
(2)若混合气体中含有CO,在F处尚缺少的实验仪器的名称是________.
(3)如果将上述装置中的A,B交换.则不能检验混合气体中是否含有________.
第七章
家用燃气主要有天然气(主要成份CH4)、管道煤气(主要成分是H2、CH4、CO)和罐装液化石油气(主要成分是C3H8、C4H10、C3H6、C4H8)等,小明家的燃气由罐装液化石油改为天然气,他家的灶具和燃气泄露报警器的位置都要进行调整。
(1)燃气泄漏报警器的位置要从低于灶具的地方移到高于灶具的地方,原因是
。
(2)如果厨房里发生燃气泄漏,是否可以开灯检查?
____________________(填“是”或“否”)。
(3)燃气燃烧不充分时火焰就会显黄色或有黑烟,这时可调大气灶__________(填“空气”或“燃气”)进入量或调小气灶__________(填“空气”或“燃气”)进入量。
(4)低碳经济是一种以低能耗、高效能和较少温室气体排放获得较大产出的新经济发展模式。
下列不属于“低碳”行为的是()
A.少用冰箱储存食物B.出门时随手关闭电器电源
C.购物时尽量使用一次性塑料袋D.用节能灯替换家里的白炽灯泡
某物质A在氧气中充分燃烧后只生成二氧化碳和水,为确定A的组成,某同学进行了如下探究.〔在本题中,浓硫酸用于吸收生成的水,碱石灰用于吸收生成的二氧化碳〕
猜想一:
A中只含C、H两种元素
猜想二:
A中只含C、H、O三种元素
〔结论〕猜想 (选“一”或“二”)正确.
〔反思〕物质A中所含元素的质量比为 .
石油资源紧张曾是制约中国发展轿车事业,尤其是制约轿车进入家庭的重要因素.推广“车用乙醇汽油”对轿车进入家庭起着重要的作用.乙醇在空气中完全燃烧生成CO2和H2O.(可知:
白色硫酸铜粉末遇水变成蓝色晶体,氢氧化钠溶液能吸收二氧化碳)
编号
①
②
③
④
装置
(1)写出乙醇完全燃烧的化学方程式________.
(2)乙醇燃烧时如果氧气不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO、CO2、H2O,应将乙醇燃烧产物依次通过(按气流从左到右顺序填装置编号):
________.(按气流从左至右顺序填装置编号)
(3)实验时可观察到装置②中A瓶的石灰水变浑浊,C瓶的石灰水不变浑浊.A瓶溶液的作用是;
B瓶溶液的作用是_;
C瓶溶液的作用是________.
(4)装置③的作用是________.装置①中所盛的是________溶液,作有是________.
(5)装置④中所盛的固体药品是________,它可以确证产生是________.
(6)尾气应如何处理?
________
(7)若乙醇燃烧产生CO、CO2、H2O的总质量是27.6g,其中H2O占10.8g,则参加反应的乙醇为________g,产物中CO为________g.
(8)海底有大量的甲烷水合的.等质量的甲烷和乙醇,完全燃烧产生温室气体CO2较多的是________.
选择铸造硬币的材料不需要考虑的因素是()
A.金属的导电性B.金属的耐腐蚀性C.金属的硬度D.金属资源是否丰富
阅读表格,综合考虑表中各方面的因素,回答以下问题:
金属
全球产量/
(104吨)
密度/(g・cm-3)
熔点/℃
导热
性能
导电
市场价格/
(元/吨)
铝
15000
2.7
660
4
16000
铜
8000
8.9
1083
2
17700
金
19.3
1063
3
88000000
铁
301430
7.9
1540
8
7
2200
铅
3000
11.3
327
9
4900
银
10.5
961
1
1365000
注:
表中导热性能、导电性能1~9是指其性能由强到弱的排列顺序。
⑴导电性能最好的两种金属是
⑵在你认为导电性能好的金属中,那种更适宜作导线?
为什么?
⑶有人说因为铝的导热性能比铁好,所以建议用铝锅烧饭要比铁锅好?
你同意这种说法吗?
请你说明理由。
⑷为什么用铝锅炒菜时锅底易变形,而铁锅则不会?
铁是应用最广泛的金属。
(1)写出铁丝在氧气中燃烧的化学方程式
▲
(2)新型材料纳米级Fe粉能用作高效催化剂。
实验室采用还原法制备纳米级Fe粉,其流程如下图所示:
①纳米级Fe粉在空气中易自燃。
实验中通人N2的目的是
②写出Ⅱ中H2还原FeCl2,置换出铁的化学方程式
某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案.结合实验方案回答下列问题:
(1)步骤①中,金属X是________,该反应的化学方程式为________;
(2)步骤②中,加入过量稀硫酸的目的是________;
(3)从滤液中获得硫酸亚铁晶体采用的方法是________.
某兴趣小组决定探究Ni、Fe、Cu的金属活动性顺序.
(1)
【查阅资料】
镍能与盐酸或稀硫酸反应,生成可溶于水的正二价镍盐,并放出氢气.
①写出镍与盐酸反应的化学方程式_____.
②结合所学知识,_____(填“能”或“不能”)直接比较出Ni、Fe的金属活动性强弱.
(2)
【探究实验】
(所用金属片均已用砂纸打磨.)
实验步骤
实验现象
实现结论
相同浓度的NiSO4
铁片表面有固体析出,铜片表面_____.
三种金属活动性由强到弱的顺序为_____.
(3)
【迁移应用】
用镍片、硫酸亚铁溶液和_____溶液通过实验也能判断Fe、Ni、Cu的金属活动性顺序.
金属单质A可发生如下系列变化.
试推断:
1,A、B、C、D、E分别是(写化学式B写主要成分),
A______、B______、C______、D______、E______.
2,写出③和⑤两反应的化学方程式.③___⑤______.
下图1是实验室模拟炼铁的装置图,试回答
(1)仪器①名称是;
仪器②的名称是
(2)实验过程中仪器①内发生反应的化学方程式是,仪器③中的现象是
3)实验过程中酒精灯的作用是。
(4)按图1接实验装置、检查装置的气密性、装药品、固定实验装置后,主要实验步骤有:
①通入一氧化碳;
②停止通入一氧化碳;
③点燃酒精灯;
④熄灭酒精喷灯;
⑤熄灭酒精喷灯.正确的操作顺序是(填序号).
(5)图2是工业生产中炼铁高炉的结构图.实际生产中炼铁的原料从入口加入,其中焦炭在高炉中的作用之一是产生高温,另一作用为;
生铁出口低于炉渣出口的原因是。
(6)取少量高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,可观察到的现象是
,发生反应的化学方程式为。
当反应停止后,还可观察到烧杯底部有黑色不溶物,该物质主要是
(填化学式)
铜是人类最早利用的金属之一。
(1)下列铜制品中,利用金属导热性的是
(填字母序号)。
A.铜质奖牌
B.铜导线
C.铜火锅
(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流
程如下(反应条件已略去):
已知:
①过程Ⅱ中分离操作的名称是
②过程Ⅲ中有气体产生,反应的化学方程式为
③A~E中含铜、锌两种元素的物质有
某兴趣小组对物质的性质和成分进行相关探究。
(1)常见金属活动性顺序如下,填写相应的元素符号:
金属活动性由强逐渐减弱
某同学用硫酸铜溶液把“铁刀变成铜刀”,其反应的化学方程式为
,该反应的基本反应类型为
(2)兴趣小组同学用氧化铜与足量的炭粉利用图甲所示的装置进行实验,对生成气体的成分进行探究。
甲
[提出问题]生成的气体中是否含有一氧化碳?
[实验与讨论]
①打开K,缓缓通入干燥的氮气一段时间。
②关闭K,加热至一定温度使之反应,用气囊收集气体样品。
③除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列装置中最为合理的是
[实验求证]
将除尽二氧化碳后的气体样品干燥,仍然用图甲所示的装置进行实验,A中的固体应选用
,B中溶液为澄清石灰水,若A中黑色固体出现了红色,B中澄清石灰水
,可说明气体样品中含有一氧化碳。
[实验反思]
炭粉还原氧化铜的实验中,若生成的气体中含有一氧化碳,则反应时消耗碳、氧元素的质量比
(填“大于”、“等于”或“小于”)3∶8。