商丘高考二模理综试题及答案Word文件下载.docx
《商丘高考二模理综试题及答案Word文件下载.docx》由会员分享,可在线阅读,更多相关《商丘高考二模理综试题及答案Word文件下载.docx(22页珍藏版)》请在冰豆网上搜索。
D.图中的“营养”是指落叶和枯枝中能被植物再利用的有机营养
6.下列各项说法中,错误的是
A.种植过大片草莓的农田,闲置数年后被杨、柳等木本植物覆盖,成片的草莓不见了。
这属于群落的次生演替
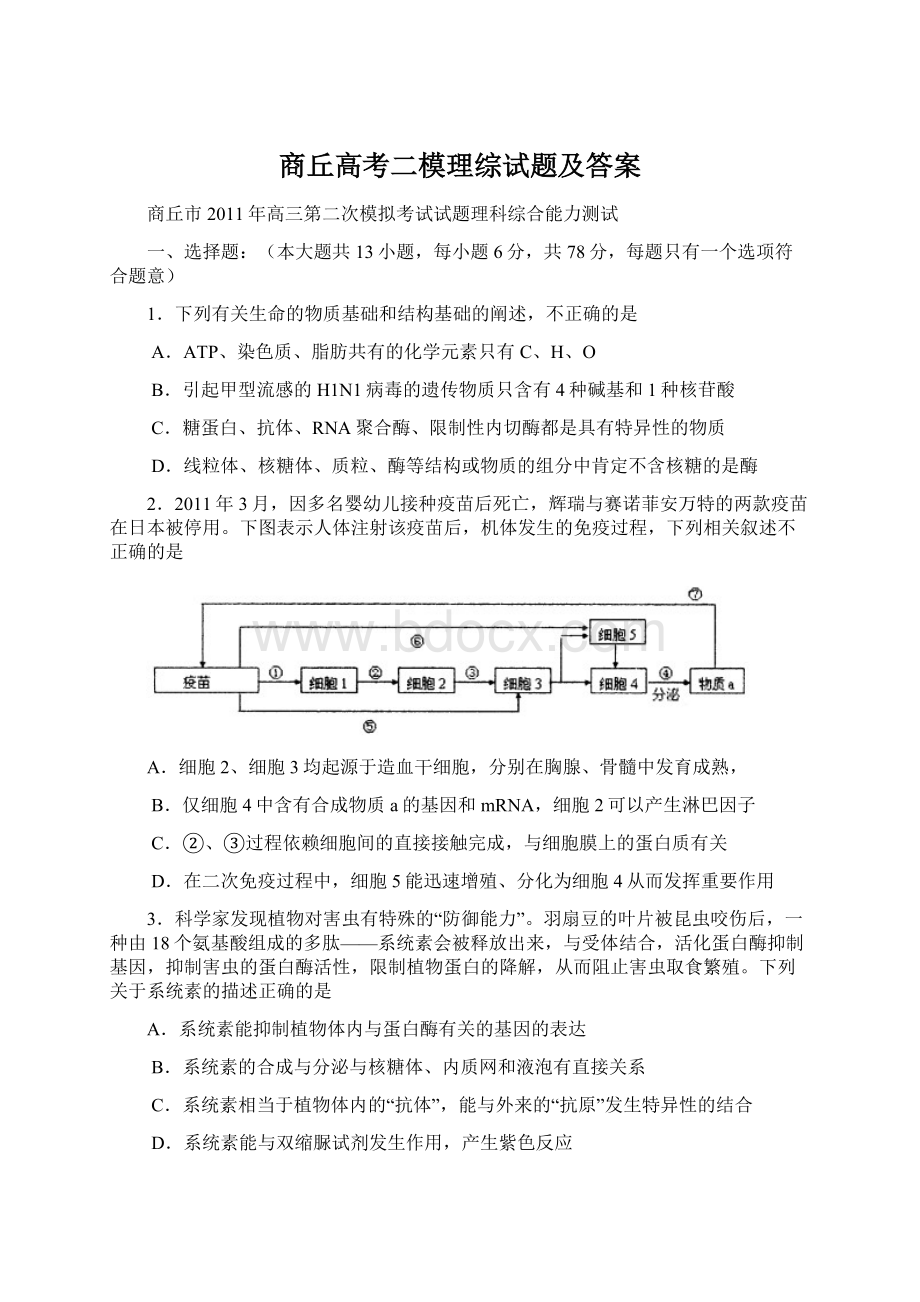
B.烟草、莴苣等植物的种子必须接受某种波长的光信息,才能萌发生长,这说明信息传递能够调节生物种间关系,维持生态系统的稳定
C.将离体神经纤维放入低钠溶液中,受刺激后产生的动作电位锋值比正常值低
D.同无性生殖相比,有性生殖产生的后代具有更大的变异性,其根本原因是产生的新的基因组合机会多
7.下列说法不正确的是
A.云、烟、雾等均能产生丁达尔现象
B.开发氢能、太阳能、风能、生物质能等新型能源是践行低碳生活的有效途径
C.用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量
D.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
8.工业上生产MnO2和Zn的主要反应有:
①MnO2(矿石)+ZnS+2H2S4=MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O
MnO2+Zn+2H2SO4下列说法正确的是
A.①中MnO2和H2SO4都是氧化剂B.①中析出32gS时转移1mol电子
C.②中MnSO4发生氧化反应D.②中生成的Zn在阳极析出
9.某无色溶液,由Na+、Ca2+、Al3+、Cu2+、
、
中的若干种组成。
取适量该溶液进行如下实验:
①加入过量盐酸,有无色、无味气体X生成;
②在①所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
③在②所得溶液中加入过量Ba(OH)2溶液并加热,有刺激性气味的气体Y生成,并析出白色沉淀乙。
则下列判断正确的是
A.原溶液中一定存在的离子是Na+、
B.原溶液中一定存在的离子是Al3+、
C.白色沉淀甲为Al(OH)3、乙为BaSO4
D.气体X为CO2、气体Y为SO2
10.有机物A可以发生下列反应:
已知C能发生银镜反应,E不发生银镜反应。
则A的可能结构有
A.1种B.2种C.3种D.4种
11.下列有关叙述错误的是
A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸
B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
C.某反应△H>
0,△S>
0,该反应可能自发进行
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(
)=9.9×
10-7mol/L.
12.下列有关化学实验操作的叙述正确的是
A.在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液
B.向SO2溶液中分别滴加Ba(NO3)2、BaCl2、Ba(OH)2溶液,均产生BaSO3白色沉淀
C.向2.0mL浓度均为0.1mol/L的KCl和Kl混合溶液中滴加1~2滴0.01mol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大
D.分别电解熔融氯化镁和熔融氯化铝可以制取金属镁和金属铝
13.下列各溶液中,微粒的物质的量浓度关系正确的是
A.等体积、等物质的量浓度的CH3COONa与CH3COOH溶液混合:
2c(Na+)=c(CH3COO-)+c(CH3COOH)
B.0.1mol/LpH为10的NaHB溶液中:
c(HB-)>
c(B2-)>
c(H2B)
C.常温下,将pH=10的NaOH溶液和pH=4的CH3COOH溶液等体积混合:
c(Na+)=c(CH3COO-)>
c(H+)=c(OH-)
D.等物质的量浓度的(NH4)2SO4和(NH4)2CO3溶液中的c(
):
前者<
后者
二、选择题(本题共8小题,共计48分。
在每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对得6分,选对但不全的得3分,有选错或不选的得0分)
14.在物理学发展过程中,有许多伟大的科学家做出了巨大贡献。
关于科学家和他们的贡献,下列说法正确的是
A.库仑最早引入电场概念,并采用了电场线描述电场
B.牛顿发现了万有引力定律,并测出了万有引力常量G
C.伽利略运用理想实验法得出“力不是维持物体运动的原因”
D.奥斯特发现了电流磁效应,并发现了磁场对电流的作用规律
15.某质点从静止开始做匀加速直线运动,已知第3秒内通过的位移是s,则物体运动的加速度大小为
A.3s/2B.2s/3C.2s/5D.5s/2
16.美国科学家通过射电望远镜观察到宇宙中存在一些离其他恒星较远的、由质量相等的三颗星组成的三星系统:
三颗星位于同一直线上,两颗环绕星围绕中央星在同一半径为R的圆形轨道上运行。
设每个星体的质量均为M,忽略其它星体对它们的引力作用,则
A.环绕星运动的角速度为
B.环绕星运动的线速度为
C.环绕星运动的周期为T=4π
D.环绕星运动的周期为T=2π
17.如图所示,质量为M、半径为R、内壁光滑的半球形容器静止在粗糙水平地面上。
O为球心。
有一劲度系数为K的轻弹簧一端固定在半球底部
处,另一端与质量为m的小球相连,小球静止于P点。
已知地面与半球形容器间的动摩擦因数μ,OP与水平方向的夹角为θ=30°
.下列说法正确的是
A.小球受到轻弹簧的弹力大小为KR
B.小球受到容器的支持力大小为
mg
C.小球受到容器的支持力大小为mg
D.半球形容器受到地面的摩擦力大小为μ(M+m)g
18.一小物块以某一初速度滑上水平足够长的固定木板,经一段时间t后停止。
现将该木板改置成倾角为30°
的斜面,让该小物块以相同大小的初速度沿木板上滑。
若小物块与木板之间的动摩擦因数为μ,则小物块上滑到最高位置所需时间t′与t之比为
A.
B.
C.
D.
19.如图所示,在离地面高为H处以水平速度v0抛出一质量为m的小球,经时间t,小球离水平地面的高度变为h,此时小球的动能为EK,重力势能为EP(选水平地面为零势能参考面)。
下列图象中大致能反映小球动能Ek、势能EP变化规律的是
20.带有等量异种电荷的平行金属板M、N水平放置,两个电荷P和Q以相同的速率分别从极板M边缘和两板中间沿水平方向进入板问电场,恰好从极板N边缘射出电场,如图所示。
若不考虑电荷的重力和它们之间的相互作用,下列说法正确的是
A.两电荷的电荷量可能相等B.两电荷在电场中运动的时间相等
C.两电荷在电场中运动的加速度相等D.两电荷离开电场时的动能相等
21.如图所示,将一根绝缘硬金属导线弯曲成一个完整的正弦曲线形状,它通过两个小金属环a、b与长直金属杆导通,在外力F作用下,正弦形金属线可以在杆上无摩擦滑动。
杆的电阻不计,导线电阻为R,ab间距离为2L,导线组成的正弦图形项部或底部到杆距离都是L/2。
在导线和杆平面内有一有界匀强磁场区域,磁场的宽度为2L,磁感应强度为B.现在外力F作用下导线沿杆以恒定的速度v向右运动,在运动过程中导线和杆组成的平面始终与磁场垂直。
t=0时刻导线从O点进入磁场,直到全部穿过磁场,外力F所做功为
第Ⅱ卷(非选择题,共174分)
三、非选择题(包括必考题和选考题两部分。
第22题~第32题为必考题,每个小题考生都必须作答。
第33题~第40题为选考题,考生根据要求作答)
(一)必考题
22.(6分)
(1)多用电表的读数为________________。
(2)用游标20分度的游标卡尺测量某工件的内径时,示数如图所示,则测量结果应该
读作________mm。
(3)用螺旋测微器测圆柱体的直径时,示数如图所示,此示数为__________mm。
23.(10分)某同学到实验室做“测电源电动势和内阻”的实验时,发现实验台上有以下器
材:
待测电源(电动势约为4V,内阻约为2Ω)
一个阻值未知的电阻R0(阻值约为5Ω)
电压表(内阻很大,有5V、15V两个量程)两块
电流表(内阻约为1Ω,量程500mA)
滑动变阻器A(0~20Ω,3A)
滑动变阻器B(0~200Ω,0.2A)
开关一个,导线若干。
该同学想在完成学生实验“测电源电动势和内阻”的同时测出定值电阻儡的阻值,设计了如图所示的电路。
实验时他用U1、U2、I分别表示电表V1、V2、A的读数。
在将滑动变阻器的滑片移动到不同位置时,记录了U1,U2、I的一系列值。
然后他在两张坐标纸上各作了一个图线来处理实验数据,并计算了电源电动势、内阻以及定值电阻R0的阻值。
根据题中所给信息解答下列问题:
①在电压表V1接入电路时应选择的量程是___________,滑动变阻器应选择________。
(填器材代号“A”或“B”)
②在坐标纸上作图线时,用来计算电源电动势和内阻的图线的横坐标轴、纵坐标轴分别应该用_________、__________表示;
用来计算定值电阻R0的图线的横坐标轴、纵坐标轴分别应该用__________、___________表示。
(填“U1、U2、I”或由它们组成的算式)
③若实验中的所有操作和数据处理无错误,实验中测得的定值电阻R0的值_________
其真实值。
(选填“大于”、“小于”或“等于”)
24.(14分)如图所示,在E=1×
103N/C的竖直匀强电场中,有一光滑的半圆形绝缘轨道QPN竖直放置与一水平绝缘轨道MN相切连接,P为QN圆弧的中点,其半径R=40cm,一带负电电荷量q=10-4℃的小滑块质量m=20g,与水平轨道间的动摩擦因数μ=0.4,从位于N点右侧s=1.5m处以初速度v0向左运动,取g=10m/s2。
求:
(1)要使小滑块恰能运动到圆轨道的最高点Q,则滑块的初速度v0应多大?
(2)这样运动的滑块通过P点时对轨道的压力是多大?
25.(17分)如图,xoy平面内存在着沿y轴正方向的匀强电场,一个质量为m、带电荷量为+q的粒子从坐标原点O以速度v0沿x轴正方向开始运动。
当它经过图中虚线上的M(
a,a)点时,撤去电场,粒子继续运动一段时间后进入一个矩形匀强磁场区域(图中未画出),又从虚线上的某一位置N处沿与y轴负方向成60°
角做匀速直线运动。
已知磁场方向垂直xoy平面(纸面)向里,磁感应强度大小为B,不计粒子的重力。
试求:
(1)电场强度的大小:
(2)N点的坐标;
(3)矩形磁场的最小面积。
26.(14分)用下图装置可以进行测定SO2转化成SO3的转化率的实验。
已知SO3的熔点是16.8℃,沸点是44.8℃。
已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+H2SO4(80%)
Na2SO4+SO2↑+H2O
【注:
80%H2SO4具有浓硫酸的特性】
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。
请从下图A~D装置中选择最合适的装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是___________、_____________、_____________。
(2)在实验中“加热催化剂”与“滴加浓硫酸”的操作,首先应采取的操作是___________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法。
①原因__________________________________________________.
验证方法________________________________________________.
②原因__________________________________________________.
(4)将足量SO2通入含1.0mol次氯酸的溶液中,有1.204×
1024个电子转移,生成两种强酸,该反应的化学方程式为____________________________________________。
(5)用25.2gNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间将反应产生的SO2全部排出,测得装置Ⅲ增重了3.2g,则SO2的转化率为__________。
27.(14分)下图为一些物质间的相互转变关系,反应①在工业上可用来生产化合物C,反应⑤在工业上可生产化合物J(Na2FeO4),反应①、②、④和⑤均是在水溶液中进行的反应.常温下,D、E、G均是气体,B是无色液体;
F的水溶液可作为杀菌消毒剂;
H是一种铁矿石的主要成分,它由两种元素组成,且其中铁元素的质量分数为70%。
请回答下列问题:
(1)工业上利用反应①生产化合物C,得到化合物C的电极名称是______________。
(2)化合物F中阴离子的电子式为_______________。
(3)反应②的化学方程式为____________________。
(4)反应⑤的离子方程式为___________________________。
(5)高铁酸钠(Na2FeO4)既能杀菌消毒又是一种“绿色环保高效”的净水剂,其原因为:
①_______________________________________________________。
②_______________________________________________________。
28.(15分)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)目前工业上有一种方法是用CO2来生产燃料甲醇。
为探究该反应原理,进行如下实验:
某温度下,在容积为2L的密闭容器中,充入1molCO2和3.25molH2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如右图所示:
①从反应开始到平衡,氢气的平均反应速率v(H2)=__________________________.
②下列措施中一定不能使CO2的转化率增大的是________________。
A.在原容器中再充入1molCO2B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气D.使用更有效的催化剂
E.缩小容器的容积F.将水蒸气从体系中分离
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×
10-5mol/L。
若忽略水的电离及H2CO3的第二级电离,则H2CO3
+H+的电离平衡常数K=____________。
(已知:
10-5.6=2.5×
10-6)。
(3)标准状况下,将4.48LCO2通入200mL1.5mol/L的NaOH溶液,所得溶液中离子浓度由大到小的顺序为_____________。
(4)如图是甲醇燃料电池(电解质溶液为KOH溶液)的
结构示意图,则a处通入的是_________(填“甲醇”或
“氧气”),其电极上发生的电极反应式为_____________。
(5)已知,常温下Ksp(AgCl)=2.0×
10-10,Ksp(AgBr)=5.4×
10-13.向BaCl2溶液中加入AgNO3和KCl,当两种沉淀共存时,溶液中c(Br-)和c(Cl-)的比值为___________。
29.(10分)下图表示生长素在植物体内合成和分解的过程。
科学家研究发现,紫外光可通过促进吲哚乙酸氧化酶的活性,降低生长素含量,进而抑制植物生长。
请据题意完成下列实验:
实验材料和用具:
生长状况相同的健康的小麦幼苗若干,普通白炽灯、紫外光灯、完全培养液、器皿和检测仪器。
(1)实验步骤如下:
步骤l:
将小麦幼苗平均分为若干组,并标记为A、B、C、D…,分别培养在______中。
步骤2:
给予A组适宜的可见光照,作为对照;
给予其他各组_________光照,作为实验组。
步骤3:
相同适宜条件下培养适宜时间后,观察各组幼苗的_______________,并检测___________________的含量。
(2)该实验的目的是_____________________________________________________。
30.(8分)警戒色是指某些有恶臭或毒刺的动物所具有的鲜艳色彩和斑纹。
某地区有一种毒蛾,有黄黑相问的花纹.如果被鸟类吞食,其毒毛会刺伤鸟的口腔,这种花纹就是警戒色:
而该地区还有另一种与之花纹颜色十分相似的无毒蛾。
无毒蛾似有毒蛾的外观对其生存有什么影响呢?
某小组对此作出假设:
无毒蛾似有毒蛾的外观会排斥捕食者。
(1)根据这个假设,预期捕食者对此类无毒蛾的捕食频率_______(高于/低于)无黄黑桐间花纹的无毒蛾。
(2)实验小组在不同的地点放置数量相等的两种人工养殖的蛾,4周后回收了所有存活下来的蛾,并把数据整理如下表:
有黄黑花纹的无毒蛾
无黄黑相间花纹的无毒蛾
放置数目
100
回收数目
82
20
根据上表数据,能得出的结论是:
___________________________________________
(3)从进化的角度来看,无毒蛾形态的形成是长期自然选择使种群的_________定向改变的结果。
(4)如图为一食物网。
若要使丙体重增加x,其食用的动物性食物所占比例为a,至少需要的生产者量为y,那么x与y的关系可表示为____________。
A.y=90ax+10xB.y=25ax+5xC.y=20ax+5xD.y=10ax+10x
31.(13分)
Ⅰ、生物的变异中由于_____________________而导致的变异为可遗传的变异,它包括____________三种来源。
普通香蕉属三倍体,其繁殖后代的过程中,可能会产生_________种可遗传的变异。
Ⅱ、某种蝴蝶纯合亲本杂交后产生的F2代的性状如图(两性状均由常染色体基因控制):
(1)请问隐性性状是______________,F2中表现型与亲本不同的概率是_________________。
(2)如果用F2中的一只杂合紫翅绿眼与黄翅白眼的异性个体杂交,后代数量足够多的情况下,得到的子代的性状类型有____________种,数量比为______________________。
32.(8分)某科研小组做了如下实验:
从A、B两种植物上,各取多片彼此相似的叶片,在适宜温度下,分别测不同光照强度下A、B植物叶片放氧速率,数据如下表,请回答有关问题:
(1)由表中数据得知,在光照强度大于600MOL光子/m2.s时,影响光合作用的主要因素是_________________,若绘制A、B两植物叶片的放氧速率曲线图,两曲线有一交点,该交点的生物学意义是___________________________。
(2)如果在某光强下,叶片放氧速率为0,其生理学含义是_________________________.
如果用此光强照射大田作物,则作物很难存活,其原因是:
_________________________________。
(二)选考题(共45分。
请考生从给出的3道物理题、2道化学题、2道生物题中每学科任选一题做答.并用2B铅笔在答题卡上把所选题目的题号涂黑。
注意所做题目的慝号必须与所涂题目的题号一致,在答题卡选答区域指定位置答题。
如果多做,则每学科按所做的第一题计分。
)
33.[物理—选修3—3](15分)
(1)(5分)下列说法中正确的是
A.对物体做功不可能使物体的温度升高
B.即使气体的温度很高,仍有一些分子的运动速率是非常小的
C.一定量气体的内能等于其所有分子热运动动能和分子之间势能的总和
D.如果气体分子总数不变而气体湍度升高,气体分子的平均动能增大,因此压强必然增大
(2)(10分)如图所示,将一个绝热的开口汽缸竖直放置在水平桌面上,在汽缸内用一个绝热活塞封
闭了一定质量的气体。
在活塞上面放置一个物体,活塞和物体的总质量为10kg,活塞的横截面积为S=100cm2。
已知外界的大气压强为P0=1×
105Pa,不计活塞和汽缸之间的摩擦力。
在汽缸内部有一个电阻丝,电阻丝的电阻值R=4Ω,电源的电压为12V。
接通电源10s后活塞缓慢升高h=10cm(g取10m/s2)。
①求这一过程中气体的内能变化量。
②若缸内气体的初始温度为27℃,体积为3×
10-3m3,试求
接通电源10s后缸内气体的温度是多少?
34.[物理—选修3-4](15分)
(1)(5分)如下图1所示,一根水平张紧的弹性长绳上有等间距的O、P、Q质点,相邻两质点间距离为1.0m。
t=0时刻O质点从平衡位置开始沿y轴方向振动,并产生沿x轴正方向传播的波,O质点的振动图象如图2所示。
当O质点第一次达到正向最大位移时,P质点刚开始振动,则
A.质点Q的