依非韦伦精制工序Word文档下载推荐.docx
《依非韦伦精制工序Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《依非韦伦精制工序Word文档下载推荐.docx(84页珍藏版)》请在冰豆网上搜索。
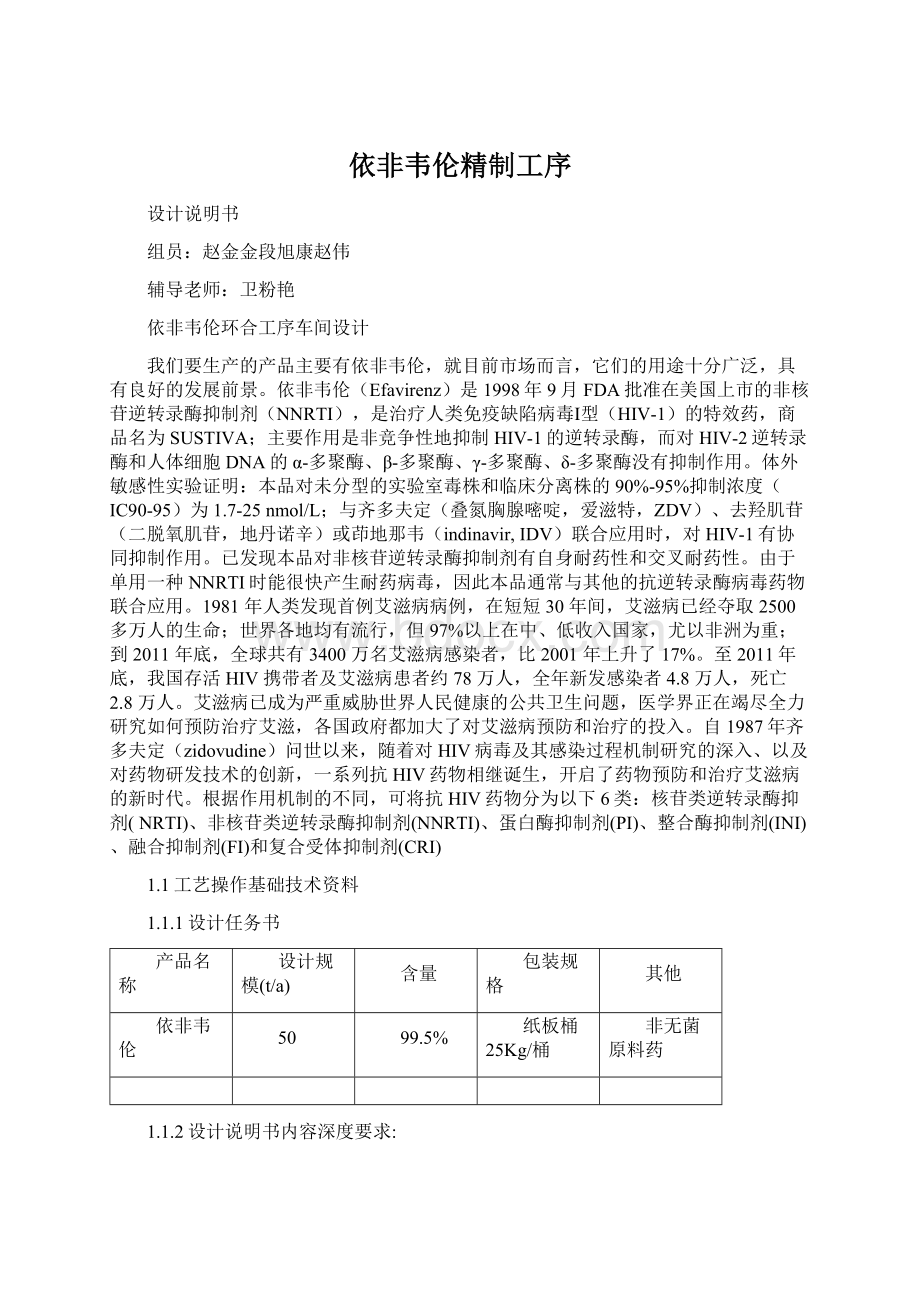
纸板桶25Kg/桶
非无菌原料药
1.1.2设计说明书内容深度要求:
(1)系统设备单元的配置是依非韦伦的生产,以合成单元操作为基础,充分考虑设备的的通用性及操作弹性。
(2)本工艺最终产品为非无菌原料药,该药品采用间歇生产,年生产工作日为260天,采用3班制,每班次工作8小时,每年共生产367批次产品。
(3)人流、物流分开设置,尽量减少或避免人流、物流之间的交叉和迂回。
(4)生产性质相似的车间尽可能集中布置,工艺流程相联系的车间靠近布置。
(5)原料药车间应布置在制剂车间的下风向,产尘和产生有害气体的车间应布置在主导风向的下风向。
1.1.3国家建设工程设计相关标准、规范
《中华人民共和国药典》(2010年)
《药品生产质量管理规范》GB/T50001-2001
《建筑设计防火规范》GBJ16-87
《工业企业卫生设计标准》TJ36-79
《石油化工企业设计防火规范》GB50160-2008
《压力管道规范工业管道》GBT20801-2006
《工业设备及管道绝热施工及验收规范》GBJ126-89
《职业性接触毒物危害程度分级》GB5044-85
《工业金属管道设计规范》GB50316-2000
《设备及管道保温设计导则》GB8175-87
《工业设备及管道绝热工程设计规范》GB50264-97
《化工设备管道外防腐设计规定》HG/T20679-1990
《爆炸和火灾危险环境电力装置设计规范》GB50058-92
《压力管道安全技术安全监察规程工业管道》TSG_D0001-2009
1.1.4设计中使用到的资料
表1-1
书名
作者
出版社
《化工单元过程及设备课程设计》第二版
匡国柱史启才
化学工业出版社
《化工设备设计全书——换热器》
秦叔经叶文邦等
《制药设备与工程设计》
朱宏基张明贤
《过程设计与造型基础》
陈志平曹志锡潘浓芬
浙江大学出版社
《化工原理》第二版
贾清贾绍义
天津大学出版社
《制药工程学》第二版
王志祥
《化工工艺制图》
周大军揭嘉
《化工计算》
葛婉华陈鸣德
《真空干燥》
徐成海张世伟关奎之
《化工基础》第三版
上海师范大学福建师范大学
高等教育出版社
1.1.5设计原则
(1)系统设备单元的配置以合成单元操作为基础,充分考虑设备管道的合理利用,采取可行的措施减少车间对环境的不利影响,并对排出的污染物提出合理的治理方案;
采取消除、预防或降低装置危险性、提高装置安全运行等级的安全卫生措施;
在满足功能和法规的前提下,尽可能降低项目投资。
(2)总平面布置的设计原则
中国医药工业公司制定的《药品生产管理规范》(1985年)第九条规定:
“厂房必须有整洁的环境,周围的空气,场地,水质应符合药品生产的要求,厂房内要减少露土面积。
”第十一条规定:
“厂房内主要道路要宽畅,做到人流,物流通道分开或固定走向,保证安全和整洁,路面要选择不易起尘的材料。
”卫生部制定的《药品生产质量管理规范》(1992年修订)第八条规定:
“药品生产企业必须有整洁的生产环境;
生产区的地面,路面及运输等不应对药品的生产造成污染;
生产,行政,生活和辅助区的总体布局应合理,不得相互妨碍。
”这些规定是我们进行药厂总平面布置应遵循的设计原则。
(3)厂房布置:
根据制药工厂组成和生产性质将厂区划分为生产区、辅助生产区、行政管理区和生活区,四个区域彼此联系,又互不影响,考虑联合布置,以节约土地、方便生产和管理;
充分考虑安全要素,严格遵守消防安全规范,特别是防止火灾和爆炸的发生。
产生或使用明火的车间应布置在主导风向的上风侧,而将可能散发可燃气体的储罐或设备布置在下风侧。
(4)管道设计:
在水平管道交叉较多的地区,一般按管道的走向,划定纵横走向的标高范围,将管道分层布置。
1.1.6设计中使用的基础数据(表1-2)
名称
分子量
密度
熔点
沸点
比热容
饱和蒸汽压
粘度
溶解性
备注
乙酸乙酯
88.11
0.9g/cm3
-83.6℃
77.2℃
1.92KJ/(Kg·
K)
10.1KPa20℃
0.449mPa·
S(20℃)
微溶于水,溶于乙醇、丙酮
临界压力3.83MPa临界温度250.1℃
活性炭
12.01
1.8g/cm3
3500℃
—
不溶于水
疏水性吸附剂
4-氯-2-(三氟乙酰基)苯胺
223.5
易溶于水
盐酸盐
丙酮
58.08
相对密度(水=1):
0.788
相对蒸气密度(空气=1):
2.00
-94.8℃
56.53℃
2.35
53.32KPa(39.5℃)
0.32mPa·
S(20℃)
与水混溶,混溶于乙醇、乙醚、氯仿、油类、烃类等多数有机溶剂
临界压力4.72MPa;
临界温度235.5℃
乙基锌
123.5
液体密度(15℃,100KPa):
1226Kg/m3
气体密度:
4.3Kg/m3
-30℃
117.6℃
(0℃):
0.479KPa
(10℃):
1KPa
(50℃:
7KPa
与水激烈反应
空气中能自燃,燃烧时产生氧化锌白烟
环丙基乙炔锂
72.041
与水互溶
氯甲酸甲酯
94.5
相对密度(水=1):
1.22
71.4℃
16.93KPa/20℃
不溶于水,溶于苯、甲醇、等多数有机溶剂
剧毒、易燃、有腐蚀性
碳酸钠
105.99
2.532g/cm3
851℃
1600℃
微溶于无水乙醇,不溶于丙醇
吸湿性很强
无水硫酸钠
142.06
2.68g/cm3
884℃
1404℃
298.15K,100
KPa
暴露于空气中易吸湿成为含水硫酸钠
纯化水
18
0.998g/cm3
0℃
100℃
4.18KJ/(Kg▪K)20s℃,定压
2.34KPa,20℃
1.005×
10-3
Pa·
S
水对各种物质都具有亲和性
临界温度(℃):
374.2,临界压力(KPa):
22.1
依非韦伦中间体OLi
295.54
依非韦伦中间体OH
285.68
溶于水
环丙基乙炔
66.1
0.7801
52-53℃
密封保存
315.68
有良好的耐受性
LiOH
23.94
1.46
450℃
925℃
溶于水,微溶于乙醇
无色、可溶性强碱
1.2生产能力和产品方案
依非韦伦产品总共在260天内依次生产,生产50t,依非韦伦以环丙基乙炔锂、4-氯-2(三氟乙酰基)苯胺为原料,经加成、环合、结晶等过程制得。
二、工艺说明
目前市场上依非韦伦的生产工艺多种多样。
依非韦伦合成方法分为两类:
化学拆分法和不对称合成法。
接下来,对两种方法涉及的文献和专利进行综述。
2.1文献中合成路线
(1)合成路线一:
以对氯苯胺为原料,得到具有光学纯的依非韦伦1,该路线总产率只有25%左右、ee%值为98%。
(2)合成路线二:
以对氯苯基异氰酸酯为原料,得到了消旋的依非韦伦5,最后经化学拆分法得到左旋的依非韦伦(图1.3)。
总得率约为16%,原子不经济,分离难度大。
(3)合成路线三:
以2-三氟乙酰基-4氯苯胺2为原料,该路线使工艺的立体选择性、产率都大大的提高(产率60%)。
但是在CAN的作用下会产生等量的对甲氧基苯甲醛(对最后产品的分离不利)和大量对环境有害的废物铈盐。
(4)合成路线四:
醌类化合物二氯二氰醌(DDQ)对中间体9进行环化,然后在碱性条件下与NaBH4反应开环,得到氨基醇12(图1.5)。
氨基醇12经光气关环得到依非韦伦(该步反应产率为94%)。
该合成方法是对硝酸铈盐法的改进,即可除去产生的对甲氧基苯甲醛,也可减少铈盐对环境的污染,但是DDQ氧化还原的产物DDQH也对环境有一定的污染。
在此基础上,Choudhury等人对脱保护的方法进行了改进:
使用醌类化合物四氯苯醌对中间体9进行环化,然后在碱性条件下与NH2OH或者TsNHNH2反应开环,得到氨基醇12,该步反应产率为82%(图1.6)。
(5)合成路线五:
2-三氟乙酰基-4氯苯胺2与N,N-四氢吡咯烷基-L-苯丙醇胺、格氏试剂和二乙基锌所形成的配合物反应,得到产率为87%、ee%值高达99.2%的12(图1.7)。
该反应用二乙基锌替代丁基锂,提高了反应的对映选择性,省去了保护和脱保护两步,进一步减少了对环境的污染,但是反应中用到的格氏试剂15、二乙基锌的价格昂贵,工业化生产成本高。
(6)合成路线六:
用了一种新的配体(1R,2R)-1-(4-硝基苯基)-2-(N,N-二甲基氨基-3-(叔丁基氧基)-1-丙醇,得到产率为80%、ee%值为99%的产品9。
该路线反应条件温和,产率高,但是该法使用的配体不是易得原料。
(7)合成路线七:
将2-三氟乙酰基-4氯苯胺2加入环丙基乙炔、中间体12、配体、二乙基锌的混合物中反应生成中间体12,产率为79%,ee%值高达99.6%。
该反应大大减少了二乙基锌、配体用量。
(8)合成路线八:
以2-三氟乙酰基-4氯苯胺盐酸盐16作为起始原料,经脱盐反应、氨基保护、不对称加成、脱氨基保护、环合等五步合成依非韦伦,总产率约为56%、纯度>
99.9%,ee%>
99.9%。
(9)合成路线九:
对氯苯胺为原料,经过水解反应即可以得到依非韦伦
(1)。
对氯苯胺和叔丁酞氯反应生成N一(4一氯苯基)一2,2一二甲基丙酞胺
(2),2先用正丁基铿处理后和三氟乙酸乙酷反应生成1一(2一胺基一5一氯苯基)一2,2,2一三氟乙酮(3)。
乙基澳化镁和环丙基乙炔反应得到环丙基乙炔基溟化镁,然后和3反应得到4一环丙基一2一(2一胺基一5一氯苯基)一1,1,1一三氟一3一丁炔一2一醇()4,4和拨基二咪哇反应生成1,4一二氢一4一环丙基乙炔基一4一三氟甲基一6一氯一ZH一3,1一苯并啥啧一2一酮(5),5被左旋茨酞氯酞化得到()6,然后用正己烷重结晶得到1,4一二氢一4一环丙基乙炔基一1一(15)一灰酞基一4一三氟甲基一6一氯一ZH一3,1一苯并啥嚓一2一酮()7,7水解即可以得到依非韦伦
(1)
(10)合成路线十:
对氯苯胺和碘反应得到4一氯一2一碘苯胺8(),8和叔丁酞氯反应得到N一4(一氯一2一碘苯基)一2,2一二甲基丙酞胺(9),9先和丁基铿作用得到苯基铿类化合物,然后和三氟乙
酸乙酷反应生成N一(1一(2一胺基一5一氯苯基)一2,2,2一三氟乙酮)一2,2一二甲基丙酞胺
(1)0,01先用盐酸水解,再用氨水调节pH为8后得到1一(2一胺基一5一氯苯基)一2,2,2一三氟乙酮(3),后面的步骤和路线一相同。
(11)合成路线十一:
对氯苯胺和叔丁酞氯反应生成N一(4一氯苯基)一2,2一二甲基丙酞胺
(1)1,2先用正
丁基铿处理后和三氟乙酸乙酷反应生成1一(2一胺基一5一氯苯基)一2,2,2一三氟乙酮的盐酸盐(12),21和光气反应得到1,4一二氢一4一三氟甲基一4,6一二氯一ZH一3,1一苯并啥嗦一2-酮(31),13和环丙基乙炔铿反应生成1,4一二氢一4一环丙基乙炔基一4一三氟甲基一6一氯一ZH一3,1一苯并啥嗦一2一酮(5)。
后面的步骤和路线一相同。
(12)合成路线十二:
2一胺基一5一氯苯甲酸和N,0一二甲基轻胺反应得到化合物N一甲氧基一2一胺基一5一氯苯酞甲胺(14),41和三苯基澳甲烷在二异丙胺的存在下反应得到N一甲氧基一2一三苯甲胺基一5一氯苯甲酞甲胺(15),51用ILAI场还原得到N一甲氧基一2一三苯甲胺基一5一氯苯甲醛
(1)6,61和三氟甲基三甲基硅烷在相转移催化剂四丁基氟化按的催化下反应得到2一胺基一5一氯-a一三氟甲基苯乙醇(17),71用氧化剂氧化后得到1一(2一三苯甲胺基一5一氯苯基)一2,2,2一三氟乙酮(18),18和环丙基乙炔铿反应得到4一环丙基一2一2(一三苯甲胺基一5一氯苯基)一1,1,1一三氟一3一丁炔一2一醇
(1)9,19和光气反应得到化合物1,4一二氢一4一环丙基乙炔基一4一三氟甲基一6一氯一ZH一3,1一苯并嚷嗦一2一酮()5,后面的步骤和路线一相同。
(13)合成路线十三:
3和对甲氧基节氯反应得到1一(2一(N一对甲氧基节胺基)一5一氯苯基)一2,2,
乙酮(20),20和环丙基乙炔铿在手性配体(IR,25)一1一苯基一2一(毗咯烷基)
的作用下,得到化合物。
)一环丙基一2一(2一(N一对甲氧基节胺基)一5一氯苯基)
2一三氟一1一丙醇1一三氟一3一丁炔一2一醇(12),21和光气反应得到。
)一1,4一二氢-丙基乙炔基一4一三氟甲基一6一氯一ZH一3,1一苯并嚷嗦一2一酮〔2)2,2伦
(1)。
N一对甲氧基节胺基一环水解后就可得到依非韦伦。
(14)合成路线十四:
三氟乙酸乙酷和环丙基乙炔基溟化镁反应得到环丙基乙炔基三氟甲基酮
(2)8,82和N一叔丁氧拨基一4一氯苯胺
(2)9在丁基铿的作用下反应得到4一环丙基一2一2(一N一叔丁氧拨
基胺基一5一氯苯基)一1,1,1一三氟一3一丁炔一2一醇3()0,30用丁基铿处理后环合得到()5,然后拆分即可得到
(1)。
(15)合成路线十五:
路线七在得到中间体化合物12以前的步骤和路线五一样,21被环合得到5一6一氯一4(一环丙基乙炔基)一1,4一HZ一4一三氟甲基一2一4(’一甲氧基苯甲基)3,1一苯哇嚓3
(1),13被还原得到5一4一环丙基一2一(2一三苯甲胺基一5一氯苯基)一1,1,卜三氟一3一丁炔一2一醇(3)2,32和光气环合得到1。
(16)合成路线十六:
这条路线是毛u」等人改进的不对称合成法,先由(I,RZ)S一毗咯烷基去甲基麻黄碱3()3和二甲基锌,甲醇反应得到中间产物(3)4,然后34和环丙基乙炔氯化镁反应得到金属络合物(35),53和1一2(一胺基一5一氯苯基)一2,2,2一三氟乙酮()3反应,选择性的得到(32),最后环合就可以获得1。
(17)合成路线十七:
以环丙基乙炔锂、4-氯-2(三氟乙酰基)苯胺为原料,经加成、环合、结晶等过程制得。
三氟乙酰基-4-氯苯胺经格式加成反应、环合反应、酰化反应、水解反应四个步骤得到依非韦,如下所示。
(18)合成路线十八:
2-三氟乙酰基-4-氯苯胺经格式加成反应、环合反应、酰化反应、水解反应四个步骤得到依非韦伦,如下所示。
1.对氯苯胺溶于氯仿和饱和碳酸钠水溶液,滴加2,2-二甲基丙酰氯。
加毕,在室温搅拌,过滤收集固体,滤液分层,分出的氯仿层用盐水洗,干燥,浓缩。
浓缩得到的物质和上述得到的固体一起用煮沸的乙酸乙酯己烷重结晶,得N-2,2-二甲基丙酰基对氯苯胺。
将该酰化物溶于四氢呋喃,滴加正丁基锂的己烷溶液,搅拌,再滴加三氟乙酸乙酯,加入盐酸和乙酸乙酯,分出有机层,用盐水洗涤,干燥,减压浓缩,得到的物质在盐酸中回流,冷却,加入乙酸乙酯,用浓氨水调至碱性。
分出有机层,用盐水洗涤,干燥,浓缩,得到2-三氟乙酰基-4-氯苯胺。
将环丙基乙炔溶于四氢呋喃,滴加乙基溴化镁的乙醚溶液进行反应,完毕后,加入2-三氟乙酰基-4-氯苯胺,再滴加饱和的氯化铵水溶液。
用乙酸乙酯萃取,萃取液合并后用盐水洗,干燥,浓缩,得烷化产物。
将其和羰基二咪唑溶于无水四氢呋喃。
然后减压蒸出溶剂,加入乙酸乙酯和水。
水层用乙酸乙酯萃取。
萃取液和有机层合并,用盐酸、饱和碳酸氢钠和盐水洗涤,经干燥、减压浓缩,得到消旋的依非韦仑。
将其和(-)樟脑酰氯在二氯甲烷反应,然后在正丁醇中,加入盐酸反应,拆分得光学活性的依非韦仑。
(19)合成路线十九
以对氯苯胺为起始原料酰化、取代等反应最终合成依非韦伦。
[4]
(20)合成路线二十
以2-胺基-5-氯苯甲酸为起始原料经酰化,亲核取代等反应最终合成依非韦伦。
(21)合成路线二十一
[5]
2.1.1本次设计使用方法
本次设计我们采用工艺路线以环丙基乙炔锂、4-氯-2(三氟乙酰基)苯胺为原料,经加成、环合、结晶等过程制得。
(一)主要化学反应方程式如下:
(1)加成反应
(2)环合反应
2.2工艺流程叙述
(1)加成工序
将52.455Kg乙基锌和52.455Kg丙酮在搅拌釜Ⅰ(R101)中进行搅拌混合(约0.5小时),控制温度30℃,制得混合溶液Ⅰ104.91Kg待用。
将45.465Kg环丙基乙炔锂和58.283Kg丙酮在搅拌釜(R102)Ⅱ中进行搅拌混合(约0.5小时),控制温度30℃,制得混合溶液Ⅱ103.75Kg待用。
将116.566Kg4-氯-2(三氟乙酰基)苯胺和116.566Kg丙酮在搅拌釜(R103)Ⅲ中进行搅拌混合(约0.5小时),控制温度30℃,制得混合溶液Ⅲ233.13Kg待用。
将233.13Kg丙酮、8.162Kg的A、55.949Kg的B加入加成反应釜(R104A)中,搅拌冷却至0℃(约1小时),将混合溶液Ⅰ缓慢加入加成反应釜中(约2小时)。
维持体系温度28℃以下,再将混合溶液Ⅱ缓慢加入加成反应釜中(约2小时),并维持体系温度在0~5℃,反应(约1.5小时)。
再将混合溶液Ⅲ缓慢加入加成反应釜中(约3小时),并维持体系温度40℃,反应(约2小时),得加成液739.03Kg(加成液比容约为950Kg/m³
)。
将此加成反应液转移至浓缩罐(R201)中进行减压浓缩,得455.83Kg馏出液并送厂外回收处理,罐中所剩浓缩液为280.15Kg,向罐中加349.70Kg乙酸乙酯,溶解此浓缩物,转移至淬灭釜(R202),并加入115.40Kg冰水,控制温度在0~5℃淬灭反应(约1小时)。
加入115.40Kg纯化水进行洗涤,洗涤液经连续分离器分离,得367.15Kg水相,其经预处理后排至污水处理站;
得有机相493.50Kg,经过滤器(M201)过滤,得482.67Kg滤液,滤液转移至浓缩罐(R203)进行减压浓缩,得到馏出液203.83Kg,浓缩液278.83Kg;
浓缩液转移至结晶罐(R204)却至10℃以下,得结晶物278.83Kg,在离心机(M202)中用11,66Kg的乙酸乙酯进行离心淋洗,得母液117.08Kg,滤饼173.41Kg(含湿量为20%);
滤饼转移至真空干燥器(E201),在真空度≥0.08MPa条件下燥,得加成物138.73Kg(加成物含量≥99%)。
回收离心母液和馏出液中的乙酸乙酯套用,回收率90%,残留物送市政处理。
加成收率为90%。
(2)环合工序
将加成物加入环合釜(R104B),再加入416.