高考化学大二轮复习 模拟试题精编十八Word格式.docx
《高考化学大二轮复习 模拟试题精编十八Word格式.docx》由会员分享,可在线阅读,更多相关《高考化学大二轮复习 模拟试题精编十八Word格式.docx(18页珍藏版)》请在冰豆网上搜索。
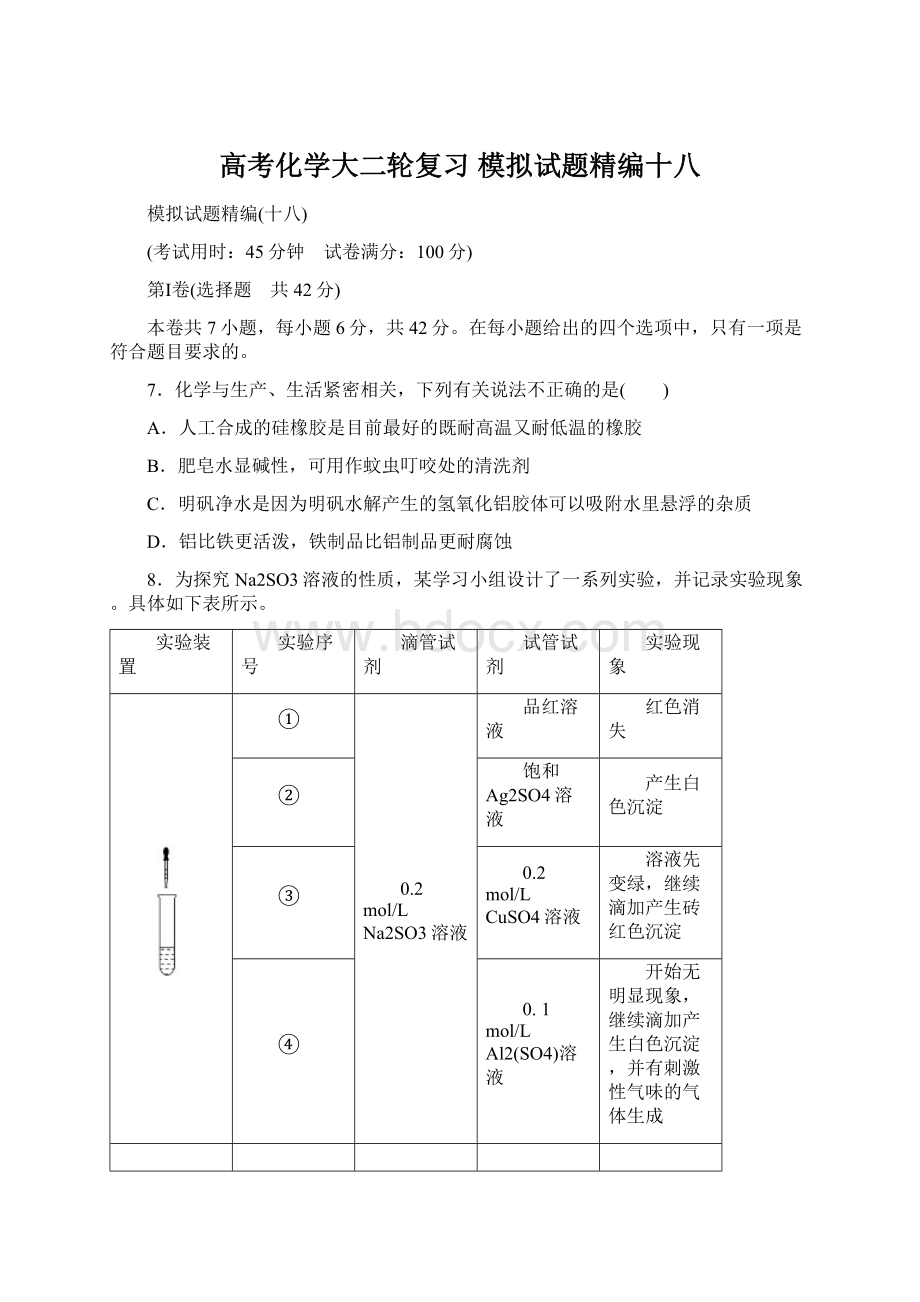
与Cu2+发生了氧化还原反应
D.实验④发生反应的离子方程式为3SO
+2Al3++3H2O===2Al(OH)3↓+3SO2↑
9.设NA为阿伏加徳罗常数值。
下列有关叙述正确的是( )
A.2molSO2与3molO2反应生成的SO3分子数为2NA
B.30g乙酸和葡萄糖混合物中的氢原子数为2NA
C.常温下pH=12的NaOH溶液中,水电离出的氢离子数为10-12NA
D.标准状况下,2.24LC2H6含有的共价键数为0.6NA
10.工业上可由乙苯(C8H10)生产苯乙烯(C8H8),其反应原理是:
下列说法中错误的是( )
A.可用溴的四氯化碳来鉴别乙苯和苯乙烯
B.乙苯分子中所有原子可能都处于同一平面
C.苯乙烯可发生氧化反应、取代反应、加成反应
D.乙苯与苯互为同系物
11.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层电子数是次外层的2倍,Y是非金属性最强的元素,在周期表中Z位于ⅡA,Y与W属于同一主族。
下说法正确的是( )
A.简单气态氢化物的热稳定性:
Y<
W
B.原子半径:
r(X)<
r(Y)<
r(Z)<
r(W)
C.Z和W的简单离子具有相同的电子层结构
D.化合物ZX2中既含有离子键,又含有共价键
12.钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池反应为2Na+xS===Na2Sx,电池结构如图所示。
下列说法不正确的是( )
A.放电时,Na作负极,反应式为Na-e-===Na+
B.钠硫电池在常温下也能正常工作
C.放电时Na+向正极移动
D.当外电路通过0.25mol电子时消耗16g硫,则x=4
13.常温下,在20mL0.1mol/LHR溶液中滴加0.1000mol/LNaOH溶液,混合溶液的pH与所加NaOH溶液体积的关系如图所示。
下列推断正确的是( )
A.①、②、③三点中,③对应的溶液中c水(H+)·
c水(OH-)最大
B.HR溶液中只存在H+、R-、OH-、H2O四种微粒
C.②点溶液中一定存在c(Na+)>
c(R-)>
c(H+)=c(OH-)
D.NaR的水解常数Ka和水解程度:
③>
②>
选择题答题栏
题号
7
8
9
10
11
12
13
答案
第Ⅱ卷(非选择题 共58分)
本卷包括必考题和选考题两部分。
第26~28题为必考题,每个试题考生都必须作答。
第35~36题为选考题,考生根据要求作答。
26.(14分)某化学兴趣小组设计实验探究Mg与盐溶液反应的多样性。
实验
向试管中加2mL溶液
实验Ⅰ:
0.1mol/LAgNO3溶液
镁条表面迅速覆盖一层疏松黑色固体,并有少量气泡产生
实验Ⅱ:
2.0mol/LNH4Cl溶液
反应开始时产生大量气体(经检验其中含有H2),一段时间后产生使湿润的红色石蕊试纸变蓝的气体
实验Ⅲ:
pH=8.2NaHCO3溶液
产生大量气体(经检验其中含有H2和CO2)和白色固体
请回答下列问题:
(1)对实验Ⅰ进行研究:
①推测实验Ⅰ中黑色固体为Ag,则发生反应的离子方程式为_______________________________________________________________。
②确认黑色固体为Ag的实验方案是_______________________________。
(2)对实验Ⅱ进行研究:
①反应开始时产生H2的原因可能是Mg和NH
直接反应,或________。
②“一段时间后”产生的气体一定含有H2和________。
③为进一步研究,设计如下实验:
操作
现象
实验Ⅳ
向装有相同镁条的试管中加入2mL1.0mol/L(NH4)2SO4溶液
产生气体的速率明显慢于实验Ⅱ
结合实验Ⅱ、Ⅳ,可以得出的结论是________。
(3)对实验Ⅲ进行研究:
①经检验,白色固体为碱式碳酸镁。
②推测在pH=8.2的该溶液中,若无HCO
,则H+和Mg反应的程度很小。
通过实验证实了该推测,其实验操作是_____________________________。
(4)根据上述实验判断,影响Mg与盐溶液反应多样性的原因有________(填字母序号)。
A.盐溶液中阳离子的氧化性B.盐溶液的温度
C.含Mg生成物的溶解性D.盐溶液中阴离子的影响
27.(15分)合理利用或转化NO2、SO2、CO、NO等污染性气体是人们共同关注的课题。
Ⅰ.某化学课外小组查阅资料后得知:
2NO(g)+O2(g)
2NO2(g)的反应历程分两步:
①2NO(g)
N2O2(g)(快) v1正=k1正·
c2(NO),v1逆=k1逆·
c(N2O2) ΔH1<
②N2O2(g)+O2(g)
2NO2(g)(慢) v2正=k2正·
c(N2O2)·
c(O2),v2逆=k2逆·
c2(NO2) ΔH2<
(1)反应2NO(g)+O2(g)
2NO2(g)的ΔH=________(用含ΔH1和ΔH2的式子表示)。
一定温度下,反应2NO(g)+O2(g)
2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示平衡常数的表达式K=________。
(2)决定2NO(g)+O2(g)
2NO2(g)反应速率是反应②,反应①的活化能E1与反应②的活化能E2的大小关系为E1________E2(填“>
”“<
”或“=”)。
Ⅱ.(3)反应N2O4(g)
2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强有如下关系:
v(N2O4)=k1·
p(N2O4),v(NO2)=k2·
p2(NO2)。
其中k1、k2是与温度有关的常数。
一定温度下,相应的速率与压强关系如图所示,在图中标出的点中,能表示该反应达到平衡状态的两个点是____________,理由是_________________________________________________________________。
(4)在25℃时,将amol·
L-1的氨水溶液与0.02mol·
L-1HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示25℃时NH3·
H2O的电离常数Kb=________。
用质量分数为17%,密度为0.93g/cm3的氨水,配制200mLamol·
L-1的氨水溶液,所需原氨水的体积V=________mL。
(5)如图电解装置可将雾霾中的NO、SO2分别转化为NH
和SO
。
物质A的化学式为________,阴极的电极反应式是__________________________。
28.(14分)高锰酸钾是常用的氧化剂。
工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。
中间产物为锰酸钾。
下图是实验室模拟制备KMnO4晶体的操作流程:
已知:
锰酸钾(K2MnO4)是墨绿色晶体,其水溶液呈深绿色,这是锰酸根离子(MnO
)在水溶液中的特征颜色,在强碱性溶液中能稳定存在;
在酸性、中性和弱碱性环境下,MnO
会发生自身氧化还原反应,生成MnO
和MnO2。
回答下列问题:
(1)KOH的电子式为________,煅烧KOH和软锰矿的混合物应放在________中加热(填标号)。
A.烧杯 B.瓷坩埚 C.蒸发皿 D.铁坩埚
(2)调节溶液pH过程中,所得氧化产物与还原产物的物质的量之比为________。
(3)趁热过滤的目的是________。
(4)已知20℃时K2SO4、KCl、CH3COOK的溶解度分别为11.1g、34g、217g,则从理论上分析,选用下列酸中________(填标号),得到的高锰酸钾晶体纯度更高。
A.稀硫酸B.浓盐酸C.醋酸D.稀盐酸
(5)产品中KMnO4的定量分析:
①配制浓度为0.1250mg·
mL-1的KMnO4标准溶液100mL。
②将上述溶液稀释为浓度分别为2.5、5.0、7.5、10.0、12.5、15.0(单位:
mg·
L-1)的溶液,分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如右。
③称取KMnO4样品(不含K2MnO4)0.1250g按步骤①配得产品溶液1000mL,取10mL稀释至100mL,然后按步骤②的方法进行测定,两次测定所得的吸光度分别为0.149、0.151,则样品中KMnO4的质量分数为________。
(6)酸性KMnO4溶液与FeSO4溶液反应的离子方程式为__________________________________________________________________。
请考生在第35、36两道化学题中任选一题作答。
如果多做,则按所做的第一题计分。
35.(15分)
【化学——选修3:
物质结构与性质】
氮的化合物在农药生产及工业制造业等领域用途非常广泛,请根据提示回答下列相关问题:
(1)基态氮原子的价层电子排布式为________,碳、氮、氧元素的第一电离能由小到大的顺序为________________(用元素符号表示)。
(2)NH4Cl中氮原子的杂化方式为________,与NH
互为等电子体的一种非极性分子的化学式为________________。
(3)NH4Cl受热易分解产生氨气,向CuSO4溶液中通入氨气至过量,产生蓝色沉淀,随后沉淀溶解得到深蓝色溶液,该溶液中存在的配离子的结构式为________。
(4)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°
和93.6°
,试分析PH3的键角小于NH3的原因_____________________________。
(5)第ⅤA族气态氢化物沸点如图所示,试解释沸点PH3<
NH3,PH3<
AsH3<
SbH3的原因____________________________________________
_____________________________________________________________。
(6)氮化镓是具有重要应用价值的半导体,其部分晶体结构如图所示,每个晶胞中Ga原子个数为________个,若晶胞底边长为anm,高为cnm,则氮化镓的晶体密度为________g/cm3(用含a、c的代数式表示,阿伏加德罗常数用NA表示)。
36.(15分)
【化学——选修5:
有机化学基础】
合成药物X、Y和高聚物Z,可以用烃A为主要原料,采用以下路线。
Ⅰ.反应①、反应②的原子利用率均为100%。
Ⅱ.
(R或R′可以是烃基或H原子)。
(1)A的结构简式为________。
(2)Z中的官能团名称为________,反应③的条件为________。
(3)关于药物Y(
)的说法正确的是________。
A.1mol药物Y与足量的钠反应可以生成33.6L氢气
B.药物Y的分子式为C8H8O4,能使酸性高锰酸钾溶液褪色
C.药物Y中⑥、⑦、⑧三处-OH的活泼性由强到弱的顺序是⑧>
⑥>
⑦
D.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗分别为4mol和2mol
(4)写出反应E→F的化学方程式_________________________________。
F→X的化学方程式__________________________________________。
(5)写出符合下列条件的E的一种同分异构体的结构简式________。
①遇FeCl3溶液可以发生显色反应,且是苯的二元取代物;
②能发生银镜反应和水解反应;
③核磁共振氢谱有6个峰。
(6)参考上述流程以CH3CHO和CH3OH为起始原料,其它无机试剂任选设计合成Z的线路。
____________________________________________________________。
高考化学模拟试题精编(十八)
7.解析:
选D。
A.硅橡胶具有空间网状结构,具有耐磨、耐高温、耐低温等性能,故A正确;
B.肥皂水显碱性,与蚊虫叮咬处释放的酸发生中和反应,故B正确;
C.明矾溶解于水水解产生的氢氧化铝胶体可以吸附水里悬浮的杂质,则明矾可作净水剂,故C正确;
D.金属铝更耐腐蚀是由于其化学性质活泼,在常温下就可以和氧气反应而形成致密的氧化铝薄膜,从而阻止进一步氧化,而铁锈是疏松多孔的结构,会加速铁的锈蚀,故D错误。
8.解析:
选B。
A.Na2SO3溶液能使品红溶液褪色,说明Na2SO3溶液具有漂白性,故A正确;
B.在饱和Ag2SO4溶液中滴加Na2SO3溶液有白色沉淀生成,说明Ksp(Ag2SO4)>
Ksp(Ag2SO3),故B错误;
C.CuSO4溶液中滴加Na2SO3溶液,溶液先变绿,继续滴加产生砖红色沉淀,说明生成Cu2O沉淀,则SO
与Cu2+发生了氧化还原反应,故C正确;
D.Al2(SO4)溶液中滴加Na2SO3溶液,产生白色沉淀,并有刺激性气味的气体生成,说明溶液中存在相互促进水解反应,发生反应的离子方程式为3SO
+2Al3++3H2O===2Al(OH)3↓+3SO2↑,故D正确。
9.解析:
A.SO2和氧气反应生成SO3是可逆反应,SO3的物质的量小于2mol,故A错误;
B.乙酸(C2H4O2)和葡萄糖(C6H12O6)最简式相同,即为CH2O,因此30g此混合物中氢原子的物质的量为30×
2/30mol=2mol,故B正确;
C.没有说明溶液的体积,无法计算物质的量,故C错误;
D.2.24L的乙烷中含有共价键的物质的量为0.7mol,故D错误。
10.解析:
A.乙苯不含有碳碳双键,不能使溴的四氯化碳褪色,苯乙烯中含有碳碳双键,能使溴的四氯化碳褪色,因此可以鉴别,故A说法正确;
B.乙苯—CH3和—CH2—中碳原子是sp3杂化,因此所有原子不共面,故B说法错误;
C.苯乙烯中含有碳碳双键,能发生氧化反应和加成反应,苯乙烯中含有苯环,能与液溴等发生取代反应,故C说法正确;
D.苯和乙苯结构相似,且组成上相差2个“CH2”,因此两者互为同系物,故D说法正确。
11.解析:
A、短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层电子数是次外层的2倍,X为C元素,Y是非金属性最强的元素,Y为F元素,在周期表中Z位于ⅡA,Z为Mg元素,Y与W属于同一主族,W为Cl元素。
A.简单气态氢化物的热稳定性:
HCl<
HF,故A错误;
B.原子半径:
r(X)>
r(Y),r(Z)>
r(W),故B错误;
C.Mg2+有2个电子层,W的简单离子Cl-有三个电子层,故C错误;
D.MgC2中Mg2+与C
之间是离子键,C
内碳与碳之间形成共价键,故D正确。
12.解析:
A.放电时,负极反应式为Na-e-===Na+,故A正确;
B.钠硫电池以熔融金属钠、熔融硫作为电极的,则常温下不能正常工作,故B错误;
C.原电池放电时Na+向正极移动,故C正确;
D.正极反应式为xS+2e-===S
,当外电路通过0.25mol电子时消耗16g硫,硫的物质的量为0.5mol,则x∶2=0.5∶0.25,解得x=4,故D正确。
13.解析:
选A。
A.根据图像可知点①HR被中和一半,此时得到的溶液是等浓度的NaR和HR的混合物,②点所示的溶液显示中性,此时得到的是NaR和剩余的少量的HR的混合物,点③恰好反应,得到的是NaR溶液,此时溶液显碱性,说明是强碱弱酸盐,R-水解,因此③对应的溶液中c水(H+)·
c水(OH-)最大,A正确;
B.HR是弱酸,溶液中只存在H+、R-、OH-、H2O、HR五种微粒,B错误;
C.②点显中性,溶液中一定存在c(Na+)===c(R-)>
c(H+)===c(OH-),C错误;
A.水解常数只与温度有关系,D错误。
26.解析:
(1)①出现黑色固体,此固体为Ag,利用金属活动顺序表,发生置换反应,即Mg+2Ag+===Mg2++2Ag;
②确认是Ag,需要检验Ag+,即将Ag转化成Ag+,具体操作是:
将黑色固体过滤、洗涤,向其中加入稀HNO3,黑色固体溶解并产生无色气体,遇空气后变成红棕色,并向所得溶液中滴加NaCl溶液,生成白色沉淀,说明黑色固体为Ag;
(2)①NH4Cl是强酸弱碱盐,NH
发生水解反应,NH
+H2ONH3·
H2O+H+,Mg+2H+===Mg2++H2↑,消耗H+促使平衡向正反应方向进行;
②根据实验Ⅱ,除得到氢气外,还有一种能使湿润红色石蕊试纸变蓝的气体,此气体为NH3;
③加入的是(NH4)2SO4,NH
的浓度与NH4Cl中NH
浓度相同,不同的是阴离子,因此得出结论是Cl-有利于Mg和铵盐溶液反应产生H2(或SO
不利于Mg和铵盐溶液反应产生H2、溶液中阴离子的种类会影响Mg和铵盐溶液反应产生H2);
(3)②HCO
在水中既有电离也有水解,HCO
H++CO
,pH=8.2说明溶液显碱性,得到Mg2(OH)2CO3,当没有HCO
,则H+和Mg2+反应的程度很小,实验设计为:
向装有相同镁条的试管中加入2mLpH=8.2的NaOH溶液,观察反应现象;
(4)A.根据实验Ⅰ,利用Ag+的氧化性较强,得到黑色固体,故A正确;
B.四个实验中没有说明温度对实验的影响,故B错误;
C.根据实验Ⅲ,得到碱式碳酸镁,碱式碳酸镁不溶于水,故C正确;
D.实验Ⅱ和Ⅳ的对比,说明阴离子的影响,故D正确。
答案:
(1)①2Ag++Mg===2Ag+Mg2+ ②将黑色固体过滤、洗涤,向其中加入稀HNO3,黑色固体溶解并产生无色气体,遇空气后变成红棕色,并向所得溶液中滴加NaCl溶液,生成白色沉淀
(2)①NH
水解使溶液中c(H+)增大,与Mg反应生成H2 ②NH3
③Cl-有利于Mg和铵盐溶液反应产生H2(或SO
不利于Mg和铵盐溶液反应产生H2、溶液中阴离子的种类会影响Mg和铵盐溶液反应产生H2)
(3)向装有相同镁条的试管中加入2mLpH=8.2的NaOH溶液 (4)ACD
27.解析:
Ⅰ.
(1)①2NO(g)
N2O2(g);
②N2O2(g)+O2(g)
2NO2(g),而目标反应2NO(g)+O2(g)
2NO2(g)的ΔH=①+②=ΔH1+ΔH2,由反应达平衡状态,所以v1正=v1逆、v2正=v2逆,所以v1正×
v2正=v1逆×
v2逆,即k1正c2(NO)×
k2正c(N2O2)·
c(O2)=k1逆c(N2O2)×
k2逆c2(NO2),则K=
=
;
(2)因为决定2NO(g)+O2(g)2NO2(g)速率的是反应②,所以反应①的活化能E1远小于反应②的活化能E2;
Ⅱ.(3)满足平衡条件v(NO2)=2v(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1∶2,所以B、D为平衡点;
(4)反应后溶液中c(NH
)=c(Cl-)=0.01mol/L,则c(H+)=c(OH-)=10-7mol·
L-1,溶液呈中性,故Kb=
=(2×
10-9)/(a-0.02);
设氨水的体积为VmL,则根据稀释定律可知:
V×
0.93g·
cm-3×
17%=amol·
L-1×
0.2L,解得V=21.5amL。
(5)NO得电子生成铵根,离子方程式为NO+5e-+6H+===NH
+H2O,为阴极反应,阳极上SO2失电子形成硫酸。
Ⅰ.
(1)ΔH1+ΔH2 k1k2/k2k1
(2)<
Ⅱ.(3)BD 图中只有D点的NO2的消耗速率是B点N2O4的消耗速率的2倍,所以表示达到化学平衡状态的点是BD (4)2×
10-9/(a-0.02) 21.5a或200a/9.3或2000a/93 (5)H2SO4 NO+6H++5e-===NH
+H2O
28.解析:
(1)KOH属于离子化合物,其电子式为
,因为是煅烧,烧杯和蒸发皿都不耐高温,瓷坩埚成分含SiO2,SiO2在高温下与KOH反应,因此不能用瓷坩埚,因此选D;
(2)根据信息,锰酸钾在酸性、中性、弱碱性环境中发生歧化反应,MnO2是锰酸钾中Mn由+6价→+4价,化合价降低得到,因此MnO2是还原产物,KMnO4是氧化产物,n(KMnO4)×
1=n(MnO2)×
2,得出n(KMnO4)∶n(MnO2)=2∶1;
(3)高锰酸钾易溶于水,MnO2不溶于水,因此趁热过滤目的是:
防止析出高锰酸钾,降低产率;
(4)高锰酸钾与浓盐酸反应,然后根据三种物质的溶解度大小,溶解度越大,得到高锰酸钾纯度越高,故选C;
(5)③吸光度的平均值为(0.149+0.151)/2=0.150,此时对应的KMnO4的浓度为11.25mg·
L-1,则1000mL的溶液中KMnO4的浓度为11.25×
1000/100mg·
L-1=112.5mg·
L-1,因此高锰酸钾的质量分数为112.5/(0.1250×
103)×
100%=90.0%;
(6)利用高锰酸钾的氧化性,把Fe2+氧化成Fe3+,本身被还原成Mn2+,然后根据化合价的升降法进行配平,即离子反应方程式为MnO
+5Fe2++8H+===Mn2++5Fe3++4H2O。
(1)
(2)2∶1 (3)防止析出高锰酸钾,降低产率 (4)C (5)90.0% (6)MnO
+5Fe2++8H+===Mn2++5Fe3++4H2O
35.解析:
(1)氮元素的核电荷数为7,其原子最外层有5个电子,则基态氮原子的价层电子排布式为2s22p3,碳、氮、氧元素均为第二周期主族元素,第一电离呈增大趋势,但氮的2p轨道为半充满结构,相对稳定,第一电离偏大,则三种元素的第一电离能由小到大的顺序为C<
O<
N;
(2)NH
离子中价层电子对=4+
=4,所以中心原子原子轨道为sp3杂化,其VSEPR模型为正四面体,该离子中不含有孤电子对,所以其空间构型为正四面体,NH
中电子数为7+4-1=10,原子数为5,CH4中电子数为6+4=10,原子数为5,CH4和NH
互为等电子体;
(3)向CuSO4的水溶液中逐滴加入氨水,离子方程式为Cu2+