沪教版数学三上《年月日》练习题Word文件下载.docx
《沪教版数学三上《年月日》练习题Word文件下载.docx》由会员分享,可在线阅读,更多相关《沪教版数学三上《年月日》练习题Word文件下载.docx(12页珍藏版)》请在冰豆网上搜索。
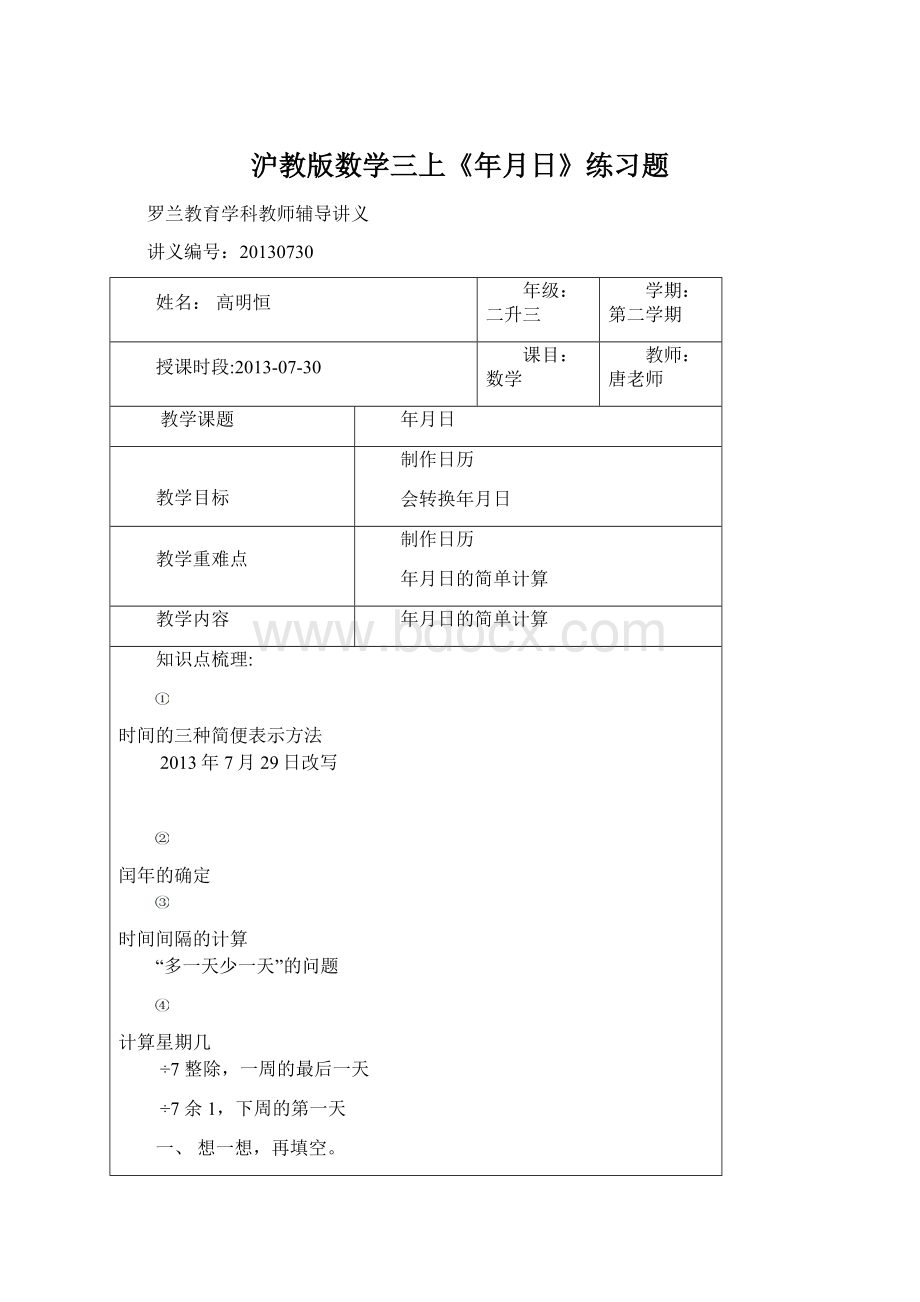
7余1,下周的第一天
一、想一想,再填空。
1.巴蜀学校创建于1933年10月,到今年10月是她(
)岁的生日。
2.九月份最多有(
)个星期一,最少有(
)星期一
3.一年有()个月,31天的月份有(),30天的月份有(),平年的二月有()天,闰年的二月有()天。
4.2004年的二月份有()天,全年共有()天,是()年。
5.刘波是1986年7月12日出生的,到2005年生日时,他满()周岁。
6.小青的生日在第三季度里的小月,而且是这个月的倒数第八天,小青的生日是( )月( )日:
小平的生日比小青的生日早10天,小平的生日是()月()日。
7.2005年1月1日是星期六,2005年1月31日是星期()
8.闰年全年有( )天,是( )个星期零( )天。
9.8月1日的前一天是( )月( )日,6月30日的后一天是( )月( )日。
10.1年=9( )个月 48时=( )日
5星期=( )天 半年=( )个月
49天=( )星期18个月=( )年( )个月
11.小华的生日是第二季度最后一个月,日子数比月份多7,小华的生日是()
12.中国共产党是1921年7月1日成立的,到今年7月1日是()周年。
二判断.(正确的打“√”,错误的打“×
”)
1.每年都是365天。
( )
2.东东出生于1994年2月29日。
()
3.一年中有7个大月,5个小月。
( )
4.2004年的一月、二月、三月共有91天。
( )。
5.2004年8月1日是星期日,8月31日是星期二。
( )
6.
小明出生于1999年2月29日。
------------------------------------(
)
7.每年都有365天。
---------------------------------------------------------()
8.凡单月都是大月,凡双月都是小月。
---------------------------------()
9.小华说:
“我爸爸去年2月29日去了一趟北京,今年2月29日又去了一趟北京。
”--------------------------------------------------------------------------()
三解决问题。
1.华明商场平均每天卖8台电视,今年第四季度能买多少台电视?
2.、某车间2000年2月每天生产零件9个,照这样计算,2000年2月全月一共生产多少个零件?
3、爷爷过生日那天对孙子说:
“我只过了十八个生日。
”你知道这是为什么吗?
4、春子明天将去北京旅游。
她把旅游7天的日历撕下来放在挎包里。
发现这7天日期的和刚好是140,今天应该是几日?
(7天旅游天数包括出发和回家的天数)
5、某年的9月1号是星期五,这一年的10月1日是星期几?
6、李星叔叔是1972年3月3日出生的,到今年3月3日,他是几岁?
课后记
作业:
练习年月日的计算
闰年的判断
家长签字:
选择题
1、短周期元素R的原子核外电子数等于核内中子数,该元素单质7.8g与氧气充分反应可生成13g化合物RO,则该元素的价电子层是:
A、1S2B、2S2C、3S2D4S2
2、下列关于稀有气体的叙述不正确的是:
A、原子的电子排布最外层都是以P6结束;
B、其原子与同周期ⅠA、ⅡA族阳离子具有相同电子排布式;
C、化学性质非常不活泼;
D、原子半径比同周期ⅦA族元素原子的大
3、居里夫人发现的镭是元素周期表的第七周期的ⅡA族,下列关于镭的性质的描述中不正确的是:
A、在化合物中呈+2价B、氢氧化物呈两性
C、单质使水分解,放出氢气D、碳酸盐难溶于水
4、在下列所示的微粒中,氧化性最强的是:
A、1S22S22P2B、1S22S22P5C、1S22S22P63S1D、1S22S22P6
5、元素电负性随原子序数的递增而增强的是:
A、Na,K,RbB、N,P,AsC、O,S,ClD、Si,P,Cl
6、根据对角线规则,下列物质的性质具有相似性的是:
A、硼和硅B、铝和铁C、铍和铝D、铜和金
7、按电子排布,可把周期表里的元素划分成5个区,以下元素属于P区的是:
A、FeB、MgC、PD、La
8.以下能级符号不正确的是()
A.3sB.3pC.3dD.3f
9.下列各原子或离子的电子排列式错误的是()
A.Na+1s22s22p6B.F¯
1s22s22p6
C.N3+1s22s22p6D.O2¯
1s22s22p6
10.以下各分子中,所有原子都满足最外层为8电子结构的是()
A.H3O+B.BF3C.CCl4D.pCl5
11.下列关于氢原子电子云图的说法正确的是()
A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大。
B.黑点密度大,单位体积内电子出现的机会大。
C.通常用小黑点来表示电子绕核作高速圆周运动。
D.电子云图是对运动无规律性的描述。
12.下列轨道表示式能表示氮原子的最低能量状态的是()
↑↓
↑
A.1S2S2P
B.1S2S2P
C.1S2S2P
D.1S2S2P
13.x、y为两种元素的原子,x的阴离子与y的阳离子具有相同的电子层结构,由此可知()
A.x的原子半径大于y的原子半径。
B.x的电负性小于y的电负性。
C.x的氧化性大于y的氧化性。
D.x的第一电离能大于y的第一电离能。
14.氢原子的电子云图中的小黑点表示的意义是()
A一个小黑点表示一个电子B黑点的多少表示电子个数的多少
C表示电子运动的轨迹D电子在核外空间出现机会的多少
15、电子构型为[Ar]3d54s2的元素是()
A.稀有气体B.过渡元素C.主族元素D.卤族元素
16、下列能级轨道数为3的是:
A、s能级B、p能级C、d能级D、f能级
17、对Na、Mg、Al的有关性质的叙述正确的是:
A、碱性:
NaOH<
Mg(OH)2<
Al(OH)3B、第一电离能:
Na<
Mg<
Al
C、电负性:
Na>
Mg>
AlD、还原性:
18、X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是:
A、X2YZ3B、X2YZ2C、XYZ2D、XYZ3
19、下列关于能层与能级的说法中正确的是:
A、原子核外电子的每一个能层最多可容纳的电子数为2n2
B、任一能层的能级总是从s能级开始,而且能级数等于该能层序数
C、同是s能级,在不同的能层中所能容纳的最多电子数是不相同的
D、1个原子轨道里最多只能容纳2个电子,但自旋方向相同。
20、
C-NMR(核磁共振)可以用于含碳化合物的结构分析。
C表示的碳原子()
A核外有13个电子,其中最外层有4个电子
B核内有6个质子,核外有7个电子
C质量数为13,原子序数为6,核内有7个质子
D质量数为13,原子序数为6,核内有7个中子
21、基态铬原子的电子排布式是()
A、1S22S22p63S23p64S14p5B、1S22S22p63S23p63d6C、1S22S22p63S23p64S23d4D、1S22S22p63S23d54S1
22、下列元素中基态原子的第一电离能最大的是()
A、BB、CC、ND、O
23、下列原子中第一电离能最大的是(C)
A、NaB、LiC、BeD、Mg
24、基态碳原子的电子排布式为()
A、1S22S22px2B、1S22S22py2C、1S22S22pz2D、1S22S22px12py1
25、下列各组元素按电离能增加顺序排列的是()
(A)Li、Na、K(B)B、Be、LiC)O、F、Ne(D)C、P、Se
26、4p轨道填充一半的元素,其原子序数是()
A、15B、33C、35D、51
27、各周期包含的元素为()
A、2、8、18、32、72、98B、2、8、8、18、18、32
C、2、8、8、18、32、32D、2、8、18、32、32、72
28、某元素价电子构型3dS4S2,是该元素是()
A、FeB、CoC、MnD、Ni
29、某元素质量数51,中子数28,其基态原子未成对电子数为()
A、0B、1C、2D、3
30、某原子第六电子层只有二个电子,其第五电子层电子数为()
A、8B、18C、8~18D、8~32
31、下列原子各电子层中电子数不合理的是()
21Sc:
K
(2)L(8)M(8)N(3)24Cr:
K
(2)L(8)M(13)N
(1)
32Ge:
K
(2)L(8)M(18)N(4)29Cu:
K
(2)L(8)M(18)N
(1)
32、某元素原子价电子构型3d54S2,其应在()
第四周期ⅡA族第四周期ⅡB族第四周期ⅦA族第四周期ⅦB族
33、某元素电子构型为[Xe]4f46S2,其应在()
A、S区B、p区C、d区D、f区
34、3d轨道中最多容纳电子数为()
A、2B、10C、14D、18
35、第三能层含有的轨道数为()
A、3B、5C、7D、9
一、填空
37、某元素最高化合价为+5,原子最外层电子数为2,半径是同族中最小的,其核外电子排布式为,价电子构型为,属区元素。
38、3d轨道半充满和全充满的元素分别为和。
39、铜原子核外电子排布式为,属于第周期,是族。
40、第四周期第六个元素的电子构型是。
41、某元素原子的所电子构型为4S24p1,它属于第周期,族,最高正化合价为,元素符号是。
42、某元素原子的价电子构型为3S23p3,它属于第周期,是族,最高正化合价为,元素名称是。
43、某元素原子的价电子构型为3S2,它是区元素,元素符号为。
44、某元素原子的价电子构型为3d104S2,它属于第周期,是族,区元素,元素符号是。
45、某元素原子的价电子构型为3d54S1,它属于第四周期,d区元素,最高正化合价为,元素符号是。
46、按原子序数从锂到氟,第一电离能由小到大的次序是。
47、电负性最大的元素是,最小的是。
48、原子序数为24的元素原子中有个电子层,个能级,个价电子,个未成对电子。
49、按构造原理写出35号元素的基态原子的电子排布式:
---------------;
其价电子层为—————————,其所在主族的价电子层为:
————;
,最高化合价为:
————————,最低化合价为:
———
50.A、B、C三种短周期元素,原子序数依次增大,三种元素数依次之和为35,A、C同族,B+离子核外有10个电子,回答下列问题
①.A、B、C三种元素分别是_________、_________、_________。
②.A、B、C之间形成多种化合物,其中属于离子化合物的化学式分别为_________、__________、___________。
③分别写出A、B、C的电子排列式:
A._______________________________________
B._______________________________________
C._______________________________________
51、1932年美国化学家鲍林首先提出了电负性的概念。
电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
元素
H
Li
Be
B
C
N
O
F
电负性
2.1
1.0
1.5
2.0
2.5
3.0
3.5
4.0
Na
Mg
Si
P
S
Cl
K
0.9
1.2
1.7
2.3
0.8
请仔细分析,回答下列有关问题:
①预测周期表中电负性最大的元素应为____________;
估计钙元素的电负性的取值范围:
___________<X<___________。
②根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是_______________________________________________________________________________;
简述元素电负性X的大小与元素金属性、非金属性之间的关系_____________
____________________________________________________________________________。
③经验规律告诉我们:
当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;
当小于1.7时,一般为共价键。
试推断AlBr3中形成的化学键的类型为______________,其理由是__________________________
_______________________________________________________________________________
_______________________________________________________________________________。
※现代原子结构理论认为,在同一电子层上,可有s、p、d、f、g、h……等亚层,各亚层分别有1、3、5、……个轨道。
试根据电子填入轨道的顺序预测:
(1)第8周期共有种元素;
(2)原子核外出现第一个6f电子的元素的原子序数是;
(3)根据“稳定岛”假说,第114号元素是一种稳定同位素,半衰期很长,可能在自然界都可以找到。
试推测第114号元素属于周期,族元素,原子的外围电子构型是
参考答案
题号
1
2
3
4
5
6
7
8
9
答案
D
10
11
12
13
14
15
16
17
18
A
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
37、某元素最高氧化数为+5,原
37、某元素最高氧化数为+5,原子最外层电子数为2,半径是同族中最小的,其核外电子排布式为1S22S22p63S23p63d34S2,价电子构型为3d34S2,属d区元素。
38、3d轨道半充满和全充满的元素分别为Cr、Mn和Cu、Zn。
39、铜原子核外电子排布式为1S22S22p63S23p63d104S1,属于第四周期,是ⅠB族。
40、第四周期第六个元素的电子构型是1S22S22p63S23p63d54S1。
41、它属于第四周期,ⅢA族,最高氧化数为+3,元素符号是Ga。
42、它属于第三周期,是ⅤA族,最高正化合价为+5,元素名称是磷。
43、它是S区元素,元素符号为Na。
44、它属于第四周期,是ⅡB族,ds区元素,元素符号是Zn。
45、它属于第四周期,d区元素,最高氧化数为+6,元素符号是Cr。
46、第一电离能由小到大的次序是Li、B、Be、C、O、N、F。
47、电负性最大的元素是F,最小的是Cs。
48、原子序数为24的元素原子中有4个电子层,7个能级,6个价电子,6个未成对电子。
49、略50.
①ONaS
②Na2O2Na2ONa2S
③0:
1s22s22p4
Na:
1s22s22p63s1
S:
1s22s22p61s23s23p
51.
①.F0.8<X<1.2
②.同主族从上向下,电负性减小;
电负性越大,非金属性越强,金属性越弱,反之亦然
③共价键因为AlCl3中Cl与Al的电负性差值为1.5,小于1.7,则AlCl3的键为共价键。
而Br的电负性小于Cl,所以AlBr3中两元素的电负性差值也小于1.7,即AlBr3的键为共价键。
※
(1)50
(2)139(3)七ⅣA7s27p2