胡波化学竞赛题库配位异构平衡滴定Word文件下载.docx
《胡波化学竞赛题库配位异构平衡滴定Word文件下载.docx》由会员分享,可在线阅读,更多相关《胡波化学竞赛题库配位异构平衡滴定Word文件下载.docx(7页珍藏版)》请在冰豆网上搜索。
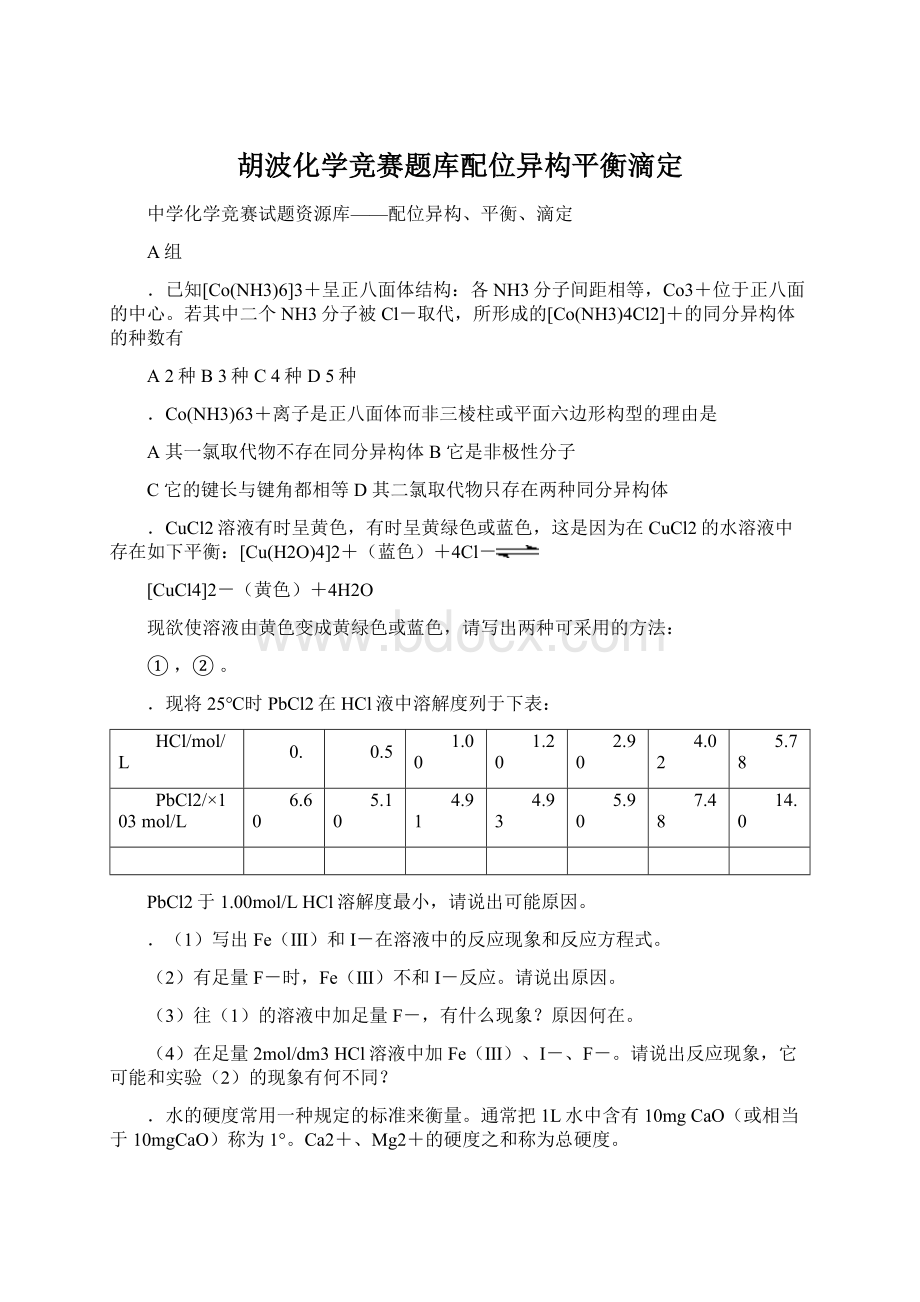
2.90
4.02
5.78
PbCl2/×
103mol/L
6.60
5.10
4.91
4.93
5.90
7.48
14.0
PbCl2于1.00mol/LHCl溶解度最小,请说出可能原因。
.
(1)写出Fe(Ⅲ)和I-在溶液中的反应现象和反应方程式。
(2)有足量F-时,Fe(Ⅲ)不和I-反应。
请说出原因。
(3)往
(1)的溶液中加足量F-,有什么现象?
原因何在。
(4)在足量2mol/dm3HCl溶液中加Fe(Ⅲ)、I-、F-。
请说出反应现象,它可能和实验
(2)的现象有何不同?
.水的硬度常用一种规定的标准来衡量。
通常把1L水中含有10mgCaO(或相当于10mgCaO)称为1°
。
Ca2+、Mg2+的硬度之和称为总硬度。
用配位滴定法分析某水样的硬度时,取50.00mL水样放入250mL锥形瓶中,加入稀盐酸数滴,煮沸,冷却,加入2mL1︰1的三乙醇胺溶液和10mLNH3·
H2O-NH4Cl缓冲溶液(pH=10),及3滴酸性铬蓝K-素酚绿B混合指示剂。
用0.01000mol/LEDTA溶液滴定至由红色到蓝色即终点,消耗EDTA溶液12.5mL。
另取水样50.00mL,将上述操作中加入缓冲溶液改为加入20%的,NaOH溶液使pH>12,用0.01000mol/LEDTA溶液滴定至终点,消耗EDTA溶液7.50mL。
已知Ca2+与EDTA以物质的量1︰1发生络合反应。
(1)试计算水样的总硬度、钙硬度;
(2)为什么要加入数滴稀盐酸并煮沸?
(3)为什么要加入三乙醇胺溶液?
(4)为什么要加入NH3·
H2O-NH3Cl缓冲溶液?
B组
.[Pt(NH3)2Cl2]分子有两种同分异构体,其中一种是治癌药物,它能与乙二胺(en)反应生成[Pt(NH3)2en]。
写出该[Pt(NH3)2Cl2]的结构式。
.若配体的分子组成为C4H7OH它和金属离子M(电荷省略)形成配合物,问可有多少种配合物异构体存在?
.如图所示,[Co(en)3]3+螯合离子是正八面体构型的,六个配位点被三个双齿配体乙二胺(en)所占据,请问该离子是否存三重轴(该离子绕轴旋转120º
与原离子图形完全重合);
与已知三重轴垂直的二重轴(绕轴旋转180º
后与原图形完全重合)有几条。
.已知配离子[Co(en)3]3+存在两种旋光异构体,说明由此能够证明它不是六方形或三棱形结构,又能否由此证明它为八面体结构。
.已知:
配位化合物和[Co(NH3)4Cl2]有两种异构体。
试判断其空间体构型是八面体型还是三棱柱型?
.今有化学式为Co(NH3)4BrCO3的配合物。
(1)画出全部异构体的立体结构。
(2)指出区分它们的实验方法。
.下列结构中哪些是①几何异构体②光学异构体③完全相同的结构
①②③④
⑤⑥⑦⑧
.电子构型相同的Ni2+、Pd2+和Pt2+均能形成配合物。
Pd(Ⅱ)、Pt(Ⅱ)配合物为平面四方形构型,而多数Ni(Ⅱ)配合物为四面体构型,只有少数是平面四方形构型,为什么?
何种Ni(Ⅱ)配合物最可能是平面四方形构型?
.A、B、C为三种不同的配合物,它们的化学式都是CrCl3·
6H2O,但颜色不同:
A呈亮绿色,跟AgNO3溶液反应,有2/3的氯元素沉淀析出;
B呈暗绿色,能沉淀1/3的氯;
而C呈紫色,可沉淀出全部氯元素。
则它们的结构简式分别为:
A,B,C。
这三种配离子的空间构型为面体,其中配离子一中的2个Cl可能有两种排列方式称为顺式和反式。
它们的结构图分别为:
_______和。
.瑞士苏黎士大学的维尔纳(Werner)对配位化学有重大贡献,因此曾荣获第13届诺贝尔化学奖。
他在化学键理论发展之前,提出了利用配合物的几何异构体来确定配合物的空间构型。
现有[Cr(H2O)4Br2]Br和[Co(NH3)3(NO2)3]两种配合物,其内界分别表示为MA4B2和MA3B3,其中M代表中心离子,A、B分别代表不同的单齿配位体。
为了获得稳定的配合物,中心离子周围的配位体相互之间的距离尽可能远,形成规则的平面或立体的几何构型。
(1)MA4B2和MA3B3可能存在哪几种几何构型(用构型名称表示)?
(2)每种几何构型中,分别存在多少种异构体?
(3)实际上,MA4B2和MA3B3巨型配合物(或配离子)都只存在两种几何异构体。
根据上面分析,判断它们分别是什么几何构型?
试写出它们各自的几何异构体。
.亚硝酸根NO2-作为配位体有两种配位方式:
其一是氮原子提供孤对电子与中心原子配位,另一是氧原子提供孤对电子与中心原子配位。
前者称为硝基(合),后者称为亚硝酸根(合)。
试画出这两种配位方式的结构式(可用M表示中心原子)。
[Co(NH3)5(NO2)]Cl2有两种存在形式;
[Co(NH3)5H2O]Cl3和NaNO2反应得一种红棕色粉末A,这种红棕色粉末在热盐酸溶液中会转变成棕黄色晶体B,B比A更稳定。
试命名这两种化合物。
.NaCl电离出的Cl-会对AgCl的溶解产生同离子效应,但随着Cl-离子浓度增大,Ag+与Cl-生成配合物将使AgCI在NaCl溶液中的溶解度增大。
(1)计算AgCl在0.0010mol/L和0.10mol/LNaCl溶液中的溶解度;
(2)计算AgCl在NaCl溶液中的最小溶解度,由此说明Cl-对AgCl溶解度的影响(忽略离子强度的影响)。
已知Ksp(AgCl)=1.8×
10-10,Ag+-Cl-配合物的lgβ1=3.04,lgβ2=5.04,lgβ3=5.04,lgβ4=5.30。
.欲使0.0010molAgCl沉淀完全溶于100mL氨水中。
问:
(1)溶解平衡时,游离氨浓度为多少?
(mol/L)
(2)溶解AgCl沉淀,需此氨水的总浓度为多少(mol/L)?
(3)已知浓氨水密度为0.9g/mL,其含量为28%,则浓氨水的浓度为多少(mol/L)
(4)应取浓氨水多少毫升可配成上述氨水100mL?
(已知AgCl的Ksp=1.8×
10-10,Ag(NH3)2+的lgK稳=7.0)
C组
.已知配合物[Pt(NH3)(OH)2Cl3]是八面体结构,请求出它的几何异构体数目。
.配合物A是1986年Jenesn合成的,它的化学式为Ni[P(C2H5)3]Br3。
化合物呈顺磁性,有极性,但难溶于水而易溶于苯,其苯溶液不导电。
试写出配合物A所有可能的立体结构。
若有对映体必须标明对应关系。
.二甲基亚硫酰Me2SO是两可配体。
(1)确定其结构。
即可通过S或O原子进行键合,确定哪一个原子与M结合,可以根据络合物S-O键红外伸缩振动频率vS-O=1/2π(k/μ)1/2(μ折合质量μS-O=ms·
mo/(ms+mo)(k为键力常数)与自由的Me2SO的vS-O对比,来确认配合物中是以S或O原子配位。
(2)试加以说明。
.金属离子与酸H2L形成一种配合物ML,该配合物的形成常数为K1。
M+L
ML,K1=[ML]/{[M]·
[L]},溶液中还含有另一种金属离子N,它与酸H2L生成配合物NHL。
配合物ML的条件形成常数K1’有下列关系:
K1”=[ML]/{[M’]·
[L’]},其中[M’]为未结合成ML的含M型体的总浓度,[L’]为未结合成ML的含L型体的总浓度。
推导出用[H+]和有关K值表示的K1’的关系式。
K值中除ML的形成常数外,还知道H2L的酸常数Ka1和Ka2以及配合物NHL的形成常数KNHL。
N+L+H+
NHL,KHNL=[NHL]/{[N]·
[H+]·
[L]},还可假定平衡浓度[H+]和[N]为已知值。
以上为简单起见,略去了除H+以外各型体的电荷。
.在315K下,将某中性单齿配体X加到NiBr2的CS2溶液中,反应产物是红色抗磁性配合物A,化学式为NiBr2X2。
冷至室温,A转变成化学式相同的绿色配合物B,测得B的磁矩为3.20B.M.。
若将B溶解在氯仿中,得到一带微红色的绿色溶液,测得配合物B在氯仿中的磁矩为2.69B.M.,右图为配合物A和B的吸收光谱。
(1)画出A和B可能存在的所有几何异构体。
(2)指出谱图中曲线Ⅰ和Ⅱ分别属于哪个配合物,说明原因。
(3)谱图中哪些吸收峰与A和B的颜色对应?
(4)说明异构体B在氯仿中的颜色和磁矩变化的原因。
(5)如果选用波长为510nm的单色光照射A,A呈什么颜色?
.金属金常常可以在铝硅酸盐岩石中发现,它很细地分散在其他矿物之中。
通过暴露在空气中的氰化钠溶液处理破碎后的矿石来提取,在这个过程中金慢慢地转变成可溶于水的Au[(CN)2]-(反应1)。
达到平衡后,被泵出的水相用锌与金的配合物反应转化为金属金,而锌则转变成Zn[(CN)4]2-(反应2)
(1)写出反应(l)和
(2)的配平的离子方程式。
金在自然界中经常和银形成合金,银也可以被暴露在空气中的氰化钠溶液氢化。
(2)500L0.0100mol/L的Au[(CN)2]-和0.0030mol/L的Ag[(CN)2]-的溶液经蒸发掉三分之一体积的液体后用锌处理(40g)。
假设偏离标准条件是不重要的,而且所有的氧化还原反应都进行到底了,试计算在反应停止后Au[(CN)2]-和Ag[(CN)2]-的浓度。
已知:
Zn[(CN)4]2-+2e→Zn+4CN-Eo=-1.26V
Au[(CN)2]-+e→Au+2CN-Eo=-0.60V
Ag[(CN)2]-+e→Ag+2CN-Eo=0.31V
(3)Au[(CN)2]-在一定条件下是很稳定的络合物。
欲使99%的金在溶液中以该氰配合物的形式存在,问需要多大浓度的氰化钠?
Au[(CN)2]-:
Kf=4×
1028
(4)已经发展了另一些提取金的方法来代替氰化法,为什么?
选择一个答案
A氰化钠溶液腐蚀采矿机械
B氰化钠流失在地下水中会生成氢化氰,后者对许多动物是有毒的
C用氰化法得到的金是不纯的
.由银(74%)、铅(25%)、锑(1%)等制成的合金是一种优良的电镀新材料。
对其中的银的分析,可采用络合滴定法,具体分析步骤概括如下:
试样
沉淀(A)
溶液(B)
溶液(C)
溶液(D)
其中(Ⅰ)加入HNO3(1︰1),煮沸,再加入盐酸(1︰9),煮沸,过滤,依次用盐酸(1︰9)和水洗涤沉淀;
(Ⅱ)加入浓氨水,过滤,用5%氨水洗涤沉淀;
(Ⅲ)加入氨水-氯化铵缓冲溶液(pH=10),再加入一定量的镍氰化钾固体;
(Ⅳ)加入紫脲酸铵指示剂(简记为In),用乙二胺四乙酸二钠(简写为Na2H2Y)标准溶液滴定至近终点时,加入氨水10mL(为了使其终点明显),继续滴定至溶液颜色由黄色变为紫红色为终点。
已知有关数据如下:
配合物
[AgY]3-、[NiY]2-、[Ag(CN)2]-、[Ni(CN)4]-、[Ag(NH3)2]+、[Ni(NH3)6]2+
LgK稳
7.3218.6221.131.37.058.74
酸
H4YH3Y-H2Y2-HY3-
lgK稳
-2.0-2.67-6.16-10.26
(1)写出A和D中Ag存在形体的化学式。
(2)写出第Ⅲ步骤的主反应的化学方程式和第Ⅳ步骤滴定终点时反应的化学方程式。
(3)试样加HNO3溶解后,为什么要煮沸?
加入盐酸(1︰9)后为什么还要煮沸?
(4)假定溶液C中Ag(Ⅰ)的总浓度为0.010mol/L,游离NH3浓度为2mol/L,要求滴定误差控制在0.2%以内,试计算溶液C中Ni(Ⅱ)总浓度至少为多少?
.在pH=10.0的氨性缓冲溶液中,以铬黑T(EBT)为指示剂,以2.0×
10-2mol/LEDTA滴定浓度为2.0×
10-2mol/L的Ca2+,问终点误差为多少?
若在相同条件下滴定的是2.0×
10-2mol/L的Mg2+,其终点误差又为多少?
K(CaY)比K(MgY)大,为什么滴定Ca2+比滴定Mg2+的终点误差反而要大?
若以MgY和EBT作为间接金属指示剂,问应加入MgY的浓度是多少?
已知lgK(CaY)=10.7,lgK(MgY)=8.7;
pH=10.0时,lgαY(H)=0.45;
EBT的pKα1=6.3,pKα2=11.6,lgK(Ca-EBT)=5.4,lg(Mg一EBT)=7.0。
.
(1)有[Pt(NH3)2(OH)2]化合物,存在两种几何异构体A和B,它们与等物质的量的草酸根发生取代反应,分别生成C和D化合物,并且产生OH-离子,用相同浓度的H+离子中和OH-离子,前者消耗的酸的体积是后者的两倍,试写出A、B、C、D的结构式。
试以[PtCl4]2-为原料,加入必要的试剂合成B化合物,说明以什么原则指导合成?
(2)[PtBrCl(PR3)2](PR3为三烷基磷)也存在两种几何异构体A和B,它们具有不同的31P-NMR(核磁共振)光谱(如右图),其中异构体A显示单一的31P线,异构体B显示两条线。
试判断A、B分别为何种异构体(用结构式表示)?
说明判断理由。
(3)四配位的平面四方形配合物[IrCl(PMe3)3](Me代表CH3)属于多少电子构型的配合物?
它能与Cl2发生何种类型的化学反应(取代反应、插入反应、还原消去、氧化加成等类型)?
形成分子式为[IrCl3(PMe3)3]两种产物,该分子又是多少电子构型?
[IrCl3(PMe3)3]两种产物的31P-NMR光谱表明一个异构体中的P原子只有一种化学环境,而另一种异构体中的P原子有两种化学环境,试画出[IrCl3(PMe3)3]的几何异构体,并解释它们的31P-NMR光谱行为。
参考答案