验证方案模板Word文档格式.docx
《验证方案模板Word文档格式.docx》由会员分享,可在线阅读,更多相关《验证方案模板Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
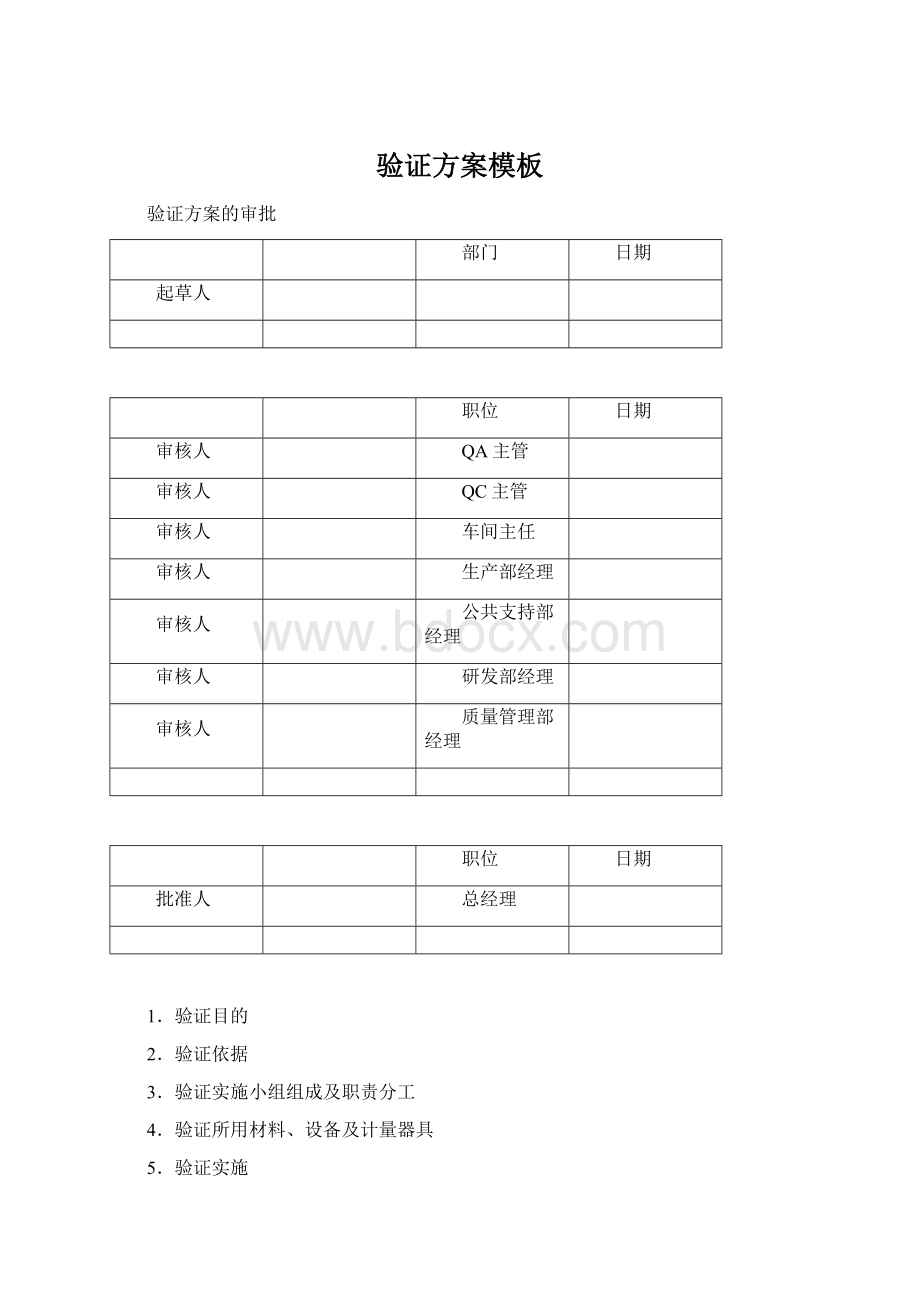
5.验证实施
6.偏差处理
7.验证结论
8.验证评价
附图1工艺流程框图
附录1工艺过程简述
附录2相关SOP
附录3批生产记录
附录4批检验记录
附录5环境监测记录
附表1SOP培训记录
附表2本验证方案培训记录
本方案的目标是经过生产工艺验证,证明按照头孢匹胺钠生产工艺能够稳定生产出合格的无菌头孢匹胺钠。
2.验证依据
本验证方案主要依据头孢匹胺钠工艺规程,头孢匹胺钠SOP。
3.1验证小组成员
人员
冻干车间
生产部
质量管理部
公共支持部
研发部
验证小组组长:
晋超
3.2职责分工
3.2.1结晶车间负责起草本验证报告。
3.2.2结晶车间,生产部,质量管理部负责本验证的实施,公共支持部,研发部配合实施,质量管理部负责审核本验证。
3.3培训
验证参加人员已进行本验证方案的培训(见附表1):
是□否□
检查人:
年月日
审核人:
生产操作人员已进行与验证相关SOP培训(见附表2):
4.1关键原材料的质量情况
原料质量情况:
年月日
序号
物料名称
标准编号
备注
1
2
3
4
评价:
4.2主要设备
设备名称
型号或规格
编号
溶解罐Ⅰ
D1200H3300
HA—SC—304
溶解罐Ⅱ
D1000H3300
HA—SC—317
溶解罐Ⅲ
HA—SC—328
结晶罐
D1700H3820
HA—SC—357
5
三合一
D1200H4500
HA—SC—359
6
VTD-东
GDXZG-151490*1170*1690
HA—SC—364
7
VTD-西
HA—SC—363
8
混粉器
V-10
HA—SC—217
4.3关键仪器仪表
工序名称
检测项目
配备计量器具
名称
数量
地点
溶解
重量
电子秤
溶配岗位
温度
温度探头
结晶
流速
流量计
无菌过滤线
时间
钟表
结晶岗位
分装
中间体重量
自动电子秤
分装岗位
4.4公用系统
项目
设计要求
-15℃水系统
≤-15℃
蒸汽
压力
≥0.4MPa
7℃水系统
4℃-7℃
氮气系统
≥0.45Mpa
5.1验证的时间进度:
5.2验证的具体实施
5.2.1工艺流程框图,见附图1。
5.2.2验证步骤
生产后由质量部对其进行取样、检验。
(详见附录1)
5.2.2.4关键工艺控制点
控制围
实测值
CFPS0908113
CFPS0908114
CFPS0908115
18℃~22℃
4.5kg±
0.25kg
25kg~30kg
7.2
1.5
1170L~1620L
0.09kg~0.45kg
3.6kg~10.8kg
干燥
39℃~41℃
39℃~51℃
18h
<6.7%
20min~50min
5.2.2.5成品检验结果应符合我公司质量标准。
5.2.3有关记录
详见附录3-5。
5.2.4收率计算
钠收率应为90.0%~113%
计算公式为:
收率=产量(kg)/投料量(kg)×
100%
批号
投料量(kg)
产量(kg)
收率(%)
5.2.5成品质量情况
5.2.5.1
成品批号:
样品名称
检测项
验证检验结果
标准
实测结果
结论
水分
5.3相关SOP,见附录2。
5.4批生产记录,见附录3。
5.5批检验记录,见附录4。
56环境监测记录,见附录5。
6.偏差处理
7.验证结论
验证结论
验证小组负责人签名/日期:
验证小组成员
会签
使用部门意见
负责人签名/日期:
意见
8.验证评价
附图1工艺流程框图
十万级区
附录2SOP一览表
SOP名称
附录3批生产记录
附表1
相关SOP培训记录
主持单位
培训日期
培训课时
培训地点
讲课人
应参加培训人数
培训容
受培训人
签名
缺席人补课记录
补课日期
应培训人数
车间负责人:
附表2
验证方案培训记录