步步高人教必修1第一章 第二节 第1课时Word下载.docx
《步步高人教必修1第一章 第二节 第1课时Word下载.docx》由会员分享,可在线阅读,更多相关《步步高人教必修1第一章 第二节 第1课时Word下载.docx(16页珍藏版)》请在冰豆网上搜索。
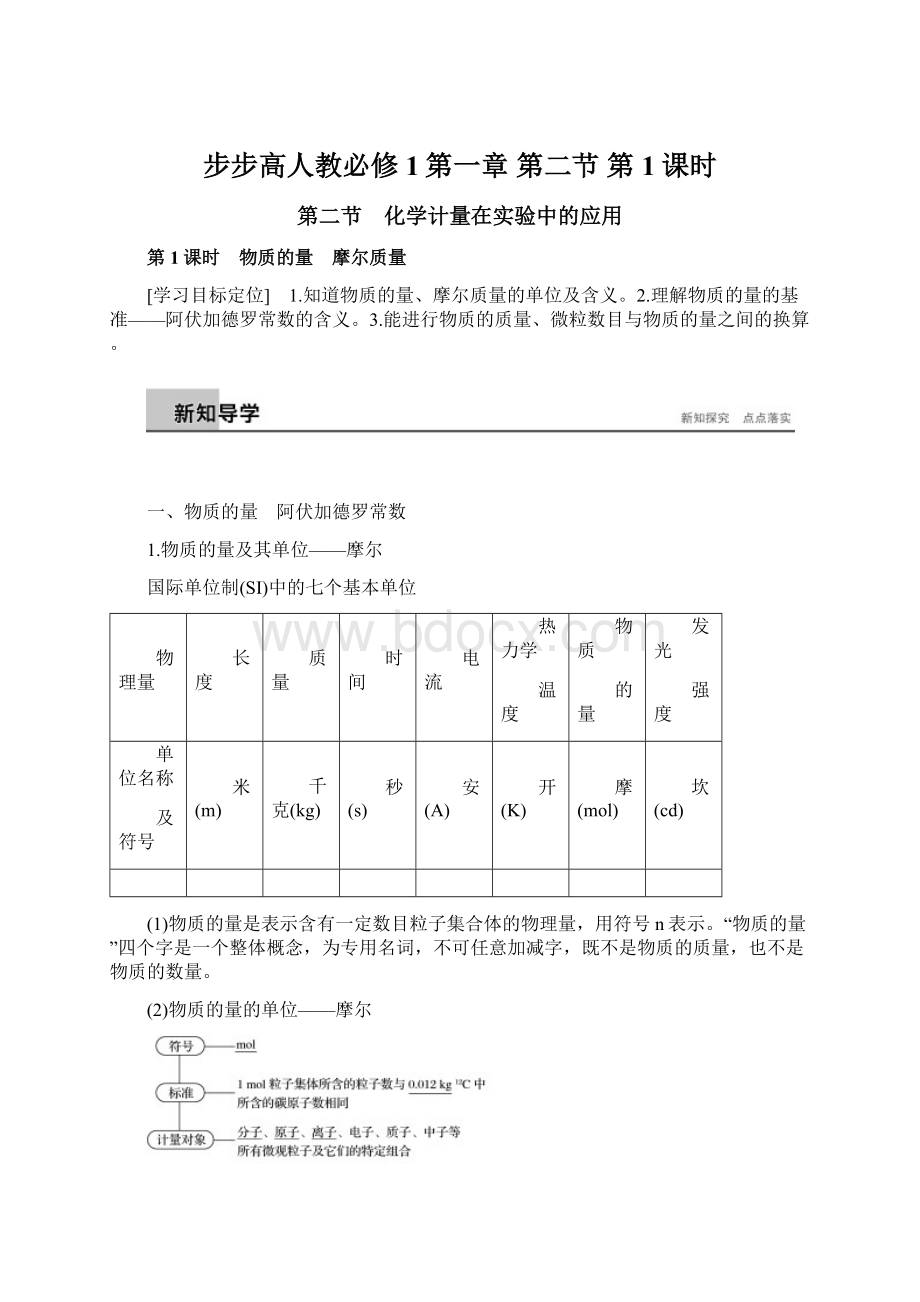
32g
5.315×
通过上表计算结果,得出的结论是12g12C所含的原子个数约为6.02×
1023(阿伏加德罗常数);
物质含有6.02×
1023个微粒的物质的量为1摩尔。
(1)阿伏加德罗常数是0.012kg12C所含的原子个数,约为6.02×
1023个,用符号NA表示。
(2)物质若含有阿伏加德罗常数(6.02×
1023)个微粒,其物质的量为1mol。
(3)阿伏加德罗常数可表示为NA,约为6.02×
1023mol-1,其单位是mol-1。
(4)物质的量、阿伏加德罗常数与粒子数之间的关系:
n=N/NA。
1.判断正误,正确的打“√”,错误的打“×
”。
(1)物质的量可以理解为物质的数量( )
(2)摩尔是国际单位制中七个基本物理量之一( )
(3)物质的量描述对象是分子、原子等微观粒子( )
(4)1mol氢中含有2mol氢原子和2mol电子( )
(5)1mol任何物质都含有6.02×
1023个分子( )
答案
(1)×
(2)×
(3)√ (4)×
(5)×
解析 物质的量是七大基本物理量之一,它表示的是一定数目粒子集合体的多少,而不表示物质的质量,也不表示物质所含微粒的数目。
摩尔只是物质的量的单位,而不是一个物理量,
(1)
(2)错误;
氢是元素的名称,没有指明粒子的种类,(4)错误;
构成物质的粒子除了分子外,还有原子、离子等,(5)错误。
易错警示 物质的量的单位使用时的注意事项
使用“mol”时,只用于表示原子、离子、分子、电子、质子、中子等所有微观粒子及它们的特定组合的多少,不能用于描述宏观物质的数量。
且必须指明物质所含粒子的种类,表述要确切。
2.下列关于阿伏加德罗常数的说法错误的是( )
A.6.02×
1023就是阿伏加德罗常数
B.0.012kg12C含有的碳原子数就是阿伏加德罗常数
C.含有阿伏加德罗常数个粒子的物质的量是1mol
D.1molNH3所含原子数约为2.408×
1024
答案 A
解析 阿伏加德罗常数(NA)是一个物理量,其单位是mol-1,数值约为6.02×
1023。
易错警示 阿伏加德罗常数(NA)是一个物理量,其单位是mol-1,而不是纯数值;
其精确值是0.012kg12C含有的碳原子数,约为6.02×
二、摩尔质量
1.试通过计算,填写下表:
1个微粒的实际质量(g)
6.02×
1023个
微粒的质量(g)
相对分子
(或原子)质量
H2O
2.990×
10-23
17.9998
18
Al
4.485×
26.9997
27
通过上表计算结果,你能得出的结论是6.02×
1023个微粒(1摩尔)的质量(以克为单位时),在数值上(近似)等于其相对分子(或原子)质量。
2.摩尔质量有关概念的理解
3.下列有关摩尔质量的描述或应用中正确的是( )
A.1molOH-的质量为17g·
mol-1
B.二氧化碳的摩尔质量为44g
C.铁原子的摩尔质量等于它的相对原子质量
D.一个钠原子的质量等于
g
答案 D
解析 A项中质量的单位为“g”;
B项单位应为“g·
mol-1”;
C项没有指出以“g·
mol-1”为单位,也没有指出在数值上相等;
D项中可用1molNa的质量除以1molNa的原子数,求得每个钠原子的质量。
三、关于物质的量的简单计算
1.基本关系式
(1)n=
(n表示物质的量,N表示粒子数)。
关系式中NA的单位是mol-1。
(2)M=
(M为摩尔质量,m为物质的质量)。
在M、n和m中,已知任意两项求第三项;
若M的单位是g·
mol-1时,则m的单位是g。
2.恒等关系式
由基本关系式n=
和n=
可得恒等关系式:
=n=
。
在N、NA、m、M中,已知任意三项可求第四项。
一般情况下,NA、M是已知的,则N与m可互求。
4.在14.2gNa2SO4中:
(1)含有的Na+的数目是;
(2)含有的SO
的质量是;
(3)含氧原子的物质的量是。
答案
(1)1.204×
1023
(2)9.6g (3)0.4mol
解析 由化学式Na2SO4可得如下关系式:
Na2SO4~2Na+~SO
~4O
方法一 n(Na2SO4)=
=0.1mol
所以有:
(1)n(Na+)=2n(Na2SO4)=0.2mol,
N(Na+)=0.2mol×
1023mol-1=1.204×
1023;
(2)n(SO
)=n(Na2SO4)=0.1mol,
m(SO
)=0.1mol×
96g·
mol-1=9.6g;
(3)n(O)=4n(Na2SO4)=0.4mol。
方法二 在关系式中,系数比等于粒子个数比,若都扩大6.02×
1023倍,则化学计量数比就等于物质的量比:
Na2SO4 ~ 2Na+ ~ SO
~ 4O
1mol 2mol 1mol 4mol
而在一个关系式中,等量的某一物质,可用不同的单位来表示。
如2molNa+,可用质量2×
23g来表示,也可用离子个数2×
1023来表示。
在计算时,为方便计算,通常是化学计量数反映的量与该物质(已知量或待求量)的题给单位相同。
如:
本题中已知量Na2SO4是14.2g,那么化学计量数反映的1mol的Na2SO4就用“142g”来计算;
(1)中求Na+的个数,化学计量数反映的2molNa+就用“2×
1023”来计算;
以此类推,有如下计算式:
Na2SO4 ~ 2Na+~ SO
=
解得:
N(Na+)=1.204×
)=9.6g n(O)=0.4mol。
5.设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A.2.3g钠由原子变成离子时,失去的电子数为0.2NA
B.0.2NA个硫酸分子与19.6g磷酸(H3PO4)含有相同的氧原子数
C.28g氮气所含的原子数为NA
D.NA个氧分子与NA个氢分子的质量比为8∶1
答案 B
解析 A中Na+为+1价,2.3g钠为0.1mol钠原子,失去的电子数为0.1NA,故A错误;
B中19.6g磷酸即为0.2NA个磷酸分子(19.6g÷
98g·
mol-1=0.2mol),等物质的量的硫酸(H2SO4)与磷酸(H3PO4)含有相同的氧原子数,故B正确;
C中28g氮气(N2)即为1mol氮分子(28g÷
28g·
mol-1=1mol),所以应含2NA个氮原子,故C错误;
D中NA个氧分子质量为32g,NA个氢分子质量为2g,则其质量比为16∶1,故D错误。
思维拓展 物质的量是物质的质量和微粒数目之间计算的桥梁,已知物质的质量求其微粒数目或已知物质的微粒数目求其质量都是先转换成物质的量,再计算微粒数目或质量。
特别要注意微粒可能是分子,也可能是所含的原子、离子、电子等。
直接代入公式时,各符号代表的微粒要统一。
也可根据物质组成的固定比例关系进行相关计算,如:
Na2SO4中各组成微粒之间的比例关系:
Na2SO4 ~ 2Na+ ~ SO
1mol 2mol 1mol 4mol
通过摩尔质量、阿伏加德罗常数就可以顺利知道一定质
量的物质中含有的微粒个数,物质的量起着桥梁的作用。
1.下列说法中正确的是( )
A.摩尔是用来描述微观粒子的物理量
B.0.5molH2O中含有的原子数目为1.5NA
C.64g氧相当于2mol氧
D.1mol任何物质都含有6.02×
1023个原子
解析 摩尔是物质的量的单位,而不是物理量,A不正确;
0.5molH2O中含有1molH原子和0.5molO原子共1.5mol原子,即1.5NA,B正确;
2mol氧未指明微粒种类,C不正确;
1mol任何物质不一定含有6.02×
1023个原子,如1molO2,D不正确。
2.下列说法正确的是( )
A.1mol氯含有6.02×
1023个微粒
B.阿伏加德罗常数的数值约等于6.02×
C.钠的摩尔质量等于它的相对原子质量
D.H2O的摩尔质量是18g
解析 使用摩尔时没有指明微粒的名称,或为1molCl2约含6.02×
1023个Cl2分子,或为1molCl约含6.02×
1023个Cl原子,A错误;
不要把摩尔质量与相对原子质量混同,应为钠的摩尔质量以g·
mol-1为单位时在数值上等于它的相对原子质量,C错误;
摩尔质量的单位为g·
mol-1,H2O的摩尔质量是18g·
mol-1,D错误。
3.某原子的摩尔质量是Mg·
mol-1,则一个该原子的真实质量是( )
A.MgB.
C.
gD.
答案 C
解析 以“g·
mol-1”为单位时,摩尔质量与相对原子质量及1mol原子的质量数值相等,所以,1mol原子的质量为Mg。
而1mol原子中含有原子的数目为6.02×
1023个,则1个原子的质量为
g。
4.下列说法不正确的是( )
A.硫酸的摩尔质量与6.02×
1023个磷酸分子的质量在数值上相等
B.6.02×
1023个N2和6.02×
1023个O2的质量比等于7∶8
C.3.2gO2所含的原子数目约为0.2×
D.常温、常压下,0.5×
1023个二氧化碳分子质量是44g
解析 H2SO4的摩尔质量为98g·
mol-1,6.02×
1023个H3PO4分子的质量为98g,二者数值相等,A正确;
1023个O2的质量比为二者的相对分子质量之比,即28∶32=7∶8,B正确;
3.2gO2物质的量为
=0.1mol,含氧原子数约为0.1×
2×
1023,C正确;
0.5×
1023个CO2物质的量为0.5mol,质量为0.5mol×
44g·
mol-1=22g,D不正确。
5.
(1)O2和O3是氧元素的两种单质。
根据分子式回答:
等质量的O2和O3所含分子数之比为,原子个数之比为。
(2)摩尔质量是指单位物质的量的物质所含有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为。
②1.28g某气体含有的分子数目为1.204×
1022,则该气体的摩尔质量为。
③已知一个铁原子的质量为bg,则铁的摩尔质量为。
④NA为阿伏加德罗常数,已知ag某气体中含分子数为b,则该气体的摩尔质量为。
答案
(1)3∶2 1∶1
(2)①17g·
mol-1 ②64g·
mol-1 ③bNAg·
mol-1 ④
g·
解析
(1)n(O2)∶n(O3)=
∶
=3∶2,则分子数之比为3∶2;
N1(O)∶N2(O)=(
×
2)∶(
3)=1∶1。
(2)依据摩尔质量的定义式:
M=
,结合物质的量(n)与NA的关系即可列出相关表达式,不要忘记单位。
[基础过关]
题组一 有关概念的理解
A.1mol氢约含有阿伏加德罗常数个氢
B.1molCaCl2含有1molCl-
C.1mol电子约含有6.02×
1023个电子
D.1molH2O含有1molH2和1molO
解析 A错误,未注明微粒的种类,氢是氢分子、氢原子还是氢离子不明确;
B错误,1molCaCl2应含有2molCl-;
D错误,由初中化学可知H2O中无H2,正确的表述为1molH2O含有2molH和1molO。
2.科学家发现一种化学式为H3的氢分子。
1molH3和1molH2具有相同的( )
A.分子数B.原子数
C.质子数D.电子数
解析 1molH3和1molH2分子数均为NA,原子数分别为3NA和2NA,质子数分别为3NA和2NA,电子数分别为3NA和2NA,A正确。
3.设NA代表阿伏加德罗常数的值。
下列说法正确的是( )
A.2.4g金属镁变成镁离子时失去的电子数目为0.1NA
B.18g水中含有0.1NA个水分子
C.1mol氮气所含的电子数目为NA
D.17g氨气所含电子数目为10NA
解析 2.4gMg的物质的量是0.1mol,变成镁离子时失去电子数目为0.2NA;
18gH2O的物质的量是1mol,含有NA个水分子;
1molN2含有14NA个电子。
4.下列叙述中正确的是( )
A.1mol任何物质都含有6.02×
1023个离子
B.0.012kg12C中含有约6.02×
1023个碳分子
C.1mol水中含有2mol氢和1mol氧
D.1molNe中含有6.02×
1024个电子
解析 因为有些物质是由分子组成(例如水、硫酸等),有些物质是由离子组成[例如NaCl、Ca(OH)2等],还有些物质是由原子直接构成的(例如金刚石等),所以A错;
碳是由原子构成的,所以B错;
没有指明粒子的种类,所以C错;
氖原子核外有10个电子,则1molNe含有10×
1023个电子,所以D正确。
5.偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。
下列叙述正确的是( )
A.偏二甲肼的摩尔质量为60g
1023个偏二甲肼分子的质量约为60g
C.1mol偏二甲肼的质量为60g·
D.6g偏二甲肼含有NA个偏二甲肼分子
解析 偏二甲肼的摩尔质量应为60g·
mol-1,A中单位不对;
1023个偏二甲肼约为1mol,其质量约为60g,B正确;
质量的单位应为g,C错误;
6gC2H8N2的物质的量为
=0.1mol,含有C2H8N2分子应为0.1NA,D错误。
题组二 n=
的应用
6.已知3.2g某气体中所含的分子数约为3.01×
1022,此气体的摩尔质量为( )
A.64g·
mol-1B.64mol
C.64gD.32g·
解析 n=
=0.05mol,M=
=64g·
mol-1,故选A项。
7.amolH2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为( )
A.
mol-1B.
mol-1D.
解析 由关系式n=
可知,NA=
,amolH2SO4中含4amol氧原子,相当于b个氧原子。
因而可得正确结果为NA=
mol-1。
8.铅笔芯的主要成分是石墨。
如果铅笔芯写一个字消耗的石墨质量约为1×
10-3g。
那么一个铅笔字含有的碳原子数约为( )
A.5×
1019个B.5×
1022个
C.2.5×
1022个D.2.5×
1019个
解析 n(C)=
mol,则含有碳原子个数为
mol×
1023
mol-1≈5×
1019。
9.下列关于相等物质的量的CO和CO2的比较中正确的是( )
①所含的分子数目之比为1∶1 ②所含的氧原子数目之比为1∶1 ③所含的原子总数目之比为2∶3 ④所含的碳原子数目之比为1∶1
A.①②B.②③
C.①②④D.①③④
解析 CO和CO2的物质的量相同,则含有的CO和CO2的分子数目也相同,则①正确;
又因CO和CO2分子中的氧原子数分别为1和2,则物质的量相同的CO和CO2所含的氧原子数目之比为1∶2,②错误;
CO和CO2的分子中原子总数之比为2∶3,③正确;
物质的量相同的CO和CO2,碳原子数目之比是1∶1,④正确。
10.下列物质中,与0.3molH2O含有相同氢原子数的物质是( )
A.18.9gHNO3
B.3.612×
1023个HCl分子
C.0.1molH3PO4
D.0.2NA个CH4分子
解析 0.3molH2O含氢原子0.6mol。
A中硝酸的物质的量为0.3mol,含氢原子为0.3mol;
B中HCl的物质的量为0.6mol,含氢原子为0.6mol;
C中含氢原子为0.3mol;
D中CH4的物质的量为0.2mol,含氢原子为0.8mol。
[能力提升]
11.在一定条件下,有下列物质:
①8gCH4 ②6.02×
1023个HCl分子 ③2molO2
按由小到大的顺序填写下列空白(填写序号):
(1)摩尔质量:
;
(2)物质的量:
;
(3)原子数目:
(4)质量:
。
答案
(1)①<
③<
②
(2)①<
②<
③ (3)②<
①<
③ (4)①<
③
解析
(1)摩尔质量分别是16g·
mol-1,36.5g·
mol-1,32g·
mol-1,故顺序是①<
②。
(2)8gCH4的物质的量:
n(CH4)=
=0.5mol,6.02×
1023个HCl分子的物质的量:
n(HCl)=
=1mol,故顺序是①<
③。
(3)原子的物质的量:
①中,0.5mol×
5=2.5mol;
②中,1mol×
2=2mol;
③中,2mol×
2=4mol。
故顺序是②<
(4)1molHCl的质量是36.5g,2molO2的质量是64g,故顺序是①<
12.填写下列空白:
(1)3.01×
1023个SO2分子中含有氧原子的个数为;
SO2气体的质量为。
(2)常温常压下,92gNO2气体含有的原子数为(用NA表示阿伏加德罗常数的值)。
(3)NO和O2可发生反应:
2NO+O2===2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为。
答案
(1)6.02×
1023 32g
(2)6NA (3)a∶(a+2b)
解析
(1)1个SO2分子含有2个氧原子,则3.01×
1023个SO2分子含有氧原子个数为3.01×
1023×
2=6.02×
该SO2气体的物质的量n=
=0.5mol,其质量m=0.5mol×
64g·
mol-1=32g。
(2)92gNO2气体含有的原子的物质的量为92g÷
46g·
mol-1×
3=6mol。
故所含原子个数为6NA。
(3)化学反应中原子进行了重新组合,但是原子的个数和种类没有改变。
反应后氮原子与氧原子的个数比等于反应前氮原子与氧原子的个数比,即a∶(a+2b)。
13.
(1)4.5gH2O与gH2SO4所含的分子数相等,它们所含氧原子数之比是。
(2)8.4gN2与9.6g某单质Rx所含原子数相同,且分子数之比为3∶2,则R的相对原子质量是,x值是。
答案
(1)24.5 1∶4
(2)16 3
解析
(1)n(H2O)=
=0.25mol,
m(H2SO4)=M(H2SO4)×
n(H2SO4)=98g·
0.25mol=24.5g。
氧原子数之比=(0.25mol×
1)∶(0.25mol×
4)=1∶4。
(2)设R的相对原子质量为y,
=3∶2,
2=
x,解得x=3,y=16。
14.已知12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为,R的相对原子质量为。
含R的质量为1.6g的Na2R,其物质的量为。
答案 62g·
mol-1 16 0.1mol
解析 1molNa2R中含有Na+2mol,R2-1mol,故含有0.4molNa+的Na2R的物质的量应为0.2mol。
那么M(Na2R)=
=62g·
mol-1,
M(R)=62g·
mol-1-2×
23g·
mol-1=16g·
mol-1,故1.6gR的物质的量为n(R)=
=0.1mol,所以n(Na2R)=n(R)=0.1mol。