元素及其化合物的计算题Word格式.docx
《元素及其化合物的计算题Word格式.docx》由会员分享,可在线阅读,更多相关《元素及其化合物的计算题Word格式.docx(12页珍藏版)》请在冰豆网上搜索。
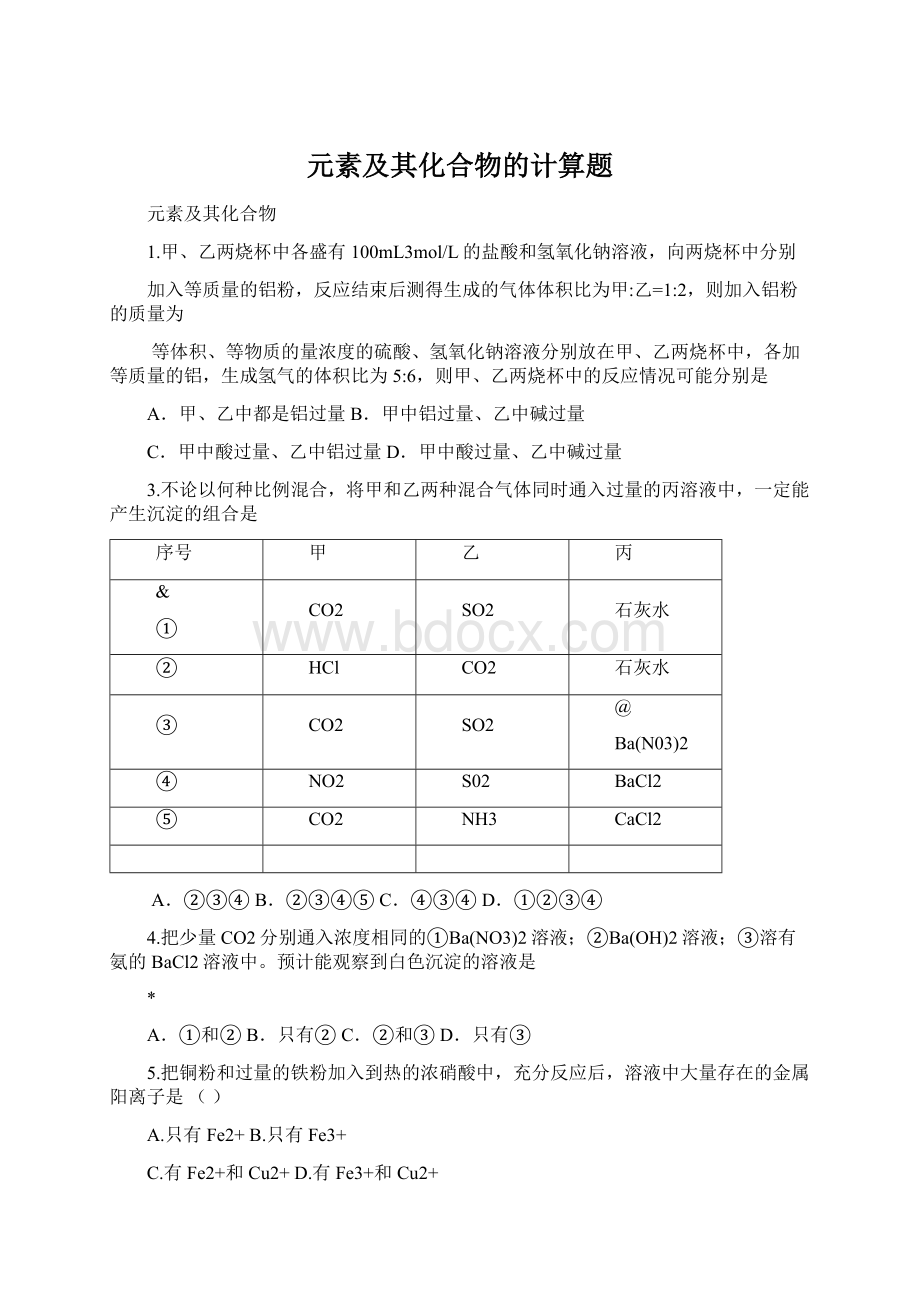
④
NO2
S02
BaCl2
⑤
NH3
CaCl2
A.②③④B.②③④⑤C.④③④D.①②③④
4.把少量CO2分别通入浓度相同的①Ba(NO3)2溶液;
②Ba(OH)2溶液;
③溶有氨的BaCl2溶液中。
预计能观察到白色沉淀的溶液是
*
A.①和②B.只有②C.②和③D.只有③
5.把铜粉和过量的铁粉加入到热的浓硝酸中,充分反应后,溶液中大量存在的金属阳离子是()
A.只有Fe2+B.只有Fe3+
C.有Fe2+和Cu2+D.有Fe3+和Cu2+
6.在硫酸铁溶液中,加入ag铜,完全溶解后,又加入bg铁,充分反应后得到cg残余固体,且b<c,则下列判断正确的是
A.最后得到的溶液中不含有Fe3+B.残余固体一定全部是铜
C.最后得到的溶液中只含Cu2+D.残余固体可能为铁、铜混合物
7.一定量的Fe和Fe2O3的混合物投入250ml2mol/L硝酸溶液中,反应完全
后,生成LNO(标况),再向反应后的溶液中加入1mol/LNaOH溶液,要使铁元素完全沉淀下来,所加入的NaOH溶液体积最少是()
mlmlmlD.不能确定
8.将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产生全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加,则下列有关叙述中正确的是
《
A.开始加入合金的质量可能为
B.参加反应的硝酸的物质的量为
C.生成沉淀完全时消耗NaOH溶液的体积为100mL
D.溶解合金时收集到NO气体的体积为
9.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等).则下列分析推理中不正确的是()
50ml盐酸
50mL盐酸
m(混合物)
]
V(CO2)(标准状况)
A.盐酸的物质的量浓度为/L
B.根据表中数据能计算出混合物中NaHCO3的质量分数
C.加入混合物时盐酸过量
D.混合物恰好与盐酸完全反应
10.把一定量的Na2O2的NaHCO3的混合粉末分为两等份,将其中一份加入100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为(标准状况下);
再将此气体通入另一份混合物中,充分反应后,得到O2(标准状况下),则原混合粉末中Na2O2和NaHCO3的物质的量之比及稀盐酸的物质的量浓度是()
)
A
B
C
D
Na2O2和NaHCO3的物质的量之比
8:
1
9:
2
2:
9
原稀盐酸的物质的量的浓度(mol·
L-1)
{
11.某无色溶液中可能含有I一、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液呈无色。
则下列关于溶液组成的判断正确的是()
①肯定不含I一②肯定不含Cu2+③肯定含有S032-④可能含有I—
A.①③B.①②③C.③④D.②③④
12.在一种酸性溶液中存在NO3-、I一、Cl_、Fe3+中的一种或几种,向该溶液中加入溴水,溴单质被还原,由此可推断该溶液中()
A.一定含有I一,不能确定是否有Cl—B.一定含有NO3-
C.不含有Fe3+D.一定含有I一、NO3-和Cl—
13.高温下硫酸亚铁发生如下反应:
2FeSO4
Fe2O3+SO2↑+SO3↑若将生成的气体通入氯化钡溶液中,得到的沉淀是()
"
A.BaSO3和BaSO4B.BaSC.BaSO3D.BaSO4
14.溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式IBr+H2O=HBr+HIO,下列有关IBr的叙述中,不正确的是()
A.IBr是双原子分子B.在很多反应中IBr是强氧化剂
C.和NaOH溶液反应生成NaBr和NaIOD.和水反应时,既是氧化剂又是还原剂
15.“XYn”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:
X<
Y),其化学性质和卤素单质相似。
下列说法中,正确的是
A.ICl与水反应可生成HCl和HIO,则1molICI参加反应转移电子为1mol
B.某温度,液态IF5电离:
2IF5≒IF4++IF6-,则c(IF4+)×
c(IF6-)是一个常数
C.BrCl与Zn反应生成ZnCl2和ZnBr2
D.XYn与卤素单质一样都是非极性分子
16.向某稀HNO3和Fe(NO3)3的混合溶液中逐渐加入铁粉,产生无色气体.该气体遇空气变红棕色,溶液中Fe2+浓度和加入Fe粉的物质的量之间的关系如图所示:
;
则稀溶液中HNO3和Fe(NO3)3的物质的量浓度之比为()
A.2:
1B.1:
1C.4:
1D.3:
17.向某FeBr2溶液中,通入(标准状况下)的Cl2,测得溶液中c(Br-)=3c(Cl—)=L。
反应过程中溶液的体积变化不计,则下列说法中正确的是()
A.原溶液的浓度为LB.反应后溶液中c(Fe3+)=L
C.反应后溶液中c(Fe3+)=c(Fe2+)D.原溶液中c(Br-)=L
18.某学生设计了如下图所示的方法对A盐进行鉴定:
—
由此分析.下列结论中,正确的有()
A.A中一定有Fe3+B.C中一定有Fe3+
C.B为AgI沉淀一定为FeBr2溶液
19.某工厂用CaSO4、H2O、NH3、CO2制备(NH4)2SO4,其工艺流程如下:
下列推断不合理的是
A.往甲中通入CO2有利于(NH4)2SO4的生成
;
B.生成lmol(NH4)2SO4至少消耗2molNH3
C.可采用加热蒸干的方法从滤液中提取(NH4)2SO4晶体
D.CaCO3煅烧所得的CO2可以循环使用
、B、C是中学化学中常见的三种化合物,它们各由两种元素组成.甲、乙是两种单质,三种化合物和单质之间存在如下关系:
(1)在A、B、C这三种化合物中,必定含有乙元素的是(用A、B、C字母填写)
(2)单质乙必定是(填“金属”或“非金属”),其理由是
(3)单质乙的化学式可能是,则化合物B的化学式是.
、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
试回答:
(1)若X的强氧化性单质,则A不可能是。
(填选项)
a.Sb.N2c.Nad.Mge.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为;
C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示),检验此C溶液中金属元素价态的操作方法是。
(3)若A、B、C为含有金属元素的化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式可能为,X的化学式可能为(写出不同类物质)
或,反应①的离子方程式为
。
或。
22.某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时验证氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。
(1)有的浓盐酸与足量的Mn02反应制C12,制得的C12体积(标准状况下)总是小于l.12L的原因是
(2)①装置B中盛放的试剂名称为,作用是.
②装置D和E中出现的不同现象说明的问题是。
③装置F的作用是。
④写出装置G中发生反应的离子方程式
…
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgN03溶液中的气体只有一种。
为了确保实验结论的可靠性,证明最终通入AgN03溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置,你认为该装置应加在与之问(填装置字母序号),装置中应放入(填写试剂或用品名称)
23.用下图装置进行SO2转化为SO3的转化率测定实验:
2SO2+O2
2SO3△H=-mol
|
(1)要顺利进行实验,上图Ⅰ、Ⅱ、Ⅲ处各应连接1个合适的装置,请从下列A~E中选择适宜的装置,将其序号填入空格内。
Ⅰ、Ⅱ、Ⅲ。
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(3)实验时,浓硫酸能顺利滴入烧瓶中,甲装置所起作用的原理是:
。
(4)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是。
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是若用大火加热有Cr2O3处的反应管时,SO2的转化率会(填升高、降低或不变)
(6)实验时若用的Na2SO3,加入的浓硫酸是足量的,反应结束时继续通入O2一段时间,称得Ⅱ处装置的质量增加,则本实验中SO2的转化率为。
(保留3位有效数字)
24.取A、B两份物质的量浓度相等的NaOH溶液.体积均为50ml.分别向其中通入一定量的CO2后,再分别稀释为100mL.
(1)在NaOH溶液中通入一定量的CO2后.溶液中溶质的组成可能是:
①②,③④.
(2)在稀释后的溶液中分别逐滴加0.1mol/L的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:
①分别加人足量的盐酸后的溶液中的溶质是.原NaOH溶液的物质的量浓度为
②A曲线表明.原溶液通入CO2后.所得溶质与HCl反应产生CO2的最大体积是mL(标准状况).
③B曲线表明,原溶液通入C02后.所得溶质的化学式为
其物质的量之比为.
【练习43】向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同溶液M的组成也不同。
若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况(不计CO2的溶解),则下列对应图形的判断正确的是
:
25.某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。
有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金。
并生产一定量的铁红和氧化铜。
填写下面的好空白
(1)图中标号处需加入的相应物质分别是①、②、③、④、⑤;
(2)写出①处发生反应的离子方程式;
写出③处发生反应的化学方程式;
(3)铁红的化学式为;
分别写出铁红和氧化铜在工业上的一种主要用途:
铁红;
氧化铜
26.下图为中学化学中几种常见物质的转化关系(部分产物已略去)。
已知:
A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。
【
(1)写出化学式A,D,F,G属于晶体;
(2)鉴定G中阳离子的实验方法和现象__________________________________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式、
。
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目。
27.在一定条件下(不需添加别的反应物),经不同的化学反应,可实现如下图的各种变化,其中,反应③、④、⑤属氧化还原反应,而反应①、②属非氧化还原反应。
X、F和Y为单质,且F是空气的主要成分之一,其余为化合物,据此请填空:
~
(1)物质A是_________,F是_______,X是________,Y是_________。
(2)写出反应②的化学反应方程式:
____________。
(3)写出反应④的化学反应方程式,并注明反应条件:
_____________。
28.铝土矿(主要成分为Al2O3、SiO2、Fe2O3)是提取氧化铝的原料。
提取氧化铝的工艺流程如下:
(1)滤液甲的主要成分是(写化学式)
(2)写出反应II的离子方程式:
(3)结合反应II,判断下列微粒结合质子(H+)的能力,由强到弱的顺序是
(填字母序号)
[
a.AlO2―或[Al(OH)4]-b.OH―c.SiO32―
(4)取滤液甲少许,加入过量盐酸,过滤;
再用惰性电极电解其滤液,两极均有气体产
生,且全部逸出,在阴极区还有沉淀生成,最后沉淀消失。
沉淀消失的原因可用离子方程式
表示为:
(5)取(4)电解以后的溶液mL,经分析,该溶液中只含有两种等物质的量浓度的碱性溶质,向其中逐滴加入mol•L-1盐酸溶液,当加入盐酸溶液时,生成的沉淀恰好溶解。
①加入盐酸溶液发生的离子反应的先后顺序依次为:
②请画出生成沉淀的物质的量与加入盐酸体积的关系图。
$
参考答案
9.B
11.
(1)de
(2)FeCl3;
2Fe3++Fe3Fe2+,防止Fe2+被氧化
用试管取少量C溶液,滴加KSCN溶液,无颜色变化,再滴加氯水(或硝酸),溶液呈红色,
证明原溶液中有Fe2+存在。
(3)Al(OH)3;
NaOH(或KOH);
HCl(或其他强酸)
Al3++3OH—Al(OH)3↓;
AlO2—+H++H2OAl(OH)3↓
12.
(1)Ⅰ:
BⅡ:
AⅢ:
E
(2)检查装置的气密性
(3)保持分液漏斗内压强与烧瓶内压强相等
(4)先加热催化剂,然后缓慢滴加浓硫酸
(5)温度过高不利于SO3的生成,且影响催化剂的活性。
降低
(6)%
14.
(1)N2、Cl2、NH3、离子晶体;
(2)取少量D的溶液加人试管中,用胶头滴管加入少量NaOH浓溶液,加热用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色
(3)2OH-+Cl2=ClO-+Cl-+H2O8NH3+3Cl2====N2+6NH4Cl
(4)
15.
⑴ NaOH、Na[Al(OH)4](或NaAlO2)、Na2SiO3
⑵ CO2+2OH-==CO32-+2H2O
CO2+2[Al(OH)4]-==2Al(OH)3↓+CO32-+H2O
⑶ b>a>c
⑷ Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2-+2H2O
⑸①H++OH-==H2O[Al(OH)4]-+H+==Al(OH)3↓+H2OAl(OH)3+3H+==Al3++3H2O
②图像如下所表示。