大学芳烃芳香性练习题和答案Word文件下载.docx
《大学芳烃芳香性练习题和答案Word文件下载.docx》由会员分享,可在线阅读,更多相关《大学芳烃芳香性练习题和答案Word文件下载.docx(30页珍藏版)》请在冰豆网上搜索。
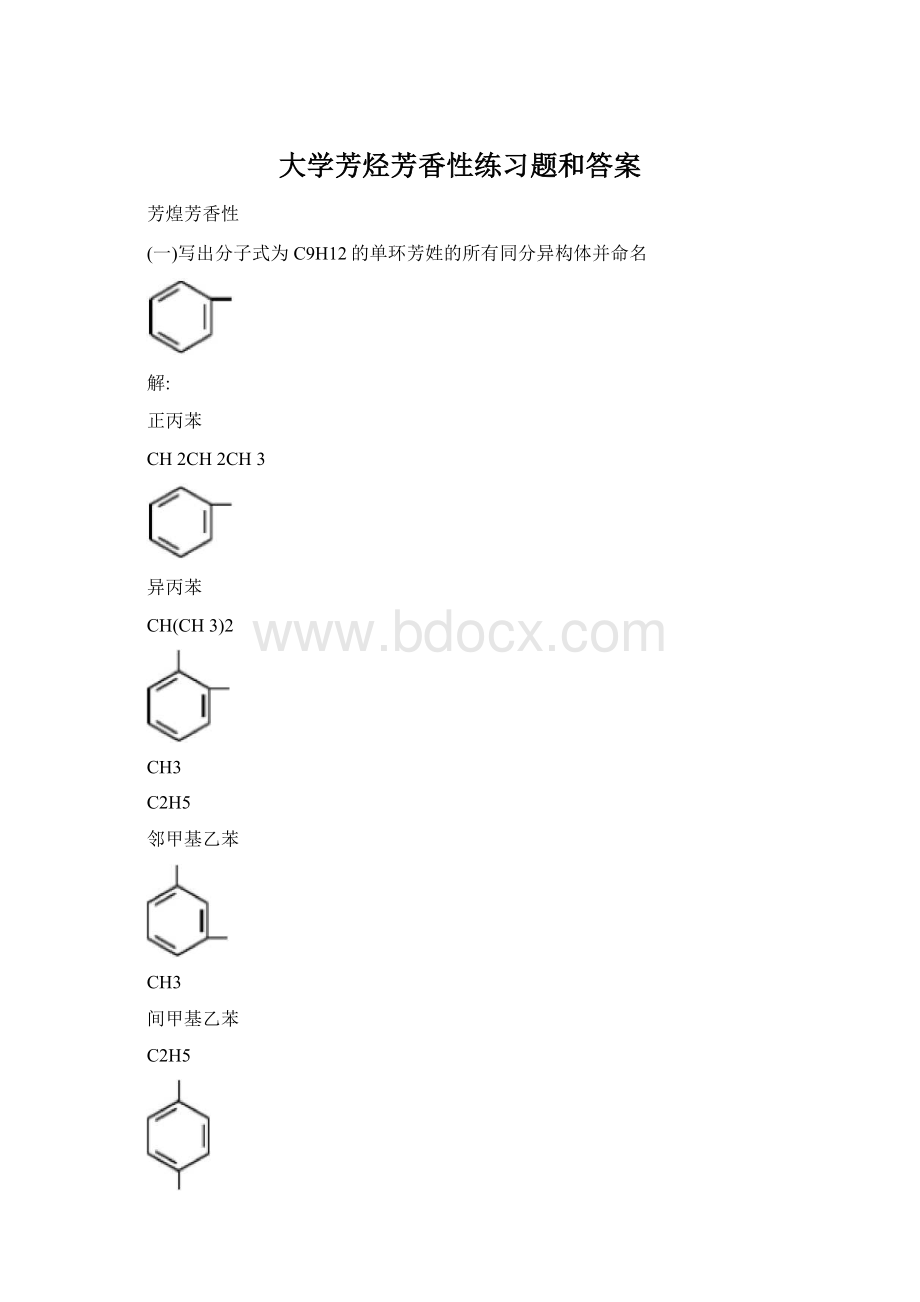
⑶4-硝基-2-氯甲苯
(6)1-甲基慈
(9)4-羟基-5-澳-1,3-苯二磺酸
解:
(1)3-对甲苯基戊烷
(4)1,4-二甲基泰
(7)2-甲基-4-氯苯胺
(2)(Z)-1-苯基-2-丁烯
(5)8-氯-1-泰甲酸
(8)3-甲基-4羟基苯乙酮
(三)完成下列各反应式:
红色括号中为各小题所要求填充的内容。
⑴
+ClCH2CH(CH3)CH2CH3
AICI3
(过重)+CH2c}
AlCl31\
"
IVJ^C-CH2CH3;
HNO3
H2SO4
ANO2+
(5)
(CH3)2C=CH
HF
K2SO7
A
HNO3,H2SO4o*
0C
BF3OH——
CH2——CH2AlCl
CH2-CH
(CH3)3C
(1)KMnO
CH2CH2CH2CH3
(2)H3O
(主要产物)
o2n
C(CH3)3
CH2O,HCl
-_ZnCl2
C2H5Br
AlCl3
CH2cH20H
COOH
CH2-CH2-
CH2C1
C(CH3)3
O-O
cHCH2
O
(12)
(13)
2H
Pt
(10)
CH2CH2CClII
O
(14)
(15)
Zn
(A)
(B)
COCH3
CH2Cl1
—CH2(CH2)2COOH
H3O
CH2cH2c(CH3)2
OH
OAQ°
AlCl3
Zn-Hg
HCl
CHO+CH2O
OII公广C(CH2)2COOH
CH2cH33
CHCH3
Br
KOH
-
CH=CH2
CH-CH2
Br2
CC14
(四)用化学方法区别下列各组化合物:
(1)环己烷、环己烯和苯
环己烯、
(2)苯和1,3,5-己三烯
・退色
(1)环己烷卜
iX、
XJ
B3Fe
K
退色
1,3,5-己三烯
KMnO4
(五)写出下列各反应的机理:
SO3H+H3O
H+
SO3H
+H2SO4+H2O
S03H-H+,-SO3
H
(2)C6H6+C6H5CH20H+H2SO4——(C6H5)2cH2+H3O++HSO4-
H+十-H2OC•C6H5CH2
C6H5CH20H—C6H5CH20H2-C6H5cH2.
-H+
一AC6H5CH2c6H6
(箭头所指方向为电子云流动的方向!
)
C6H5\H2SO4
(3)C=CH2
叫
CH3C\
产2
C6H5
C6H5XC=CH2H+rC6H5—[CH3CH2=C(CH3)Ph
CH3/CH3
cCCH2C-Ph
CH3、,CH3
C
-H
CH2——
c]
HI、C6H5
CH3\/CH3
cz
、CH2
CH3,'
c6H5
CH3—C—Cl
(4)3C
十
aCH3—C
II
+AlCl4
|+CH
工mch
(六)己知硝基苯(Ph—NO2)进行亲电取代反应时,具活性比苯小,一NO2是第类定位基。
试部亚硝基苯(Ph—NO)进行亲电取代反应时,其活性比苯大还是小?
一NO是第几类定位基?
由于氧和氮的电负性均大于碳,在亚硝基苯中存在下列电动去的转移:
所以亚硝基苯(Ph-NO)进行亲电取代反应时,其活性比苯小,一NO是第二类定位基。
(七)写出下列各化合物一次硝化的主要产物:
H3L41COOH
高温
低温
OCH3
相关的L络合物中正电荷分散程度更大,反应活化能更低:
HNO2
B.(13)的一元硝化产物为
而不是
是因
为前者的空间障碍小,
热力学稳定。
(八)利用什么二取代苯,经亲电取代反应制备纯的下列化合物?
O2N
NO
可用下列二取代苯分别制备题给的各化合物:
(九)将下列各组化合物,按其进行硝化反应的难易次序排列:
(1)苯、间二甲苯、甲苯
(1)间二甲苯〉甲苯〉苯
(2)乙酰苯胺、苯乙酮、氯苯
解释:
苯环上甲基越多,对苯环致活作用越强,越易进行硝化反应。
(2)乙酰苯胺〉氯苯〉苯乙酮
连有致活基团的苯环较连有致钝集团的苯环易进行硝化反应。
对苯环起致活作用的基团为:
一NH2,—NHCOCH3且致活作用依次减小。
对苯环起致钝作用基团为:
一Cl,一COCH3且致钝作用依次增强。
(十)比较下列各组化合物进行一元澳化反应的相对速率,按由大到小排列。
(1)甲苯、苯甲酸、苯、澳苯、硝基苯
(2)对二甲苯、对苯二甲酸、甲苯、对甲基苯甲酸、间二甲苯
(1)一元澳化相对速率:
甲苯>苯>澳苯〉苯甲酸〉硝基苯
致活基团为一CH3;
致钝集团为一Br,—COOH,-NO2,且致钝作用依次增强。
(2)间二甲苯〉对二甲苯〉甲苯〉对甲基苯甲酸〉对苯二甲酸
一CH3对苯环有活化作用且连接越多活化作用越强。
两个甲基处于间位的致活
效应有协同效应,强于处于对位的致活效应;
一
COOH有致钝作用。
(十一)在硝化反应中,甲苯、甲基澳、平基氯和平基氟除主要的到邻和对位硝
基衍生物外,也得到问位硝基衍生物,其含量分别为3%、7%、14%和18%
试解释之。
这是一F、一Cl、一Br的吸电子效应与芳基中一CH2一的给电子效应共同作用的结果。
电负性:
F>
Cl>
Br>
邻、对位电子云密度:
甲苯〉茉基澳〉芳基氯〉茉基氟
新引入硝基上邻、对位比例:
新引入硝基上间位比例:
甲苯〈茉基澳〈茉基氯〈茉基氟
(十二)在硝化反应中,硝基苯、苯基硝基甲烷、2-苯基-1-硝基乙烷所得间位异
构体的量分别为93%、67%和13%。
为什么?
硝基是强的吸电子基
(-I、-C),它使苯环上电子云密度大大降低,新引入基上间位。
CH2^—CH2-NO2CH>
—CH2—CH2—NO2
硝基苯
苯基硝基甲烷
2-苯基-1-硝基乙烷
硝基对苯环的-I效应迅速减弱,烧基对苯环的+C效应逐渐突显
硝化产物中,间位异构体的比例依次降低
(十三)甲苯中的甲基是邻对位定位基,然而三氟甲苯中的三氟甲基是问位定位
基。
由于氟的电负性特别大,导致F3C—是吸电子基,对苯环只有吸电子效应,而无供电子
效应,具有间位定位效应。
(十四)在A1C13催化下苯与过量氯甲烷作用在0c时产物为1,2,4.三甲苯,而在
100c时反应,产物却是1,3,5-三甲苯。
前者是动力学控制反应,生成1,2,4-三甲苯时反应的活化能较低;
后者是热力学控制反
应,得到的1,3,5-三甲苯空间障碍小,更加稳定。
(十五)在室温下,甲苯与浓硫酸作用,生成约95%的邻和对甲苯磺酸的混合物。
但在150~200c较长时间反应,则生成问位(主要产物)和对位的混合物。
试解释
之。
(提示:
问甲苯磺酸是最稳定的异构体。
高温条件下反应,有利于热力学稳定的产物(间甲苯磺酸)生成。
(十六)将下列化合物按酸性由大到小排列成序:
(3)>
(1)>
(5)>
(2)>
(4)
各化合物失去H+后得到的碳负离子稳定性顺序为:
碳负离子越稳定,H+越易离去,化合物酸性越强。
(4)。
(十七)下列反应有无错误?
若有,请予以改正。
CH2
NO2H2SO4
CH2,--NO2
错。
右边苯环由于硝基的引入而致钝,第二个硝基应该进入电子云密度较大的、左边的苯环,且进入亚甲基的对位。
I+FCH2cH2cH2c1
^CH2cH2cH2F
A1C13
FCH2CH2CH2+在反应中要重排,形成更加稳定的2o或3o碳正离子,产物会异构化。
即主要产物应该是:
rrcH
CH2F
若用BF3作催化剂,主要产物为应为
产3
CH2CI
CH2-CH3
no2
CH3COC1
A1C13
C-CH3HC1
IIO
①硝基是致钝基,
②用Zn-Hg/HCl
还原为氨基。
硝基苯不会发生傅
还原间硝基苯乙酮时,
-克酰基化反应;
不仅默基还原为亚甲基,而且还会将硝基
++C1CH=CH2
rsi<
>
I-CH=CH2
AI
CH2=CHC1分子中—C1和C=C形成多电子p—兀共轲体系,使C-C1具有部分双
键性质,不易断裂。
所以该反应的产物是
PhCH(Cl)CH3。
(十八)用苯、甲苯或蔡等有机化合物为主要原料合成下列各化合物:
(2)邻硝基苯甲酸
(4)4-硝基-2,6二澳甲苯
⑸
对硝基苯甲酸对硝基氯苯
CH=CH-CH3
COOHNO2
NO2NO2
.1-H2SO4
[*
CH3CH3
NO2H2O/H+
o~也
180C
SO3HSO3H
(3)
CI2,Fe3
A
h2soJ
CH2=CHCH2Cl
r^\]-CH2CH=CH2HCl.
CH2CHCH3
Cl
NaOH