无机及分析化学学习指导答案文档格式.docx
《无机及分析化学学习指导答案文档格式.docx》由会员分享,可在线阅读,更多相关《无机及分析化学学习指导答案文档格式.docx(16页珍藏版)》请在冰豆网上搜索。
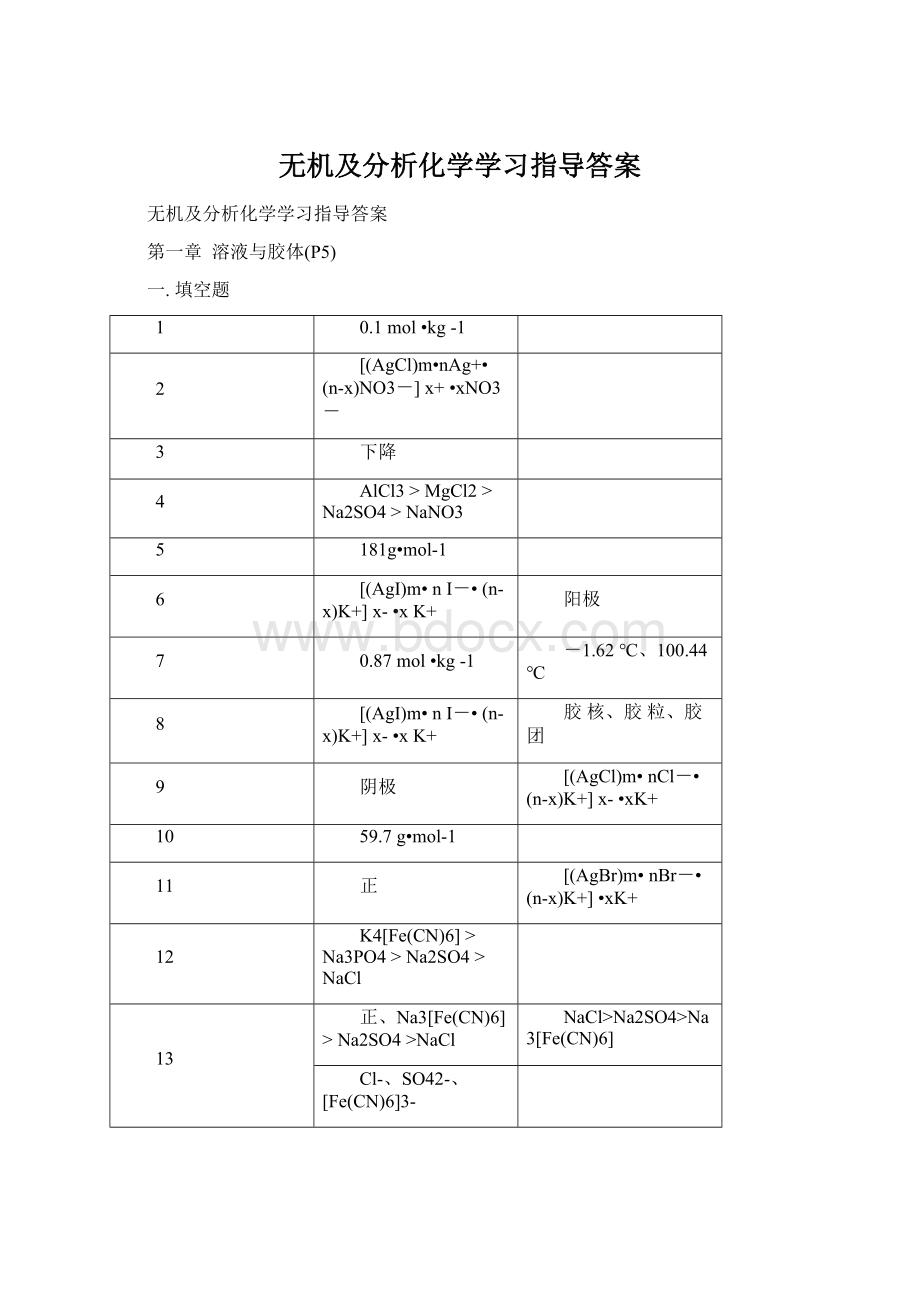
阴极
[(AgCl)m•nCl-•(n-x)K+]x-•xK+
10
59.7g•mol-1
11
正
[(AgBr)m•nBr-•(n-x)K+]•xK+
12
K4[Fe(CN)6]>
Na3PO4>
NaCl
13
正、Na3[Fe(CN)6]>
NaCl
NaCl>
Na2SO4>
Na3[Fe(CN)6]
Cl-、SO42-、[Fe(CN)6]3-
14
渗透压大小顺序为:
Na2SO4>
KCl>
甘油(C3H8O3)=葡萄糖(C12H22O11)
蒸汽压高低顺序:
甘油(C3H8O3)=葡萄糖(C12H22O11)>
KCl>
Na2SO4
沸点高低顺序为:
甘油(C3H8O3)=葡萄糖(C12H22O11)
凝固点高低顺序:
二.选择题
1.D2.D3.D4.D5.B6.B7.C
三、简答题
1.解:
分两种情况
NaCl溶液浓度大于AgNO3溶液,NaCl过量,溶胶为负溶胶,电场中向正极移动。
则胶团结构为[(AgCl)m•nCl-•(n-x)Na+]x-•xNa+
AgNO3溶液浓度大于NaCl溶液,AgNO3过量,溶胶为正溶胶,电场中向负极移动。
则胶团结构为[(AgCl)m•nAg+•(n-x)NO3-]x+•xNO3-
2.解:
溶胶稳定的因素主要是胶粒带电,其他有布朗运动和溶剂化膜等;
促使聚沉的办法有加入电解质、加热和按比例混合正负溶胶等;
用电解质聚沉溶胶时,表现为哈迪-叔尔采规律,即离子电荷数越高,则其聚沉能力越强。
(说明:
胶体稳定性的原因主要有胶粒带电、布朗运动以及溶剂化膜等方面,但以胶粒带电贡献最大,所以一般回答胶粒带电即可。
)
3.解:
依数性问题,故看溶液中的粒子数量多少,由于电离作用,NaCl溶液相当0.2mol•L-1,Na2SO4溶液相当0.3mol•L-1,甘油和葡萄糖溶液不发生电离,故粒子数量浓度为0.1mol•L-1。
故四种溶液的依数性性大小顺序为:
甘油(C3H8O3)=葡萄糖(C12H22O11)。
4.解:
经判断,BaCl2过量,溶胶为正溶胶,胶团结构为
[(BaSO4)m•nBa2+•(n-2x)Cl-]2x+•2xCl-
对于正溶胶的聚沉作用,电解质起作用的主要为阴离子,并且满足哈迪-叔尔采规律,故聚沉能力大小顺序为:
K3[Fe(CN)6]>
MgSO4>
AlCl3
第二章化学反应的能量和方向(P14)
内能、焓、熵
>
0,<
0,>
0
201.3kJ·
mol-1
大于
金刚石
△U=Q+W
封闭体系
460J
全部
1.B2.C3.C4.D5.C6.D7.B
三.判断题
1.√2.×
3.×
4.×
四.计算题
根据题意
,
吉布斯-亥姆霍兹方程
T=1000K时:
反应1克氢气,该反应进度为0.5mol,则每克氢气完全反应后,最多可得到的有用功为:
2Ag2O(s)=4Ag(s)+O2(g)
吉布斯-亥姆霍兹方程:
Ag2O的热分解温度,即
2NH3(g)=N2(g)+3H2(g)
(1)在标准状态和298.15K时,
在标准状态和298.15K时反应不能正向自发。
(2)在标准状态下反应自发进行的最低温度:
即
说明在标准状态下反应自发进行的最低温度为463.8K。
C2H5OH(l)=C2H5OH(g)
-276.98-234.81
160.67282.70
(1)100kPa与298K时:
,所以反应不能正向进行。
(2)同理:
100K与373K时,
,所以反应能正向进行。
(3)100kPa乙醇沸腾时,气态与液态乙醇达到平衡时,
5.解:
H为状态函数,故可根据下式计算该过程的rHm。
C6H12O6(s)→2CH3CH2OH(l)+2CO2(g)
查表:
fHm[C6H12O6(s)]=-1274.4kJ/mol,fHm[CH3CH2OH(l)]=-276.98kJ/mol,
fHm[CO2(g)]=-393.51kJ/mol,
rHm=2fHm[CH3CH2OH(l)]+2fHm[CO2(g)]-fHm[C6H12O6H(s)]
=2×
(-276.98)+2×
(-393.51)-(-1274.4)
=-66.58(kJ/mol)
(该法为本题的标准解法)
另解:
H为状态函数,故可根据下式计算该过程的rHm。
cHm[C6H12O6(s)]=-2815.8kJ/mol,cHm[CH3CH2OH(l)]=-1366.75kJ/mol
cHm[CO2(g)]=0
rHm=cHm[C6H12O6(s)]-2cHm[CH3CH2OH(l)]-2cHm[CO2(g)]
=-2815.8-2×
(-1366.75)-2×
=-82.3(kJ/mol)
第三章化学反应的速率和限度(P19)
1.减少,增加
2.v=kc(NO2Cl)
3.加,降,不变
4.反应NH4HS(s)=NH3(s)+H2S(s),
,53kPa
5.v=kc(NO)c(O2)
6.减少,增加
7.单位体积内活化分子数
8.v=kc(CO)c(NO2),质量作用,二,一
9.二
1.D2.C3.B4.D5.(反应ΔH<
0)A6.D7.C8.A9.B
10.D11.D12.D13.D14.C
1.×
2.×
3.√4.√5.√6.√7.√
第四章物质结构简介(P30)
1.诱导力、色散力
2.sp2,sp3,PF3
3.4,VA,p,33
4.1s22s22p63s23p63d54s2,4,VIIB,d
5.分子间,分子内,分子间
6.电负性差,偶极矩
7.4s3d4p
8.屏蔽效应和钻穿效应,18,8
9.H2O、H2S、H2Se,H2O、H2Se、H2S,氢键
10.1
11.4,IIIA,p,33
12.正三角形,三角锥,sp2,sp3
13.诱导力、色散力
14.正三角形,三角锥,sp2,sp3
15.4,VA,p,33
16.诱导力、色散力
17.4s3d4p
18.若n=2,3,4时,填“大”;
若n=5,6时,填“小”;
1.A2.B3.B4.A5.C6.B7.D8.B9.D
10.C11.D12.D13.B14.C
1.×
2.√3.×
4.√
第五章分析化学概论(P35)
三、二、无限多
1.B2.C3.D4.C5.D6.B7.C8.A
4.√5.×
6.×
7.√
第六章酸碱平衡和酸碱滴定法(P42)
1.CO32-HPO42-F-
2.3.303.15
3.HAc减小
4.cKaθ≥10-8
5.酚酞
6.c(H+)=c(Ac-)+c(OH-)
7.HSO3-Ka2θ(H2SO3)Kw/Ka2θ(H2SO3)=7.7×
10-13
1.D2.C3.B4.B5.C6.D7.A8.A
9.B10.A11.C12.A13.A14.A15.C16.A
1.×
2.√3.√4.×
5.√6.√7.×
8.×
设取0.1mol•L-1的HAc和NaAc溶液分别为xmL和ymL
2.
该药品纯度达到了药典的规定。
3.该试样是由NaHCO3和Na2CO3
4.设需1.0mol•L-1的NH3•H2O和1.0mol•L-1的NH4Cl各y毫升和x毫升
需NH3•H2O溶液360mL和NH4Cl溶液640mL。
第七章沉淀于溶解平衡与沉淀滴定法(P48)
1.CaF>
BaCO4>
AgCl
2.Mg(OH)2>
Ag2CrO4>
3.
4.同离子效应
1.C2.C3.A4.B5.C
1、×
1.答:
可用同离子效应解释
由题意可知:
c(Ag+)=0.08mol•L-1c(Cl-)=0.1mol•L-1
Ag(CN)2-+Cl-=AgCl+2CN-
该反应的平衡常数:
答:
需在溶液中保持自由CN-的最低浓度为2.26
10-7mol•L-1。
由多重平衡得:
AgCl+2NH3=[Ag(NH3)2]++Cl-
溶解时还要消耗0.2mol,所以,需要氨水的最初浓度是2.6mol•L-1。
要溶解0.01molAgCl需要的最低氨水浓度:
溶解时还要消耗0.02mol,所以,需要氨水的最初浓度是0.78mol•L-1。
0.78<
1,故AgCl全部溶解
第八章配位化合物和配位滴定法(P54)
1.三氯•一氨•合铂(
)酸钾
2.[PtCl2(NH3)4]2+Cl2,[PtCl2(NH3)4]2+,6,NH3、Cl-
3.小、大
4.二溴化一草酸根•四水合铂(Ⅳ)、6
5.氯化二硫氰酸根•二乙二胺合铬(
)、6
6.越大、越小越好
7.二氯化二氯•二乙二胺合铂(Ⅳ)、6
1.A2.D3.B4.D5.D
2.×
3.√
煤中所含硫的质量分数为0.3207
(1)在50mL0.10mol•L-1AgNO3溶液中,加入等体积6.4mol•L-1NH3·
H2