人教版选修3第二节《分子的立体结构》word学案Word文档格式.docx
《人教版选修3第二节《分子的立体结构》word学案Word文档格式.docx》由会员分享,可在线阅读,更多相关《人教版选修3第二节《分子的立体结构》word学案Word文档格式.docx(12页珍藏版)》请在冰豆网上搜索。
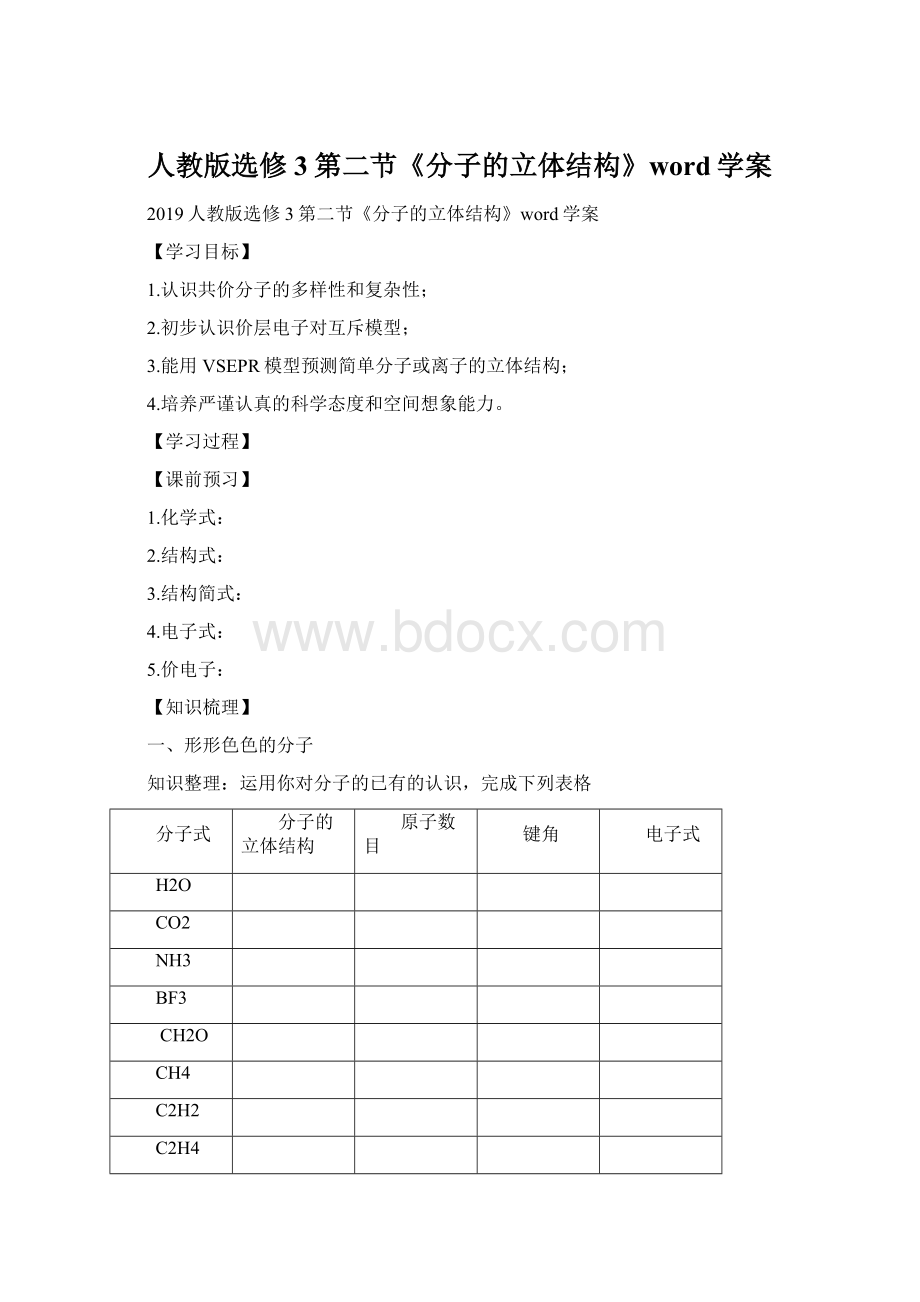
原子数目
键角
电子式
H2O
CO2
NH3
BF3
CH2O
CH4
C2H2
C2H4
C6H6
C8H8
P4
二、价层电子对互斥模型(VSEPR模型)
1.填表
分子
CH2O
分子内原子总数
价层电子数
中心原子孤对电子对数
空间结构
2.“价层电子对互斥模型”简称()的基本观点:
分子中的价电子对----成键电子对和孤对电子由于相互排斥作用,尽可能趋向彼此远,排斥力最。
3.对于ABn型分子,A原子与B原子间以共价双键、共价三键结合,价层电子对互斥理论仍然适用,这时应把双键或三键当作电子对来看待。
4.价层电子对之间斥力大小顺序为:
>
。
5.对于ABm型分子空间结构确定的一般规则为:
1)确定中心原子(A)的价层电子对数n
其中,中心原子的价电子数为中心原子的,氢原子和卤素原子按价电子,按不提供价电子算。
2)根据从推断出理想的几何结构。
3)根据孤对电子和成键电子对数估计实际构型,要求实际构型应该满足互斥力,结构。
【典题解悟】
例1.在以下的分子或离子中,空间结构的几何形状不是三角锥形的是()
A.NF3B.CH3-C.BF3D.H3O+
解析:
其中NF3、CH3-和H3O+的中心原子N、C、O均为sp3杂化,但是只形成3个化学键,有1个杂化轨道被孤对电子占据,又由于价层电子对相互排斥,所以为三角锥形;
只有BF3中的B以sp2杂化,形成平面正三角型分子。
所以选C。
答案:
C
例2.有关甲醛分子的说法正确的是()
A.C原子采取sp杂化B.甲醛分子为三角锥形结构
C.C原子采取sp2杂化D.甲醛分子为平面三角形结构
甲醛分子分子(CH2O)中心C原子采用的是sp2杂化,三个杂化轨道呈平面三角形,2个sp2杂化轨道分别与一个H原子形成一个C—H键,另一个sp2杂化轨道与O原子形成一个键,C原子中未用于杂化的个p轨道与O原子的p轨道形成一个键。
CD
【当堂检测】
1.下列物质中,分子的立体结构与水分子相似的是()
A.CO2B.H2SC.PCl3D.SiCl4
2.下列分子的立体结构,其中属于直线型分子的是()
A.H2OB.CO2C.C2H2D.P4
3.下列分子中,各原子均处于同一平面上的是()
A.NH3B.CCl4C.H2OD.CH2O
4.下列分子的结构中,原子的最外层电子不都满足8电子稳定结构的是()
A.CO2B.PCl3C.CCl4D.NO2
5.下列分子或离子的中心原子,带有一对孤对电子的是()
A.XeO4B.BeCl2C.CH4D.PCl3
6.写出你所知道的分子具有以下形状的物质的化学式,并指出它们分子中的键角分别是多少?
(1)直线形
(2)平面三角形
(3)三角锥形
(4)正四面体
7.为了解释和预测分子的空间构型,科学家在归纳了许多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。
这种模型把分子分成两类:
一类是;
另一类是。
BF3和NF3都是四个原子的分子,BF3的中心原子是,NF3的中心原子是;
BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是
8.用价层电子对互斥模型推测下列分子或离子的空间构型。
BeCl2;
SCl2;
SO32-;
SF6
参考答案:
1.D2.BC3.CD4.D5.D
6.
(1)CO2、CS2、HCN键角180°
(2)BF3、BCl3、SO3、CH2O键角60°
(3)NH3、PCl3键角107.3°
(4)CH4、CCl4键角109°
28′
7.中心原子上的价电子都用于形成共价键中心原子上有孤对电子BNBF3分子中B原子的3个价电子都与F原子形成共价键,而NF3分子中N原子的3个价电子与F原子形成共价键,还有一对为成键的电子对,占据了N原子周围的空间,参与相互排斥,形成三角锥形
8.直线形V形三角锥正八面体
第二节分子的立体结构
第二课时
1.认识杂化轨道理论的要点
2.进一步了解有机化合物中碳的成键特征
3.能根据杂化轨道理论判断简单分子或离子的构型
1.杂化轨道理论是一种价键理论,是为了解释分子的立体结构提出的。
2.杂化及杂化轨道:
叫做杂化,
称为杂化轨道。
1.甲烷分子中,C的价电子是,C原子的4个价层原子轨道是3个相互垂直的和1个球形的;
H的价电子是,用C原子的4个价层原子轨道跟4个H原子的1s球形原子轨道重叠,它们形成的四个C-H键应该(填“一样”或“不一样”,下同),而实际上,甲烷中四个C-H键是 ,为了解决这一矛盾,提出了杂化轨道理论。
2.当C原子和4个H原子形成甲烷分子时,C原子的 轨道和3个轨道就会发生混杂,混杂时保持轨道总数不变,得到四个相同的轨道,称为杂化,夹角是。
3.杂化后形成的都是键(填σ或π)。
sp杂化由轨道和轨道杂化而成,得到条夹角为的形轨道。
sp2杂化由轨道和轨道杂化而成,得到条夹角为的形轨道。
【总结评价】
分析、归纳、总结多原子分子立体结构的判断规律,完成下表
化学式
杂化轨道数
杂化轨道类型
分子结构
例1.有关苯分子中的化学键描述正确的是()
A.每个碳原子的sp2杂化轨道中的其中一个形成大π键
B.每个碳原子的未参加杂化的2p轨道形成大π键
C.碳原子的三个sp2杂化轨道与其它形成三个σ键
D.碳原子的未参加杂化的2p轨道与其它形成σ键
解析:
苯分子中每个碳原子中的三个sp2杂化轨道分别与两个碳原子和一个氢原子形成σ键.同时每个碳原子还有一个未参加杂化的2p轨道,他们均有一个未成对电子.这些2p轨道相互平行,以“肩并肩”方式相互重叠,形成一个多电子的大∏键.
BC
例2:
在乙烯分子中有5个σ键、一个π键,它们分别是()
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键
D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键
乙烯分子结构式为
,六个原子位于同一平面,键角为120°
,分子的中心原子C形成的都是sp2杂化轨道。
每个C原子都用1个sp2杂化轨道与H原子形成一个键,两个C原子间用各自的另一个sp2杂化轨道形成C—C键,C原子中未用于杂化的一个2p轨道分别与另一个C原子的2p轨道形成一个键。
1.下列分子中心原子是sp2杂化的是()
APBr3BCH4CBF3DH2O
2.关于原子轨道的说法正确的是()
A凡是中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体
BCH4分子中的sp3杂化轨道是由4个H原子1s轨道和C原子的2p轨道混合起来而形成的
Csp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相近
的新轨道
D凡AB3型的共价化合物,其中中心原子A均采用sp3杂化轨道成键
3.用Pauling的杂化轨道理论解释甲烷分子的四面体结构,下列说法不正确的是()
A.C原子的四个杂化轨道的能量一样
B.C原子的sp3杂化轨道之间夹角一样
C.C原子的4个价电子分别占据4个sp3杂化轨道
D.C原子有1个sp3杂化轨道由孤对电子占据
4.下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是()
Asp杂化轨道的夹角最大Bsp2杂化轨道的夹角最大
Csp3杂化轨道的夹角最大Dsp3、sp2、sp杂化轨道的夹角相等
5.乙烯分子中含有4个C—H和1个C=C双键,6个原子在同一平面上。
下列关于乙烯分子的成键情况分析正确的是()
A每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道
B每个C原子的1个2s轨道与2个2p轨道杂化,形成3个sp2杂化轨道
C每个C原子的2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道
D每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道
6.ClO-、ClO2-、ClO3-、ClO4-中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构
微粒
ClO-
ClO2-
ClO3-
ClO4-
立体结构
7.根据杂化轨道理论,请预测下列分子或离子的几何构型:
CO2,CO32-
H2S,PH3
8.为什么H2O分子的键角既不是90°
也不是109°
28′而是104.5°
?
1~5CCDABD
6、直线;
V型;
三角锥形;
正四面体
7、sp杂化,直线;
sp2杂化,三角形;
sp3杂化,V型;
sp3杂化,三角锥形
8、因为H2O分子中中心原子不是单纯用2p轨道与H原子轨道成键,所以键角不是90°
;
O原子在成键的同时进行了sp3杂化,用其中2个含未成对电子的杂化轨道与2个H原子的1s轨道成键,2个含孤对电子的杂化轨道对成键电子对的排斥的结果使键角不是109°
28′,而是104.5°
第三课时
【学习目标】:
1.配位键、配位化合物的概念2.配位键、配位化合物的表示方法
1.配位键:
;
2.配位化合物(简称):
1.配位键:
由一个原子(如A)单方面提供而跟另一个原子(如B)的
键叫做配位键,常用符号AB表示。
配位键的成键条件是:
给予体有,接受体有。
2.配位化合物:
通常把(或原子)与某些(称为配位体)以键结合形成的化合物称为配位化合物。
3.配合物的组成:
在配合物[Co(NH3)6]Cl3中,中心离子是,配位体是,中心离子和配位体构成了配合物的,通常把它们放在括号内,内界中配位体总数称为。
Cl-称为,内外界之间形成了键,在水中电离。
4.配合物的命名:
[Zn(NH3)2]SO4内界名称为(Ⅱ),K3[Fe(CN)