届高考化学一轮复习 第十一章 化学实验检测一Word下载.docx
《届高考化学一轮复习 第十一章 化学实验检测一Word下载.docx》由会员分享,可在线阅读,更多相关《届高考化学一轮复习 第十一章 化学实验检测一Word下载.docx(14页珍藏版)》请在冰豆网上搜索。
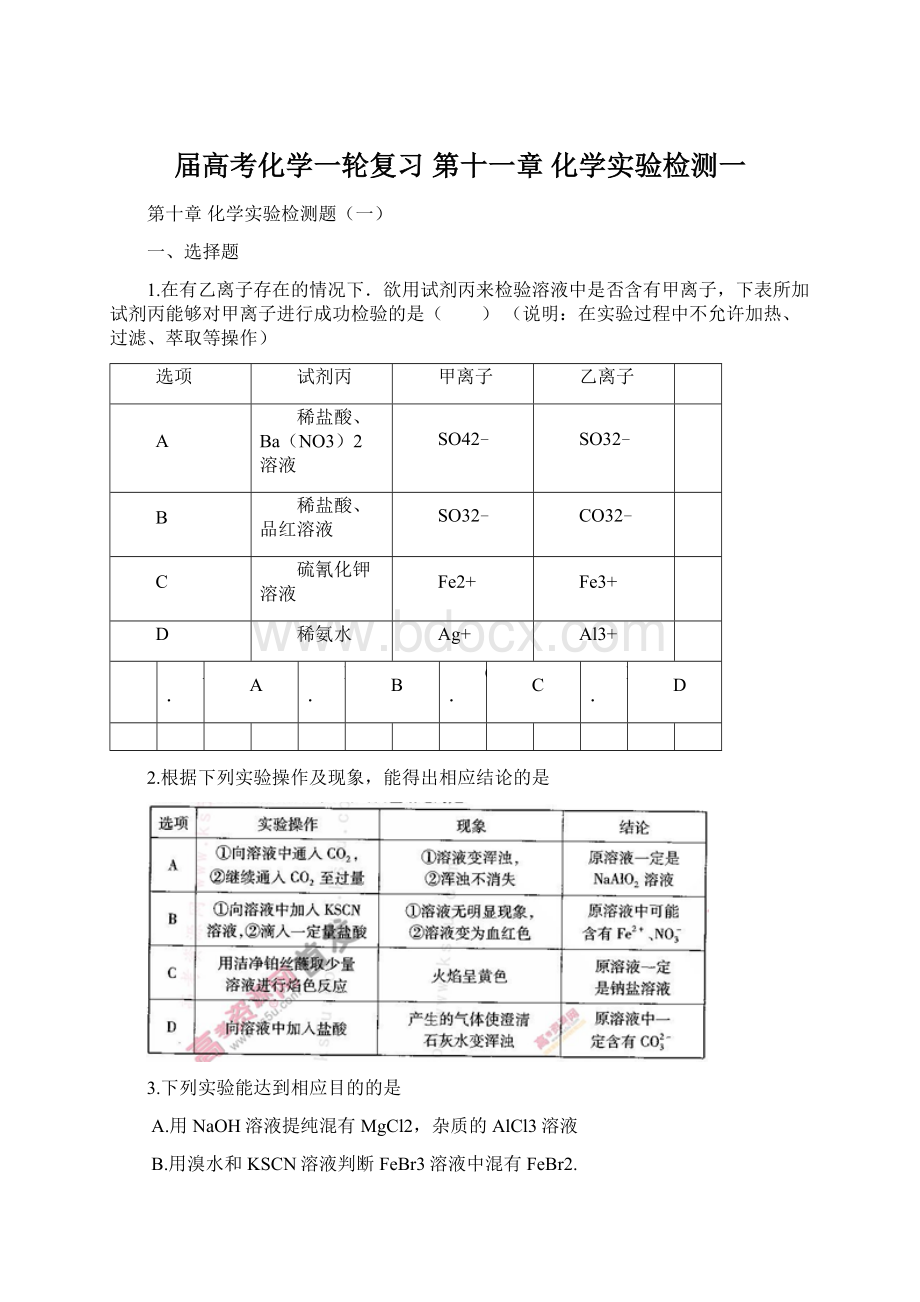
Fe3+
D
稀氨水
Ag+
Al3+
A.
B.
C.
D.
2.根据下列实验操作及现象,能得出相应结论的是
3.下列实验能达到相应目的的是
A.用NaOH溶液提纯混有MgCl2,杂质的AlCl3溶液
B.用溴水和KSCN溶液判断FeBr3溶液中混有FeBr2.
C.用Ba(0H)2溶液可鉴别
四种溶液
D.用溶液和硝酸检验亚硫酸钠固体是否变质
4.已知氨气极易溶于水,而难溶于有机溶剂CCl4,下列不能作NH3尾气吸收装置的是( )
B.
C.
D.
5.下列有关实验的叙述,正确的是( )
A.用广泛pH试纸测得氯水的pH为2
B.用托盘天平称取10.50g干燥的NaCl固体
C.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏高
D.制备Fe(OH)2时,向FeSO4溶液中滴入NaOH溶液时,胶头滴管不能伸入液面以下
6.下列各图所示装置的气密性检查中,一定漏气的是( )
7.下列有关实验装置进行的相应实验,能达到实验目的是( )
A.用图1装置制取并收集干燥纯净的NH3
B.用图2所示装置可除去NO2中的NO
C.用图3所示装置可分离CH3C
OOC2H5和饱和碳酸钠溶液
D.用图4装置制备Fe(OH)2并能较长时间观察其颜色
8.某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。
某校课外兴趣小组以两条途径分别对X进行如下实验探究。
下列有关说法不正确的是:
A.由工可知X中一定存在Fe2O3、Cu
B.无法判断混合物中是否含有Al2O3
C.1.92g固体成分为Cu
D.原混合
物中m(Fe2O3):
m(Cu)=1:
1
9.以下实验方案可以从海洋生物中提取具有抗肿瘤活性的天然产物:
下列说法错误的是
A.步骤
(1)需要用到玻璃棒B.步骤
(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚D.步骤(4)需要用到温度计
10.关于下列各实验装置的叙述中,不正确的是
A.图①可用于实验室制备少量Cl2或NH3
B.可用从a处加水的方法检验装置②的气密性
C.实验室也可以用装置③收集HCl气体
D.装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出
11.下列关于仪器使用的说法正确的是
A.在量取液体后,量筒中残留的液体要用蒸馏水洗涤并转入相应容器
B.熔融纯碱、烧碱时,不能选用石英坩埚,应该选用铁坩埚
C.蒸发结晶实验中,蒸发皿应放在石棉网上加热
D.在测量或监测温度时,温度计水银球碰到容器内壁不影响测量结果
12.下列实验方
案不能达到实验目的的是()
A.图A装置用Cu和浓硝酸可制取NOB.图B装置可用于实验室制备Cl2
C.图C装置可用于实验室制取乙酸乙酯D.图D装置可用于实验室分离CO和CO2
13.下列实验不能达到目的的是()
A.向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体
B.只用少量水就可鉴别Na2CO3和NaHCO3固体
C.用FeSO4、NaOH和盐酸等试剂在空气中可以制备纯净的FeCl3溶液
D.用NaOH溶液和盐酸
可除去MgCl2溶液中混有的AlCl3
14.下述实验能达到预期目的是( )
编号
实验内容
实验目的
取两只试管,分别加入4mL0.01mol/LKMnO4酸性溶液,然后向一只试管中加入0.1mol/LH2C2O4溶液2mL,向另一只试管中加入0.1mol/LH2C2O4溶液
4mL,记录褪色时间
证明草酸浓度越大反应速率越快
向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅
证明Na2CO3溶液中存在水解平衡
向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀
证明在相同温度下,溶解度Mg(OH)2>Fe(OH)3
测定等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者
较大
证明非金属性S>C
15.下列有关实验的叙述正确的是( )
A.用HF溶液可以除去硅晶体中含有的少量二氧化硅晶体
B.向两份Fe3O4固体中分别加入HCl溶液与HI溶液,二者反应现象一样
C.向某溶液中滴加NaOH溶液后又加入酚酞,溶液呈红色,说明原溶液中含有NH4+
D.向某溶液中加入足量的稀HNO3溶液,所得气体能使澄清石灰水变浑浊,证明该溶液中存在CO32﹣或HCO3﹣
二、非选择题
16.铝土矿的主要成分是Al2O3,含有Fe2O3、SiO2等杂质,按下列操作从铝土矿中提取Al2O3.回答下列问题:
(1)沉淀物的化学式分别是:
a ____;
d ____;
f ____;
(2)写出加入过量NaOH溶液时所发生主要反应的离子方程式 ___________ 、 ___________ .
(3)写出通入气体B(过量)时溶液C中发生反应的离子方程式 ___________ 、 ___________ .
(4)气体B能否改用试剂A代替?
为什么?
____, ___________ .
17.现有A、B、C、D、E、F六种化合物,已知它们的阳离子有K+,Ag+,Ca2+,Ba2+,Fe2+,Al3+,阴离子有Cl﹣,OH﹣,CH3COO﹣,NO3﹣,SO42﹣,CO32﹣,现将它们分别配成0.1mol•L﹣1的溶液
,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色.
根据上述实验现象,回答下列问题:
(1)实验②
中反应的化学方程式是_____________________________________________
________________________________________
(2)E溶液是____________,判断依据是_______________________________________
______________________________________________________________;
(3)写出下列四种化合物的化学式:
A___________、C__________ 、D_____________ 、F_________________.
18.无水AlCl3可用作有机合成的催化剂、食品膨松剂等。
工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下图所示流程进行一系列反应来制备无水AlCl3。
(1)氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则AlCl3是晶体,其结构式为。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式是。
(3)冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反应的离子方程式为:
。
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是:
(5)AlCl3产品中Fe元素含量直接影响其品质,为测定产品中Fe元素的含量,现称取16.25g无水AlCl3产品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重残留固体质量为0.32g。
则产品中Fe元素的含量为:
19.镁合金是重要的民用和航空材料,镁作为一种强还原剂,还用于钛、镀和铀的生产,氯酸镁[
]常用作催熟剂、除草剂等。
(1)氧化镁的电子式为________。
(2)写出镁与TiCl4在高温条件下制取钛的化学方程式:
____________________。
(3)从海水中提取金属镁用到的主要化学药品有________________。
(4)某研究小组同学在实验室用卣块制备少量
,其流程如下:
已知:
I卤块主要成分为
,含有MgSO4、FeCl2等杂质。
Ⅱ可选用的试剂:
H2O2,稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
1加入BaCl2溶液的目的是____________。
②步骤X中需将Fe2+转化为Fe3+,所选的试剂为__________。
③Mg(ClO3)2加入到含有KSCN的FeSO4酸性溶液中立即出现红色,写出相关反
应的离子方程式:
________________________________________.
20.常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
(1)写出该反应的反应方程式:
;
并指明该氧化还原反应的还原剂是 ,氧化剂是 .
(2)实验前必须对整套装置进行气密性检查,操作方法是
.
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;
烧瓶底部放置了几片碎瓷片,碎瓷片的作用是 .
(4)酒精灯和酒精喷灯点燃的顺序是 ,为什么?
(5)干燥管中盛装是的物质是 ,作用是 .
(6)试管中收集气体是 ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行 ,方法是
.
这一操作的目的是 .
参考答案
1.B
解:
A.硝酸根和氢离子在一起具有稀硝酸的性质,有强氧化性,可将SO32﹣氧化为SO42﹣,与钡离子结合生成硫酸钡沉淀,无法确定是否含有SO42﹣,故A错误;
B.SO32﹣与稀盐酸反应生成二氧化硫,二氧化硫能使品红溶液褪色;
CO32﹣与稀盐酸反应生成二氧化碳,二氧化碳不能使品红溶液褪色;
故可确定含有SO32﹣,故B正确;
C.KSCN与Fe3+反应,溶液呈红色,不能判断是否含有Fe2+,故C错误;
D.过量氨水与Ag+反应产生银氨溶液,与Al3+反应只生成Al(OH)3沉淀,无法确定是否含有Ag+,故D错误。
2.B3.C
4.C
解析:
A.氨气不溶于四氯化碳,该装置可以防止倒吸,可用于吸收氨气,故A错误;
B.使用倒置的漏斗,可以防止倒吸,可用于吸收氨气尾气,故B错误;
C.氨气极易溶于水,不能直接将导管插入水中,否则容易发生倒吸,故C正确;
D.球形漏斗可以防止倒吸,可用于吸收氨气尾气,故D错误;
故选C.
5.C
A.氯水中的次氯酸有强氧化性,应用pH计,故A错误;
B.托盘天平只能准确到0.1g,所以用托盘天平称取10.5g的干燥的NaCl固体,不能称量10.50g,故B错误;
C.定容