八年级科学下册期末复习第3章空气与生命第三节化学反方程式练习题Word格式.docx
《八年级科学下册期末复习第3章空气与生命第三节化学反方程式练习题Word格式.docx》由会员分享,可在线阅读,更多相关《八年级科学下册期末复习第3章空气与生命第三节化学反方程式练习题Word格式.docx(10页珍藏版)》请在冰豆网上搜索。
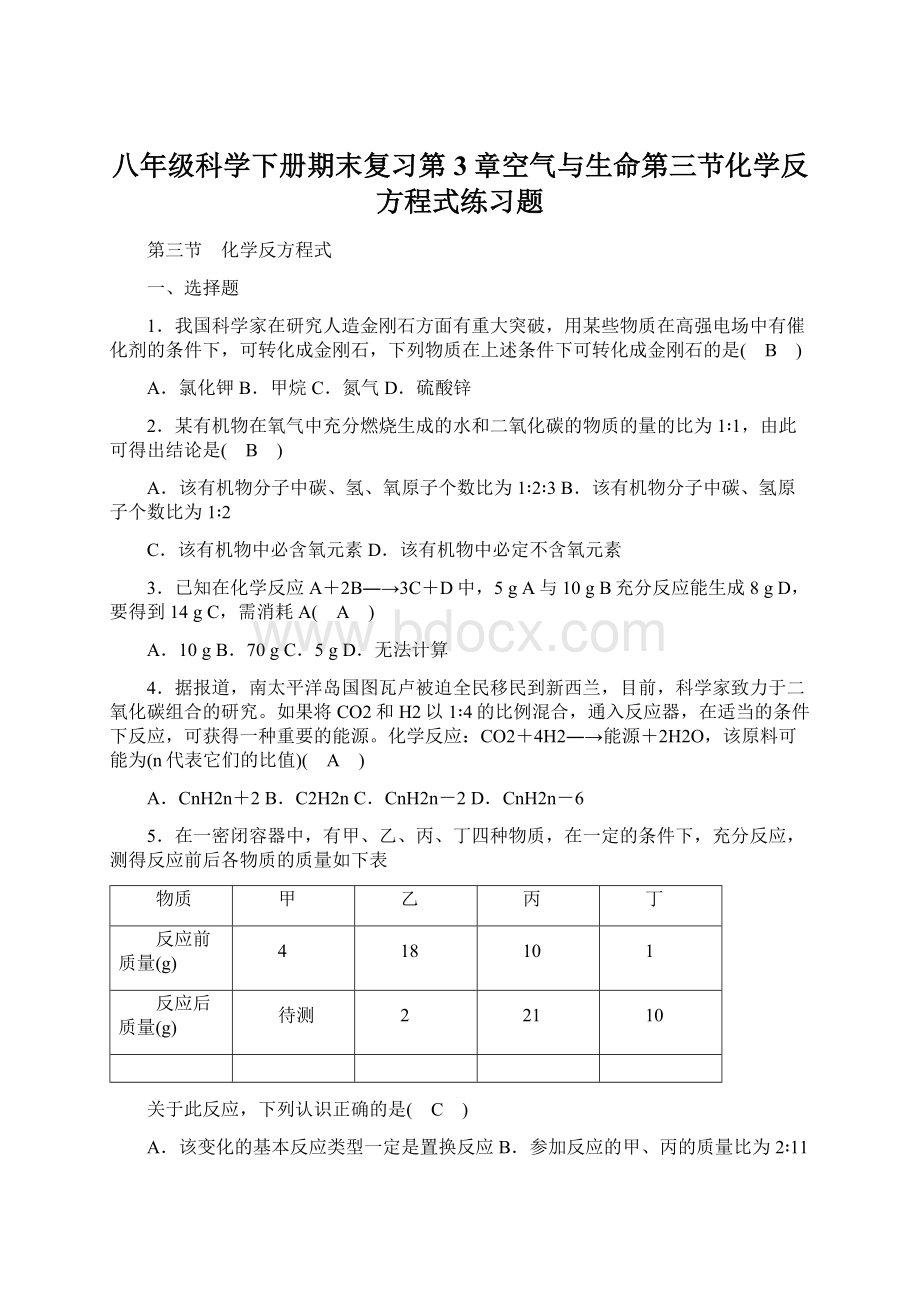
物质
甲
乙
丙
丁
反应前质量(g)
4
18
10
1
反应后质量(g)
待测
2
21
关于此反应,下列认识正确的是( C )
A.该变化的基本反应类型一定是置换反应B.参加反应的甲、丙的质量比为2∶11
C.丙、丁的质量比一定为11∶9D.甲反应后的质量为8g
6.英国科学家成功研制出二氧化硅纳米纤维,制造超纯SiO2的反应原理为SiCl4(气)+O2(气)SiO2(固)+nCl2(气)。
下列说法不正确的是( A )
A.硅是地壳中含量最高的非金属元素B.该化学方程式中n=2
C.该反应需要吸收大量热量D.反应前后原子总数不发生变化
7.关于2H2O2H2↑+O2↑的读法,正确的是( D )
A.水在通电条件下,分解为氢元素和氧元素B.每2个水分子等于2个氢分子和氧分子
C.水在通电条件下,分解为氢气加氧气D.水在通电条件下,分解为氢气和氧气
8.如图3-12-2四位同学正在讨论某一个化学方程式表示的意义,根据他们描述的内容,试判断他们所指的化学方程式是( C )
图3-12-2
A.S+O2SO2B.2H2+O22H2O
C.2CO+O22CO2D.CH4+O2CO2+2H2
9.泡沫灭火器是利用碳酸钠与盐酸反应产生大量的二氧化碳来灭火的,其反应为□Na2CO3+□HCl===□NaCl+□CO2↑+□H2O,各物质的化学计量数依次为( D )
A.2、3、1、1、2B.1、2、1、1、2C.2、1、1、1、2D.1、2、2、1、1
10.下列化学方程式完全正确的是( C )
A.天然气燃烧CH4+2O2===CO2+2H2O
B.处理污水中的硫酸Ca(OH)2+H2SO4===CaSO4+H2O
C.二氧化碳气体的检验CO2+Ca(OH)2===CaCO3↓+H2O
D.稀硫酸除铁锈2H2SO4+Fe2O3===2FeSO4+2H2O
11.在托盘天平的两个托盘上各放一只烧杯,两只烧杯中都盛有过量的相同质量分数的盐酸,天平两边保持平衡,此时向左边烧杯中加入5.6gCaO,若使天平两边再次保持平衡,需向右边烧杯中加入CaCO3的质量为( C )
A.5.6gB.17.6gC.10gD.11.2g
12.“西气东输”使我们浙江地区的很多居民家都用上了天然气。
液化气的主要成分是C3H8,其燃烧的化学方程式是C3H8+5O23CO2+4H2O,天然气燃烧的化学方程式是CH4+2O2CO2+2H2O。
现有一同学家有一套以液化气为燃料的灶具,要改成以天然气为燃料的灶具。
你认为应采取的正确措施是( C )
A.同时减少空气和天然气的进入量
B.同时增加空气和天然气的进入量
C.增加天然气的进入量或减少空气的进入量
D.减少天然气的进入量或增加空气的进入量
13.下列叙述正确的是( D )
A.5gMg与3gO2反应可生成8gMgOB.4gMg与4gO2反应可生成8gMgO
C.3.2gMg与4.8gO2反应可生成8gMgOD.6gMg与4gO2反应可生成10gMgO
图3-12-3
14.在化学反应2A+B2===2AB中,A与B2反应的质量关系如图3-12-3所示,现将6gA和8gB2充分反应,则生成AB的质量是( C )
A.9gB.11gC.12gD.14g
15.可以用加热氯酸钾和二氧化锰混合物的方法在实验室制取氧气。
图3-12-4是反应生成氧气和氯化钾的质量与反应时间的关系坐标图,其中合理的是( C )
图3-12-4
16.加热31.6gKMnO4,当得到3gO2时剩余固体的成分是( D )
A.K2MnO4和MnO2B.KMnO4和MnO2
C.KMnO4和K2MnO4D.KMnO4、K2MnO4和MnO2
17.一定质量的氯酸钾与二氧化锰的混合物,加热一段时间后,二氧化锰的含量由a%增加到b%,则产生的氧气占原混合物质量的百分比为( B )
A.(1-)×
100%B.(1-)×
100%
C.(1+)×
100%D.(1+)×
图3-12-5
18.某同学按如图3-12-5装置做质量守恒定律的探究实验,他的做法是:
第一步,将装稀盐酸和套有气球(气球中装有Na2CO3粉末)的锥形瓶放在托盘天平的左侧托盘上,向右盘中加砝码调至天平平衡;
第二步,将气球中的Na2CO3粉末加入锥形瓶中,充分反应后,天平所处的状态是( C )
A.天平仍平衡B.天平指针向左偏转
C.天平指针向右偏转D.无法确定
图3-12-6
19.图3-12-6中反映了某化学反应各物质质量与时间的关系,下列描述正确的是( C )
A.该反应是复分解反应
B.丁是该反应的催化剂
C.该反应的化学方程式可表示为:
乙―→甲+丙
D.t1℃时,丙的质量一定等于甲、乙的质量之和
20.某物质充分燃烧的产物是CO2和H2O,为了确定该物质的组成,某小组设计了如图3-12-7所示实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略)。
称取0.84g待测物完全燃烧后,称得D装置增重1.08g,E装置增重2.64g。
则下列推断正确的是( B )
图3-12-7
A.该物质一定含有C、H元素,没有氧元素
B.该物质一定含有C、H、O元素
C.用充有空气的储气球代替装置A、B更有利于实验的进行
D.B装置的有无对实验结果没有影响
21.某组成为CaHbNc(a,b,c为正整数)的ABS工程树脂可通过下面的反应制得:
C3H3N+C4H6+ C8H8CaHbNc(未配平)
丙烯腈 1,3丁二烯 苯乙烯 ABS
则参加反应的原料中丙烯腈和1,3丁二烯的分子个数之比为( A )
A.B.C.D.无法确定
22.一种焰火火药中所含的Cu(NO3)2在燃放时产生绿色火焰,发生如下反应:
2Cu(NO3)22CuO+O2↑+4X↑,其中X是一种污染空气的有毒气体,依据质量守恒定律,推测X应是( A )
A.NO2B.NOC.N2O5D.N2O
23.某些科学家对3个互相联系的化学反应:
①3FeCl2+4H2OFe3O4+6HCl+H2,②Fe3O4+Cl2+6HCl3FeCl3+3H2O+O2,③3FeCl3===3FeCl2+Cl2很感兴趣,他们想利用这三个反应来制取一种很有意义的物质是( A )
A.H2B.O2C.Cl2D.HCl
24.“绿色化学”是当今社会提出的一个新概念。
在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得的产物,即原子的利用率为100%。
在用C3H4(丙炔)合成C5H8O2(2�甲基丙烯酸甲酯)的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要的其他反应物是( A )
A.CO和CH3OHB.CO2和H2O
C.CO和C2H5OHD.CH3OH和H2
25.(双选)为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图3-12-8所示:
图3-12-8
下列说法正确的是( BD )
A.图中表示化合物的是“”
B.该反应类型为置换反应
C.该反应中反应物两种分子的个数比为3∶1
D.反应前后原子的种类和数目保持不变
26.我们常用原子利用率来衡量化学反应过程的原子经济性,其计算公式为:
原子利用率=×
100%,下面是联合工艺法制备新型自来水消毒剂ClO2的反应原理:
①电解氯化钠溶液NaCl+3H2ONaClO3+3H2↑
②氢气与氯气合成氯化氢
③生成二氧化氯2NaClO3+4HCl===2NaCl+2ClO2↑+Cl2↑+2H2O
此方法的原子利用率最大为( D )
A.37.6%B.53.6%C.62.2%D.94.4%
二、填空题
27.a.乙醇是一种清洁能源.乙醇的燃烧可发生以下两个反应:
①C2H6O+3O22CO2+3H2O ②aC2H6O+5O22CO2+2CO+6H2O
试填空:
(1)反应②中的化学计量数a=2。
(2)反应①(选填化学方程式的序号)属于完全燃烧,产物无毒性。
b.乙醇汽油就是在汽油中加入适量的乙醇(C2H5OH)。
(1)关于乙醇汽油的说法错误的是B(填序号)。
A.乙醇属于有机物B.乙醇属于不可再生能源
C.使用乙醇汽油可减少大气污染D.使用乙醇汽油可节省石油资源
(2)工业上利用石油中各成分的沸点不同,分离制备汽油、煤油等产品,属于物理(选填“物理”或“化学”)变化。
(3)汽油和乙醇汽油完全燃烧后产物相同。
则汽油中一定含有C和H(填元素符号)。
(4)汽车尾气中含有CO、NO,一种新型催化剂能使二者发生反应。
生成两种常见的无毒气体,分别是CO2、N2(填化学式)。
三、解答题
28.合成氨工业生产中所用的α�Fe催化剂的主要成分是FeO、Fe2O3。
(1)当催化剂中FeO与Fe2O3的质量之比为9∶20时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为多少?
(用小数表示,保留两位小数)
(2)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳,发生如下反应:
2Fe2O3+C4FeO+CO2↑。
为制得这种活性最高的催化剂,应向480gFe2O3粉末中加入碳多少克?
(1)0.72
(2)6g
能力提升
图3-12-9
1.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图3-12-9所示,下列说法正确的是( C )
A.丁是该反应的催化剂
B.该反应的基本类型是分解反应
C.该反应中乙、丙的质量比为3∶17
D.该反应中甲、丙的质量比为7∶10
2.根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:
①CaBr2+H2OCaO+2HBr ②2HBr+HgHgBr2+H2↑
③HgBr2+CaOHgO+CaBr2 ④2HgO2Hg+O2↑
该方案的目的是制备( C )
A.HBrB.CaOC.H2D.Hg
3.将一严重锈蚀而部分变成铜绿的铜块研磨成粉末,在空气中充分灼烧成氧化铜,固体质量的变化情况可能是( C )
①增重40% ②增