学年九年级化学下册专题复习四科学探究题练习新版鲁教版Word格式.docx
《学年九年级化学下册专题复习四科学探究题练习新版鲁教版Word格式.docx》由会员分享,可在线阅读,更多相关《学年九年级化学下册专题复习四科学探究题练习新版鲁教版Word格式.docx(11页珍藏版)》请在冰豆网上搜索。
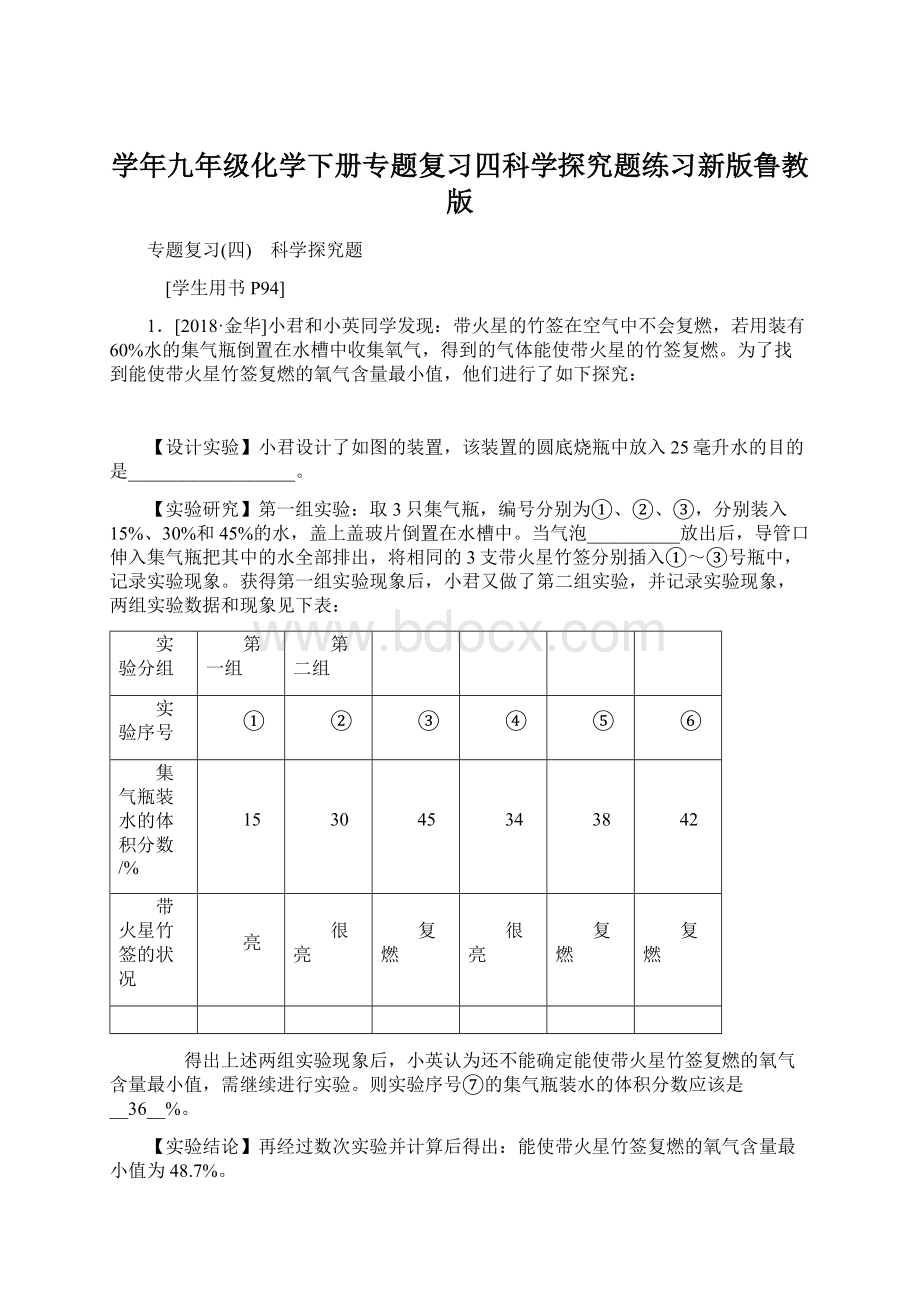
15
30
45
34
38
42
带火星竹签的状况
亮
很亮
复燃
得出上述两组实验现象后,小英认为还不能确定能使带火星竹签复燃的氧气含量最小值,需继续进行实验。
则实验序号⑦的集气瓶装水的体积分数应该是__36__%。
【实验结论】再经过数次实验并计算后得出:
能使带火星竹签复燃的氧气含量最小值为48.7%。
【继续探究】小君认为采用该方法收集的氧气中含有一定量的水蒸气,请你提出实验改进的措施__________________。
2.[2018·
梧州]梧州市某中学化学兴趣小组的同学查资料知道,乙醇(分子式为C2H6O)俗称酒精,通常情况下化学性质稳定,在一定条件下能与氧气反应。
现对乙醇与氧气反应进行探究。
探究活动一
同学们把绕成螺旋状的红色铜丝在酒精灯的外焰上灼烧到通红,取出铜丝,发现表面变黑,趁热插入装有无水乙醇的试管中(如图),铜丝很快变为红色,并闻到刺激性气味。
重复上述操作多次,得到A溶液;
经称量,实验前后铜丝质量不变。
铜丝灼烧后生成的黑色物质是__________,铜丝除了给反应加热外,还起到_______________作用。
【提出问题】生成的激性气味的气体是什么?
【猜想与假设】有同学提出刺激性气味的气体可能是:
猜想一:
SO2;
猜想二:
CO2;
猜想三:
醋酸(C2H4O2)。
【讨论与结论】同学们讨论后发表看法:
小吴认为猜想一不正确,判断的依据是___________。
小周认为猜想二也不正确,判断的依据是______________。
小施认为猜想三有可能正确,原因是醋酸具有挥发性,并有刺激性气味。
探究活动二
小施同学设计实验验证后,发现猜想三也不正确。
请补充完成小施的实验操作和现象:
取少量A溶液加入试管中,然后______________。
【讨论与结论】
老师提示这种刺激性气味气体来源于易挥发的B物质,其相对分子质量为44,且含有C、H、O三种元素(氢元素的质量分数不超过20%),由此可推知物质B的分子式为________________。
【拓展活动】
(1)同学们再取少量A溶液加入试管中,加少量无水硫酸铜固体,变蓝色(已知:
乙醇、B物质遇无水硫酸铜均不显蓝色),说明乙醇在一定条件下与氧气的反应有___________生成。
(2)乙醇在微生物(醋酸菌)作用下与氧气反应能生成醋酸,写出该反应的化学方程式:
____________________________。
3.[2018·
宿迁]实验课上,老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种,为确定该粉末的成分,同学们进行了如下探究,请你参与其中并回答问题。
【提出猜想】
甲组:
铜粉;
乙组:
氧化铁粉末;
丙组:
________________________。
【设计实验】
方案1:
取少量红色粉末放入试管中,滴加足量的_________________(从下列试剂中选择:
氯化钠溶液、稀盐酸、氢氧化钠溶液)振荡,若甲组猜想正确,则实验现象为__________________。
方案2:
取8g红色粉末放入硬质玻璃管中,先通入CO,然后用酒精喷灯加热一段时间(实验装置如图1所示),停止加热并继续通入CO至装置冷却。
图1)
若乙组或丙组猜想正确,则硬质玻璃管内发生反应的化学方程式是_____________。
实验时要先通CO再加热的目的是__________________。
【数据处理】等装置完全冷却到室温,称量硬质玻璃管内剩余固体质量为mg。
若乙组猜想正确,则m的取值范围是____________。
【实验反思】图1虚线框内的装置是用于吸收CO2,并收集CO,请从图2(广口瓶内均为氢氧化钠溶液)中选择最合适的装置____________(填序号)。
图2)
4.实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过询问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
【进行猜想】
猜想I:
原溶液的溶质是NaCl;
猜想II:
原溶液的溶质是NaOH;
猜想III:
原溶液的溶质是Na2CO3;
猜想IV:
原溶液的溶质是NaHCO3。
【查阅资料】常温下,有关物质的相关信息如下表:
物质
NaCl
NaOH
Na2CO3
NaHCO3
常温下的溶解度/g
36
109
21.5
9.6
常温下稀溶液的pH
7
13
11
9
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为________。
【进行实验】
(1)取少量样品,测得溶液的pH>7,则原溶液的溶质肯定不是______。
(2)同学们另取样品又进行了如下实验,实验过程如下:
①生成白色沉淀A的化学方程式为_______________。
②通过实验可以判断样品无色溶液中含有的溶质有__________。
【获得结论】实验完成后,最终得到的结论:
原瓶中的溶质是___________,且已变质。
5.[2018·
安徽]“蓝瓶子”实验是一个有趣的化学振荡实验:
盛有氢氧化钠、亚甲蓝(C16H18N3SCl)、葡萄糖混合液的试管,经振荡、静置后溶液颜色会出现反复变化(如图1)。
某兴趣小组开展如下探究,回答下列问题。
(1)混合液中属于人类基本营养物质的有水和____________。
(2)小明对振荡实验后溶液变蓝的原因进行如下猜想:
①溶液中溶入CO2;
②溶液中溶入O2;
③溶液中溶入__________(填化学式)。
(3)小红利用图2装置,从A端吹入呼出的气体,混合液由无色变为蓝色,由此__________(填“能”或“不能”)得出猜想①正确,原因是____________。
(4)为探究猜想②,利用图2装置设计实验方案:
____________。
6.[2018·
安顺]氢化钙固体是登山运动员常用的能源提供剂。
某探究小组的同学通过查阅资料得知:
氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
NaOH;
NaOH、Ca(OH)2
NaOH、Na2CO3;
猜想四:
NaOH、Na2CO3、Ca(OH)2。
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因:
【实验验证】
实验
现象
结论
(1)取少量滤液,向其中滴入少量碳酸钠溶液
无明显现象
猜想_______不成立
(2)另取少量滤液,向其中加入足量稀盐酸
______
猜想三成立
【反思与拓展】
(1)写出氢化钙(CaH2)与水反应的化学方程式:
___________。
(2)若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和_________。
(3)登山运动员携带CaH2作为能源提供剂与携带氢气相比,其优点是__________(写一条即可)。
7.过碳酸钠(化学式为2Na2CO3·
3H2O2)俗称固体双氧水,溶于水可看作是Na2CO3溶液和H2O2溶液混合。
为了方便保存,过碳酸钠样品可能添加少量的MgSO4和硅酸镁中的一种或两种作为稳定剂。
已知:
①双氧水可用于供氧、消毒和漂白;
②硅酸镁不溶于水。
(1)过碳酸钠的用途不合理的是_________。
A.鱼池供氧剂B.消毒剂
C.干燥剂D.漂白剂
(2)取少量过碳酸钠样品于烧杯中,加入足量蒸馏水,有不溶于水的固体产生。
判断样品中__________(填“可能”或“一定”)有硅酸镁。
(3)利用实验室限选试剂,设计实验确定该样品中是否添加少量的MgSO4。
限选试剂:
稀盐酸、稀H2SO4、BaCl2溶液、蒸馏水、AgNO3溶液。
实验操作
实验目的、预期现象或结论
步骤1:
取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤
这样做是为了除去__________
步骤2:
取少量步骤1所得的滤液于试管中,加入__________,振荡后静置
现象:
________
步骤3:
取少量步骤2所得的溶液于试管中,加入__________,振荡后静置
________,说明样品中有MgSO4
__________,说明样品中没有MgSO4
8.[2018·
广安]某实验小组在做“用澄清石灰水检验二氧化碳”的实验时,发现一个有趣的实验现象:
试管中浑浊现象为何消失?
实验小组的同学对此实验进行了下列探究活动:
(1)根据已学知识,实验小组对CO2使澄清石灰水变浑浊的现象作出了合理的解释,其化学方程式为______________。
(2)
【查阅资料】
①碳酸盐一般不溶于水。
如碳酸钙不溶于水。
②碳酸钙能与二氧化碳、水反应生成碳酸氢钙[Ca(HCO3)2],碳酸氢钙易溶于水。
③碳酸氢钙受热易分解,生成碳酸钙、二氧化碳、水。
从物质组成角度分类,碳酸氢钙应属于___________。
A.氧化物B.酸
C.碱D.盐
写出碳酸氢钙受热分解的化学方程式:
________________。
(3)
【提出问题】碳酸氢钙能与哪些物质反应呢?
(4)
【假设与猜想】
能与盐酸反应;
猜想Ⅱ:
能与氢氧化钠反应;
……
(5)
【设计实验并验证】
实验步骤
实验现象
实验一:
取丙中少量液体于试管中,滴加稀盐酸
有______生成
猜想I成立
实验二:
取丙中少量液体于试管中,滴加氢氧化钠溶液
有白色沉淀生成
猜想II成立
实验三:
取丙中少量液体于试管中,加热
澄清液体又变浑浊
验证了资料描述
根据验证实验写出碳酸氢钙与盐酸反应的化学方程式:
(6)
【讨论与反思】
该实验小组在实验中发现问题,并对问题进行不断探究。
他们不但发现了新的物质,还了解了它的一些性质,并对生活中煮沸可以降低水的硬度、水垢的形成以及自然界中溶洞与钟乳石的形成有了更进一步的认识。
9.[2018·
泰州]为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
Ⅰ.20℃时,几种物质在水中的溶解度见下表:
Ca(OH)2
Ba(OH)2
溶解度/g