化学化学反应速率与化学平衡的专项培优练习题及答案1Word文件下载.docx
《化学化学反应速率与化学平衡的专项培优练习题及答案1Word文件下载.docx》由会员分享,可在线阅读,更多相关《化学化学反应速率与化学平衡的专项培优练习题及答案1Word文件下载.docx(17页珍藏版)》请在冰豆网上搜索。
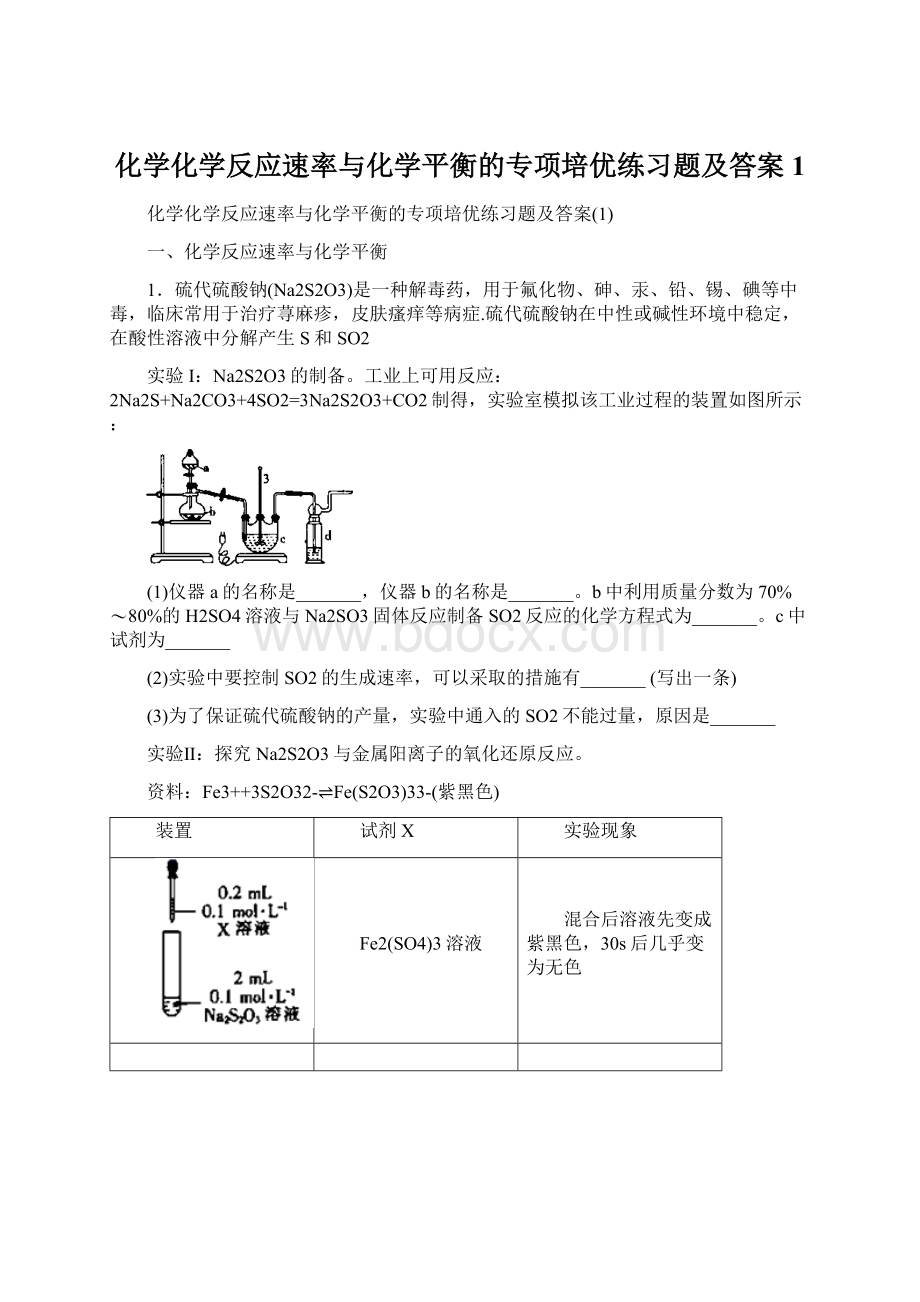
资料:
Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)
装置
试剂X
实验现象
Fe2(SO4)3溶液
混合后溶液先变成紫黑色,30s后几乎变为无色
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。
从化学反应速率和平衡的角度解释实验Ⅱ的现象:
_______
实验Ⅲ:
标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:
用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294g∙mol-1)0.5880g。
平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:
6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32-=2I-+S4O62-,三次消耗Na2S2O3溶液的平均体积为25.00mL,则所标定的硫代硫酸钠溶液的浓度为_______mol∙L-1
【答案】分液漏斗蒸馏烧瓶硫化钠和碳酸钠的混合液调节酸的滴加速度若SO2过量,溶液显酸性.产物会发生分解加入铁氰化钾溶液.产生蓝色沉淀开始生成Fe(S2O3)33-的反应速率快,氧化还原反应速率慢,但Fe3+与S2O32-氧化还原反应的程度大,导致Fe3++3S2O32-⇌Fe(S2O3)33-(紫黑色)平衡向逆反应方向移动,最终溶液几乎变为无色0.1600
【解析】
【分析】
【详解】
(1)a的名称即为分液漏斗,b的名称即为蒸馏烧瓶;
b中是通过浓硫酸和Na2SO3反应生成SO2,所以方程式为:
;
c中是制备硫代硫酸钠的反应,SO2由装置b提供,所以c中试剂为硫化钠和碳酸钠的混合溶液;
(2)从反应速率影响因素分析,控制SO2生成速率可以调节酸的滴加速度或者调节酸的浓度,或者改变反应温度;
(3)题干中指出,硫代硫酸钠在酸性溶液中会分解,如果通过量的SO2,会使溶液酸性增强,对制备产物不利,所以原因是:
SO2过量,溶液显酸性,产物会发生分解;
(4)检验Fe2+常用试剂是铁氰化钾,所以加入铁氰化钾溶液,产生蓝色沉淀即证明有Fe2+生成;
解释原因时一定要注意题干要求,体现出反应速率和平衡两个角度,所以解释为:
开始阶段,生成的反应速率快,氧化还原反应速率慢,所以有紫黑色出现,随着Fe3+的量逐渐增加,氧化还原反应的程度变大,导致平衡逆向移动,紫黑色逐渐消失,最终溶液几乎变为无色;
(5)间接碘量法滴定过程中涉及两个反应:
①;
②;
反应①I-被氧化成I2,反应②中第一步所得的I2又被还原成I-,所以①与②电子转移数相同,那么滴定过程中消耗的得电子总数就与消耗的失电子总数相同;
在做计算时,不要忽略取的基准物质重铬酸钾分成了三份进行的滴定。
所以假设c(Na2S2O3)=amol/L,列电子得失守恒式:
,解得a=0.1600mol/L。
2.用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:
KI在该反应中的作用:
H2O2+I-=H2O+IO-;
H2O2+IO-=H2O+O2↑+I-。
总反应的化学方程式是________________。
(2)资料2:
H2O2分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。
下列判断正确的是___________(填字母)。
a.加入KI后改变了反应的路径
b.加入KI后改变了总反应的能量变化
c.H2O2+I-=H2O+IO-是放热反应
(3)实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。
再加入CCl4,振荡、静置,气泡明显减少。
资料3:
I2也可催化H2O2的分解反应。
①加CCl4并振荡、静置后还可观察到___________,说明有I2生成。
②气泡明显减少的原因可能是:
i.H2O2浓度降低;
ii.________。
以下对照实验说明i不是主要原因:
向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。
A试管加入CCl4,B试管不加CCl4,分别振荡、静置。
观察到的现象是_____________。
(4)资料4:
I-(aq)+I2(aq)I3-(aq)K=640。
为了探究体系中含碘微粒的存在形式,进行实验:
向20mL一定浓度的H2O2溶液中加入10mL0.10mol·
L-1KI溶液,达平衡后,相关微粒浓度如下:
微粒
I-
I2
I3-
浓度/(mol·
L-1)
2.5×
10-3
a
4.0×
①a=__________。
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是________________。
【答案】2H2O22H2O+O2↑a下层溶液呈紫红色在水溶液中I2的浓度降低A试管中产生气泡明显变少;
B试管中产生气泡速率没有明显减小2c(I2)+c(I-)+3c(I3-)<0.033mol·
L-1
(1)H2O2+I-=H2O+IO-,H2O2+IO-=H2O+O2↑+I-,把两式加和,即可得到总反应的化学方程式。
(2)a.加入KI后,一步反应分为两步进行,也就是改变了反应的路径,a正确;
b.加入KI后,反应物和生成物的能量都没有改变,b不正确;
c.由图中可知,H2O2+I-=H2O+IO-是吸热反应,c不正确。
(3)①加CCl4并振荡、静置后还可观察到下层溶液呈紫红色,说明有I2生成。
ii.在水溶液中I2的浓度降低。
观察到的现象是H2O2溶液的浓度相同,但产生气泡的速率差异很大。
(4)①,由此可求出a。
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是原来溶液中c(I-)=,求出I-,I2,I3-中所含I的浓度和,二者比较便可得到结论。
(1)H2O2+I-=H2O+IO-,H2O2+IO-=H2O+O2↑+I-,把两式加和,即可得到总反应的化学方程式为2H2O22H2O+O2↑。
答案为:
2H2O22H2O+O2↑;
c.由图中可知,H2O2+I-=H2O+IO-的反应物总能量小于生成物总能量,所以该反应是吸热反应,c不正确。
a;
下层溶液呈紫红色;
在水溶液中I2的浓度降低;
A试管中产生气泡明显变少,B试管中产生气泡速率没有明显减小;
(4)①,由此可求出a=2.5×
10-3mol/L。
10-3;
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是原来溶液中,c(I-)=;
现在溶液中,I-,I2,I3-中所含I的浓度和为2c(I2)+c(I-)+3c(I3-)=2×
10-3+2.5×
10-3+3×
10-3=0.0195<
0.033,I不守恒,说明产物中还有含碘微粒。
2c(I2)+c(I-)+3c(I3-)<
0.033mol·
L-1。
【点睛】
在做探究实验前,要进行可能情况预测。
向H2O2溶液中加入KI溶液,待溶液变黄,则表明生成了I2,加入CCl4且液体分层后,发现气泡逸出的速率明显变慢,CCl4与H2O2不反应,是什么原因导致生成O2的速率减慢?
是c(H2O2)减小,还是c(I2)减小所致?
于是我们自然想到设计对比实验进行验证。
3.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图1、2所示的实验。
请回答相关问题。
(1)定性分析:
如图1可通过观察_______,定性比较得出结论。
有同学提出将FeCl3改为0.05mol/LFe2(SO4)3更为合理,其理由是_______。
(2)定量分析:
如图2所示,实验时均生成40mL气体,其它可能影响实验的因素均已忽略。
实验中需要测量的数据是_________。
(3)加入0.10molMnO2粉末于50mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如图3所示。
①写出H2O2在二氧化锰作用下发生反应的化学方程式________________。
②实验时放出气体的总体积是________mL。
③A、B、C、D各点反应速率快慢的顺序为:
___>___>___>___。
解释反应速率变化的原因___________________。
④H2O2的初始物质的量浓度是___________(请保留两位有效数字)。
【答案】产生气泡的快慢消除阴离子不同对实验的干扰产生40mL气体所需的时间2H2O22H2O+O2↑60DCBA随着反应的进行,H2O2浓度减小,反应速率减慢0.11mol/L
⑴该反应中产生气体,所以可根据生成气泡的快慢判断;
氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用;
硫酸钠和硫酸铜阴离子相同,可以消除阴离子不同对实验的干扰,答案为:
两支试管中产生气泡的快慢;
消除阴离子不同对实验的干扰;
⑵仪器名称分液漏斗,检查气密性的方法:
关闭分液漏斗的活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;
该反应是通过生成气体的反应速率分析判断的,所以根据v=知,需要测量的数据是产生40ml气体所需要的时间,答案为:
分液漏斗,关闭分液漏斗的活塞,将注射器活塞向外拉出一段,过一会后看其是否回到原位;
产生40ml气体所需要的时间。
⑶从曲线的斜率可排知,反应速率越来越小,因为反应速率与反应物浓度成正比,随着反应的进行,反应物浓度逐渐降低,反应速率逐渐减小;
①在二氧化锰作催化剂条件下,双氧水分解生成水和氧气,反应方程式为:
2H2O22H2O+