高考化学二轮复习讲义第十二讲 常见无机物的相互转化文档格式.docx
《高考化学二轮复习讲义第十二讲 常见无机物的相互转化文档格式.docx》由会员分享,可在线阅读,更多相关《高考化学二轮复习讲义第十二讲 常见无机物的相互转化文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
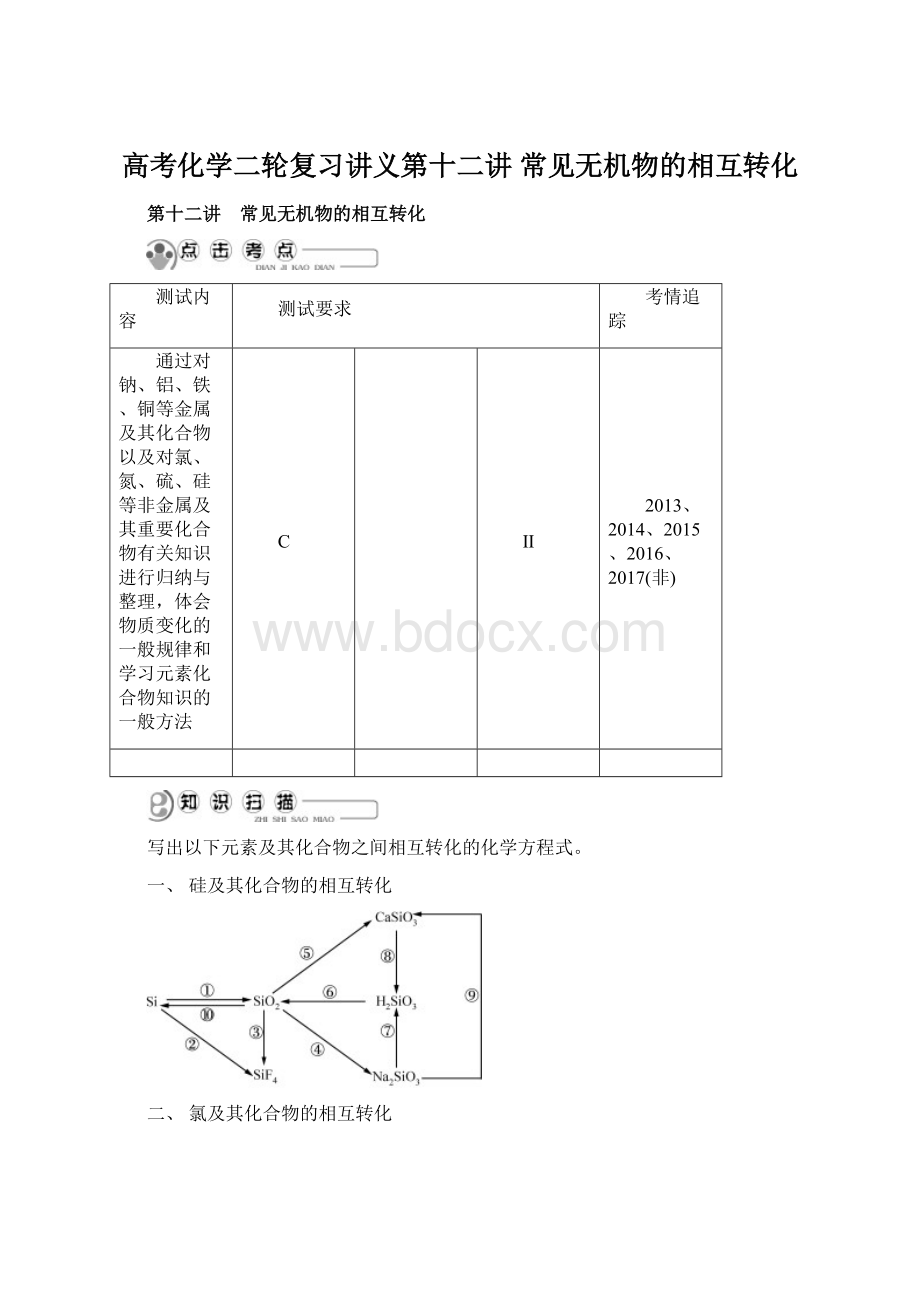
六、铝及其化合物的相互转化
七、铁及其化合物的相互转化
常见无机物的相互转化常以框图题形式考查。
解这类题首先要熟悉有关物质的性质及其反应,其次还要会正确使用化学用语表达问题。
其解题程序可概括为:
(1)抓题眼。
所谓题眼就是特征物质和特征现象,如使湿润红色石蕊试纸变蓝色的气体——氨气;
淡黄色粉末——Na2O2;
红棕色气体——NO2;
焰色反应呈黄色——钠元素;
红褐色固体——Fe(OH)3;
紫红色固体——Cu;
黄绿色气体——Cl2;
地壳中含量最多的元素——O;
地壳中含量最多的金属元素——Al;
最常见的无色液体——H2O;
浅绿色溶液——含Fe2+;
蓝色溶液——含Cu2+;
黄色溶液——含Fe3+;
日常生活中常见的金属——Al、Fe、Cu;
胃酸的主要成分——盐酸;
无色刺激性气味的气体——SO2、NH3、HCl;
大气污染物——NO、CO、SO2;
气体相遇产生大量的白烟——HCl、NH3;
既能与盐酸又能与氢氧化钠溶液反应——Al(单质)、Al2O3(氧化物)、Al(OH)3(氢氧化物)等。
这些特征往往是解题的突破口。
(2)限范围。
题目一般考查的是中学化学中常见的物质,如题目中的金属单质可初步猜想为Na、Al、Fe、Cu等,常见气体单质可初步猜想为H2、O2、N2、Cl2等,又如短周期元素等。
再结合“题眼”和转化关系进一步缩小范围直至确定。
(3)细求证。
即把推断的初步结果代入框图转化中,看是否完全符合,物质是否唯一确定。
(4)会表达。
推断结果往往结合化学用语的考查,一定要按题目要求回答和表达。
特别注意区别“名称”与“符号”、“化学式”与“电子式”、“离子方程式”与“化学方程式”等化学用语。
【例1】
(2018届无锡市第一次模拟测试)有关物质的转化关系如右下图所示(部分生成物与反应条件已略去)。
其中A是最常见的无色液体,B、C、D、E均为单质,G是一种极易溶于水的碱性气体,F是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应④是工业制X的主要反应之一。
(1)G的电子式为 。
(2)I的化学式为 。
(3)写出反应②的离子方程式:
。
(4)写出反应④的化学方程式:
笔记:
【例2】(2017届南通市模拟)下图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。
已知X、Y、Z是日常生活中常见金属单质,X由地壳中含量最高的金属元素组成;
D、E是常见气态非金属单质,其中D呈黄绿色。
A的焰色反应呈紫色(透过蓝色钴玻璃),F的稀溶液呈蓝色。
请回答下列问题:
(1)C的电子式为 。
(2)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,该反应的化学方程式为 。
(3)X与C溶液反应的离子方程式为 。
(4)写出J与Y反应的化学方程式,并标出电子转移的方向和数目:
。
1.(2017年江苏省普通高中学业水平测试)有关物质的转化关系如下图所示(部分生成物和反应条件已略去)。
D、F、G、H均为常见气体,其中D能使湿润的红色石蕊试纸变蓝,G呈黄绿色,H在空气中含量最高;
C的摩尔质量为32g·
mol-1;
E为难溶性碱。
(1)C的化学式为 。
(2)H的电子式为 。
(3)写出反应①的离子方程式:
。
(4)写出反应②的化学方程式:
。
2.(2016年江苏省普通高中学业水平测试)有关物质的转化关系如下图所示(部分生成物与反应条件已略去)。
A是常见的非金属固体单质,F是紫红色的金属单质,B、C是常见的强酸,D、G、I是常见的气体,D与I的组成元素相同,且D的相对分子质量比I的大16;
E是最常见的无色液体。
(1)E的电子式为 。
(2)H的化学式为 。
(3)写出反应①的化学方程式:
(4)写出反应③的离子方程式:
3.(2015年江苏省普通高中学业水平测试)有关物质的转化关系如下图所示(部分物质与条件已略去)。
A是常见的金属单质,B是常见的强酸,E是空气中含量最多的单质,I是既能与强酸又能与强碱反应的氧化物,G是最常见的无色液体,J是一种高硬度材料(摩尔质量为41g·
mol-1)。
(1)D的化学式为 。
(2)F的电子式为 。
4.(2014年江苏省普通高中学业水平测试)有关物质的转化关系如下图所示(部分物质的条件已略去)。
A是海水中含量最多的盐,B、E、F是气体单质,C是金属单质,X是能使湿润红色石蕊试纸变蓝的气体,Y是最常见的无色液体。
(1)X的化学式为 。
(2)E的电子式为 。
(3)写出C与Y反应的化学方程式:
。
(4)写出D溶液与G溶液反应的离子方程式:
。
5.(2013年江苏省普通高中学业水平测试)有关物质的转化关系如下图所示(部分物质和条件已略去)。
B、C、E是常见气体;
A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;
G的焰色反应显黄色;
I的溶液呈黄色。
(1)F的化学式为 。
(2)E的电子式为 。
(3)写出Y和D溶液反应的离子方程式:
(4)写出C与H溶液反应的化学方程式,并用单线桥标出电子转移的方向和数目:
。
6.(2012年江苏省普通高中学业水平测试)在下图所示的物质转化关系中(反应条件未全部列出),A为某金属矿的主要成分,B、D为组成元素相同的无色液体。
C、E是单质,I的溶液呈蓝色,反应①是工业上冶炼金属的一种方法。
(1)B的电子式为 。
(2)G的化学式为 。
(3)E与H的浓溶液反应的化学方程式为 。
(4)I的溶液与氢氧化钠溶液反应的离子方程式为 。
1.(2018届徐州市第一次模拟测试)有关物质的转化关系如下图所示(部分物质与条件已略去)。
A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物;
I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中。
(1)H的化学式为 。
(2)D的电子式为 。
。
(4)写出G的水溶液与C的硝酸盐溶液反应的离子方程式:
2.(2018届苏州市第一次模拟测试)下图所示的是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。
(2)J的化学式为 。
(3)I露置于空气中,颜色由白色迅速变成灰绿色,最终变成红褐色,该反应的化学方程式为 。
(4)X与C溶液反应的离子方程式为 。
3.(2018届徐州市第二次模拟测试)有关物质的转化关系如下图所示(部分物质与条件已略去)。
A是中学化学常见的单质。
C为中学化学常见的暗紫色固体,其水溶液为紫红色。
B、D为常用的强酸溶液,E是温室气体的主要成分,检验F气体常用品红溶液,G是日常生活中的常见溶液,H是黄绿色气体。
J、K的焰色为黄色,M是普通玻璃的成分之一。
(1)E的电子式为 。
(2)M的化学式为 。
(4)写出反应①的化学方程式:
4.(2018届南京市金陵中学模拟测试)有关物质的转化关系如下图所示(部分物质与条件已略去)。
已知单质A、B常温下为气体且B为黄绿色。
反应③是置换反应,反应⑥是实验室鉴定气体化合物I的方法,化合物J遇KSCN溶液显血红色。
(1)C的化学式为 。
(2)化合物D的电子式为 。
(3)写出反应⑤的离子反应方程式:
(4)写出反应⑦的化学反应方程式:
5.(2018届镇江市模拟测试)有关物质的转化关系如下图所示(反应条件未全部列出)。
A、B、C、D、K为常见的单质,其中A为淡黄色固体,K为紫红色金属,B、C、D在常温常压下是气体,C在空气中含量最多。
G为最常见的无色液体,反应③中F过量,I是常用化肥。
(3)写出反应③的离子方程式:
。
(4)写出反应⑤的化学方程式:
知识扫描
略
典例分析
【例1】
(1)
(2)AgNO3
(3)Ag+2H++NO===Ag++NO2↑+H2O
(4)4NH3+5O24NO+6H2O
解析:
A是最常见的无色液体,A为H2O,G是一种极易溶于水的碱性气体,则G为NH3,F是胃酸的主要成分,为HCl,K是不溶于稀硝酸的白色沉淀,为AgCl,由转化关系可知C为O2,D为H2,E为N2,反应④是工业制X的主要反应之一,则X为硝酸,反应④生成J为NO,反应②为Ag和硝酸的反应,B为Ag,H为NO2