高考冲刺化学大题百题精练 专题02 氧化还原反应Word格式.docx
《高考冲刺化学大题百题精练 专题02 氧化还原反应Word格式.docx》由会员分享,可在线阅读,更多相关《高考冲刺化学大题百题精练 专题02 氧化还原反应Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
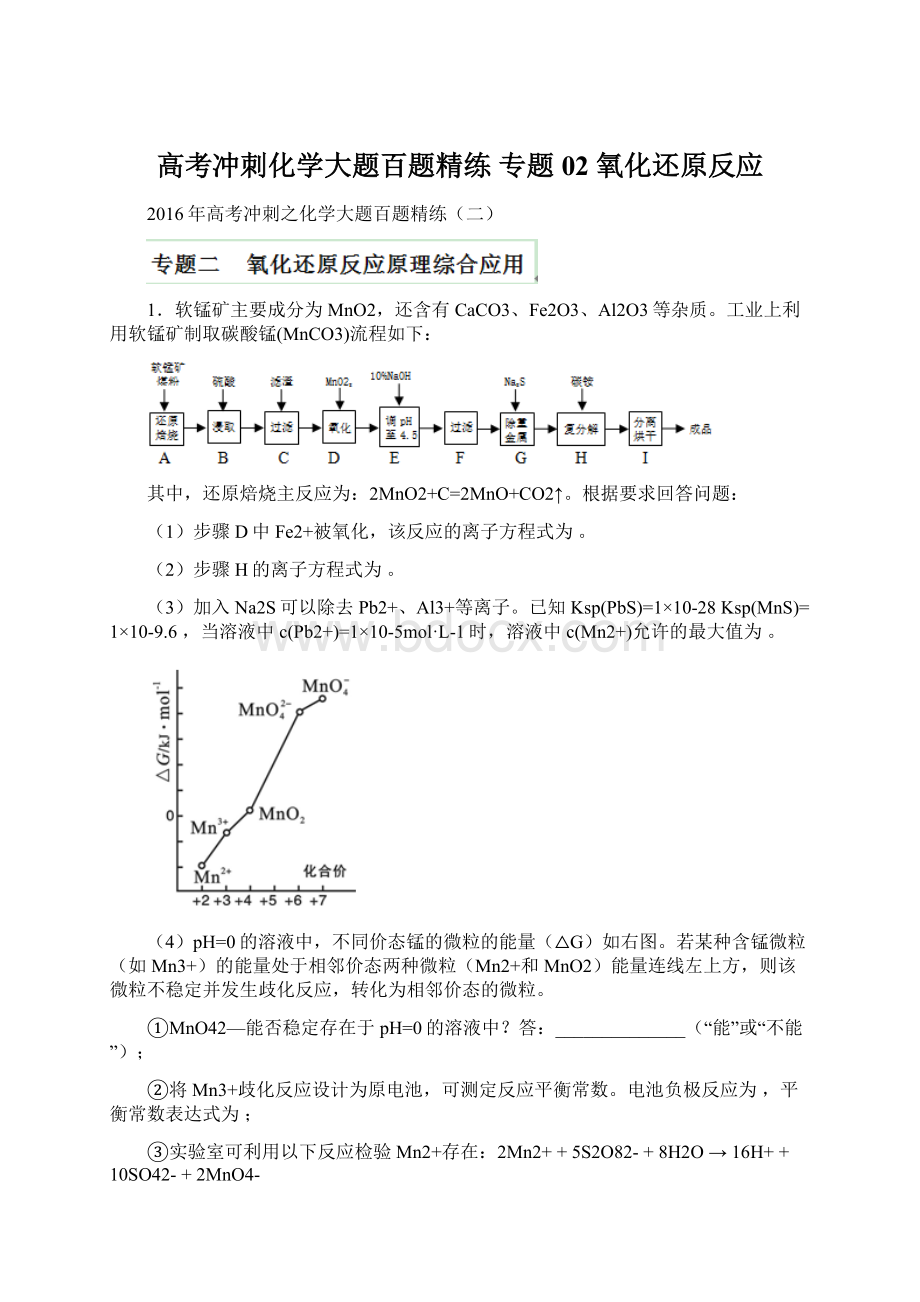
10-5mol·
L-1时,溶液中c(Mn2+)允许的最大值为。
(4)pH=0的溶液中,不同价态锰的微粒的能量(△G)如右图。
若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。
①MnO42—能否稳定存在于pH=0的溶液中?
答:
______________(“能”或“不能”);
②将Mn3+歧化反应设计为原电池,可测定反应平衡常数。
电池负极反应为,平衡常数表达式为;
③实验室可利用以下反应检验Mn2+存在:
2Mn2++5S2O82-+8H2O→16H++10SO42-+2MnO4-
确认Mn2+存在的现象是;
检验时必须控制Mn2+浓度和用量不能过大,否则实验失败。
理由是。
【答案】
(1)2Fe2++MnO2+4H+==2Fe3++Mn2++2H2O
(2)Mn2++2HCO3—=MnCO3↓+CO2↑+H2O(3)1×
1013.4mol·
L-1
(4)①不能②Mn3++2H2O-e-=MnO2+4H+K=c(Mn2+)·
c4(H+)/c2(Mn3+)
③溶液呈紫红色过量的Mn2+能与反应生成的MnO4-反应,影响实验现象的观察
(4)①由图像可知,MnO42—的能量处于相邻价态两种微粒(MnO4—和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒;
②Mn3+歧化反应会生成Mn2+和MnO2,方程式为2Mn3++2H2O=Mn2++MnO2+4H+,设计成原电池,负极反应为Mn3++2H2O-e-=MnO2+4H+,平衡常数表达式为K=c(Mn2+)·
c4(H+)/c2(Mn3+);
③MnO4-是紫红色,所以确认Mn2+存在的现象是溶液呈紫红色;
检验时必须控制Mn2+浓度和用量不能过大,因为过量的Mn2+能与反应生成的MnO4-反应,影响实验现象的观察。
考点:
物质的分离与提纯,氧化还原反应,溶度积常数
2.海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。
下图是海水综合利用的部分流程图,据图回答问题:
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式)________________________________________。
(2)①目前较先进的电解制碱法是离子交换膜电解法,即用阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是________,电解饱和食盐水的化学反应方程式为______________。
②制取MgCl2的过程中涉及反应:
MgCl2·
6H2OMgCl2+6H2O,该反应要在HCl气氛中进行,原因是____________。
(3)苦卤中通入Cl2已经置换出Br2,为什么吹出后用SO2吸收转化为Br-再用Cl2置换_________,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为__________________。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。
该反应的离子方程式是_____________;
最后再用H2SO4处理得到Br2,之后加入CCl4进行Br2的萃取,最终用_____________方法得到单质Br2。
(1)BaCl2、NaOH、Na2CO3、HCl;
(2)①阻止H2与Cl2发生反应甚至发生爆炸或阻止Cl2与生成的NaOH溶液反应而使烧碱产品不纯;
2NaCl+2H2OCl2↑+H2↑+2NaOH;
②防止MgCl2水解;
(3)第一次吹出的Br2浓度太低,分离浪费原料,SO2吸收主要起到富集作用 Cl2>Br2>SO2(4)3Br2+3CO32-═5Br-+BrO-3+3CO2↑;
蒸馏
(2)①阳离子交换膜只能阳离子通过,阴离子和气体不能通过,用石墨作电解电解饱和氯化钠时,阳极上氯离子放电生成氯气,氯气不能通过阳离子交换膜而进入阴极,如果氯气进入阴极易和氢气混合产生爆炸,且易和氢氧化钠溶液反应生成氯化钠、次氯酸钠而导致制取的氢氧化钠不纯,电解饱和食盐水反应的化学方程式为:
2NaCl+2H2OCl2↑+H2↑+2NaOH,故答案为:
阻止H2与Cl2发生反应甚至发生爆炸或阻止Cl2与生成的NaOH溶液反应而使烧碱产品不纯;
2NaCl+2H2OCl2↑+H2↑+2NaOH;
②氯化镁在水中乙发生水解,为抑制水解,氯化镁晶体应在氯化氢气流中脱水,故答案为:
在HCl气流中加热脱水(防止MgCl2水解);
故答案为:
防止MgCl2水解;
(3)苦卤中通入Cl2已经置换出Br2,吹出后用SO2吸收转化为Br-再用Cl2置换是为了富集溴元素,第一次吹出的Br2浓度太低,分离浪费原料,SO2吸收主要起到富集作用,在自发进行的氧化还原反应中,还原剂的还原性大于还原产物的还原性,氧化剂氧化性大于氧化产物,Cl2+2Br-=Br2+2Cl-中还原性Br->Cl-,SO2+2H2O+Br2=H2SO4+2HBr中还原性SO2>Br-,所以还原性强弱顺序是SO2>Br->Cl-,氧化性强弱顺序为:
Cl2>Br2>SO2,故答案为:
第一次吹出的Br2浓度太低,分离浪费原料,SO2吸收主要起到富集作用 Cl2>Br2>SO2
考查了海水资源及其综合利用的相关知识。
3.我国产铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出。
该工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法。
I.氧化浸出
(1)在硫酸介质中用双氧水将黄铜矿氧化,测得有SO42-生成。
①该反应的离子方程式为____。
②该反应在25—50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,试分析其原因为。
.
Ⅱ,配位浸出反应原理为:
(2)为提高黄铜矿的浸出率,可采取的措施有____(至少写出两点)。
(3)为稳定浸出液的pH,生产中需要向氨水中添加NH4C1,构成NH3.H2O-NH4Cl缓冲溶液。
某小组在实验室对该缓冲体系进行了研究:
25℃时,向amol.L-l的氨水中缓慢加入等体积0.02mol.L-l的NH4C1溶液,平衡时溶液呈中性。
则NH3.H2O的电离常数Kb=_(用含a的代数式表示);
滴加NH4C1溶液的过程中水的电离平衡____(填“正向”、“逆向”或“不”)移动。
Ⅲ,生物浸出
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
(4)在微生物的作用下,可以循环使用的物质有(填化学式),微生物参与的离子反应方程式为________(任写一个)。
(5)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2molSO42-生成时,理论上消耗O2的物质的量为____。
(1)①2CuFeS2+17H2O2+2H+=2Cu2++2Fe3++4SO+18H2O②H2O2受热分解;
产物Cu2+、Fe3+催化H2O2分解等
(2)提高氨水的浓度、提高氧压(3)正向(4)Fe2(SO4)3、H2SO44Fe2++O2+4H+4Fe3++2H2O或S8+12O2+8H2O8SO+16H+任写一个(5)4.25mol
(4)据图像可得,三价铁被还原成二价,经微生物转化成三价,另一条微生物路线生成了氢离子,故两考点:
考查无机图像及相关计算
4.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
已知:
①Na2CO3+Al2O32NaAlO2+CO2↑;
②Cr2O72-+H2O2CrO42-+2H+
根据题意回答下列问题:
(1)请完成下列化学方程式的配平:
FeO•Cr2O3+Na2CO3+O2Na2CrO4+Fe2O3+CO2↑;
其中CO2的结构式______
(2)酸化步骤用醋酸调节溶液pH<5,其目的是______;
(3)固体Y的主要成分是,写出生成Y的离子方程式;
(4)操作Ⅲ由多步组成,获得K2Cr2O7晶体的操作依次是:
加入KCl固体、蒸发浓缩、______、过滤、______、干燥;
(5)操作Ⅲ发生反应的化学方程式为;
(6)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化成乙醛,自身被还原为三价铬离子。
该反应的离子方程式为。
(1)4、8、7、8、2、8;
O=C=O;
(2)使CrO42-转化Cr2O72-;
(3)Al(OH)3;
AlO2-+CH3COOH+H2O═Al(OH)3↓+CH3COO-;
(4)冷却结晶;
洗涤;
(5)Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl;
(6)Cr2O72-+3CH3CH2OH+8H+=2Cr3++3CH3CHO+7H2O。
(3)根据流程分析可知,用醋酸调节pH值后产生的沉淀为氢氧化铝,所以Y为Al(OH)3,生成Al(OH)3的离子方程式为AlO2-+CH3COOH+H2O═Al(OH)3↓+CH3COO-,故答案为:
Al(OH)3;
(4)获得K2Cr2O7晶体的方法是蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:
冷却结晶;
(5)Na2Cr2O7的溶解度小于K2Cr2O7,反应向溶解度小的方向进行,所以反应的化学方程式为Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl,故答案为:
Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl;
(6)K2Cr2O7在酸性条件下将乙醇氧化成乙醛,自身被还原为三价铬离子,反应的离子方程式为Cr2O72-+3CH3CH2OH+8H+=2Cr3++3CH3CHO+7H2O,故答案为:
Cr2O72-+3CH3CH2OH+8H+=2Cr3++3CH3CHO+7H2O。
考查了物质制备流程和方案的分析判断的相关知识。
5.以某菱锰矿(含MnCO3、SiO2、FeCO3和少量Al2O3等)为原料通过以下方法可获得碳酸锰粗产品。
(已知:
Ksp(MnCO3)=2.2×
10−11,Ksp[Mn(OH)2]=1.9×
10−13,Ksp[Al(OH)3]=1.3×
10−33)
(1)滤渣1中,含铁元素的物质主要是(填化学式,下同);
加NaOH调节溶液的pH约为5,如果pH过大,可能导致滤渣1中含量减少。
(2)滤液2中,+1价阳离子除了H+外还有(填离子符号)。
(3)取“沉锰”前溶液amL于锥形瓶中,加入少量AgNO3溶液(作催化剂)和过量的1.5%(NH4)2S2O8溶液,加热,Mn2+被氧化为MnO4−,反应一段时间后再煮沸5min[除去过量的(NH4)2S2O8],冷却至室温。
选用适宜的指示剂,用bmol·
L−1的(NH4)2Fe(SO4)标准溶液滴定至终点,消耗(NH4)2Fe(SO4)2标准溶液VmL。
①M