化学试题无机框图推断题Word下载.doc
《化学试题无机框图推断题Word下载.doc》由会员分享,可在线阅读,更多相关《化学试题无机框图推断题Word下载.doc(20页珍藏版)》请在冰豆网上搜索。
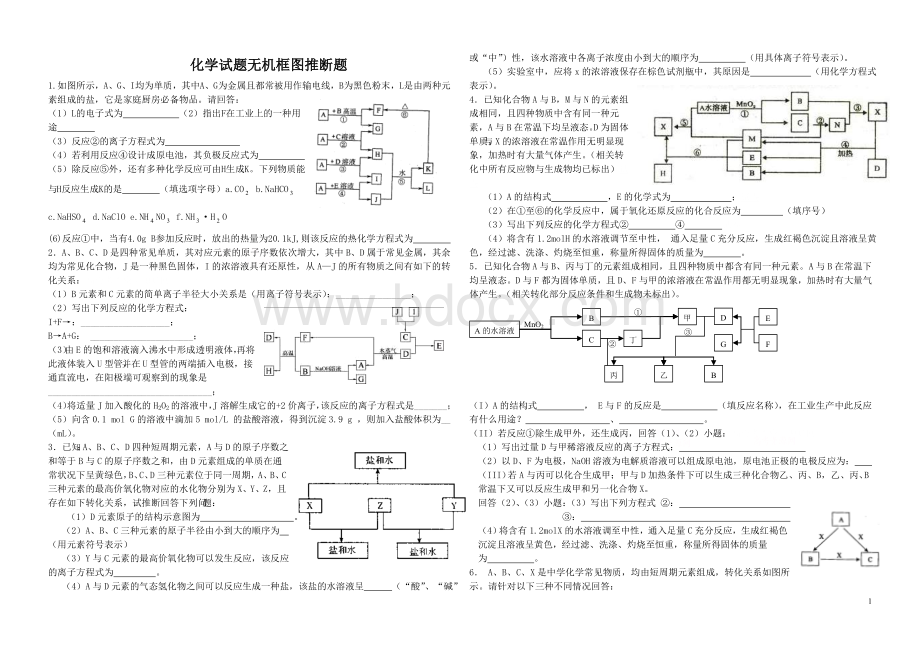
___________________;
B→A+G:
______________________;
(3)由E的饱和溶液滴入沸水中形成透明液体,再将此液体装入U型管,并在U型管的两端插入电极,接通直流电,在阳极端可观察到的现象是___________________________________;
(4)将适量J加入酸化的H2O2的溶液中,J溶解生成它的+2价离子,该反应的离子方程式是_______;
(5)向含0.1molG的溶液中滴加5mol/L的盐酸溶液,得到沉淀3.9g,则加入盐酸体积为__(mL)。
3.已知:
A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题:
(1)D元素原子的结构示意图为。
(2)A、B、C三种元素的原子半径由小到大的顺序为(用元素符号表示)
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为。
(4)A与D元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈(“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为(用具体离子符号表示)。
(5)实验室中,应将x的浓溶液保存在棕色试剂瓶中,其原因是(用化学方程式表示)。
4.已知化合物A与B,M与N的元素组成相同,且四种物质中含有同一种元素,A与B在常温下均呈液态。
D为固体单质,与X的浓溶液在常温作用无明显现象,加热时有大量气体产生。
(相关转化中所有反应物与生成物均已标出)试卷
(1)A的结构式,E的化学式为;
试卷
(2)在①至⑥的化学反应中,属于氧化还原反应的化合反应为(填序号)
(3)写出下列反应的化学方程式②④试卷
(4)将含有1.2molH的水溶液调节至中性,通入足量C充分反应,生成红褐色沉淀且溶液呈黄色,经过滤、洗涤、灼烧至恒重,称量所得固体的质量为。
5.已知化合物A与B、丙与丁的元素组成相同,且四种物质中都含有同一种元素。
A与B在常温下均呈液态。
D与F都为固体单质,且D、F与甲的浓溶液在常温作用都无明显现象,加热时有大量气体产生。
(相关转化部分反应条件和生成物未标出)。
A的水溶液
B
C
MnO2
丁
甲
D
G
F
E
丙
乙
②
③
①
(I)A的结构式,E与F的反应是(填反应名称),在工业生产中此反应有什么用途?
、。
(II)若反应①除生成甲外,还生成丙,回答
(1)、
(2)小题:
(1)写出过量D与甲稀溶液反应的离子方程式:
(2)以D、F为电极,NaOH溶液为电解质溶液可以组成原电池,原电池正极的电极反应为:
(III)若A与丙可以化合生成甲;
甲与D加热条件下可以生成三种化合物乙、丙、B,乙、丙、B常温下又可以反应生成甲和另一化合物X。
回答
(2)、(3)小题:
(3)写出下列方程式②:
③:
(4)将含有1.2molX的水溶液调至中性,通入足量C充分反应,生成红褐色沉淀且溶液呈黄色,经过滤、洗涤、灼烧至恒重,称量所得固体的质量为。
6.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示。
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀①A中含有的金属元素为___________。
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式为________。
(2)若A为固态非金属单质,A与X同周期,常温常压下C为白色固体,B分子中各原子最外层均为8e结构。
①B的电子式为_____________。
②C与水剧烈反应,生成两种常见酸,反应的化学方程式为_____________。
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①A中所含有的化学键是_____________。
②将4.48L(标准状况下)X通入100mL3mol/LA的水溶液后,溶液中离子浓度由大到小的顺序为___________。
③自然界中存在B、C和H2O按一定比例结晶而成的固体。
取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L。
若取相同质量的固体加热至恒重,剩余固体的质量为__________。
8.合金A由4种单质组成,经过一系列反应分别进入了沉淀或气体中.
试回答:
(1)合金A由哪4种元素的单质组成?
_________、________、________、_________.
(2)写出固体B、溶液C、沉淀D和气体E、F有关组成的化学式:
B_________、C_________、D_________、E_________、F_________.
(3)写出合金A中的有关组成与过量烧碱溶液反应生成无色气体E的化学反应方程式:
__________________________________________________________________________.
(4)写出向无色溶液C加适量盐酸生成白色沉淀D有关反应的离子方程式:
附加:
(近几年高考加强了计算的考查,提供两个计算推断)
9、有A、B两种无机含氧酸的正盐,A盐中的阳离子为+2价,B盐中的阳离子为+1价.现把两盐的浓溶液混合使其发生复分解反应,完全作用后产生带+2价阳离子的沉淀C及含溶质D的滤液.取5.00g沉淀C在高温下灼烧可得2.80g固态的金属氧化物E,并生成了能使澄清石灰水变浑浊的无色刺激性气味的气体F.1mol固体D受热分解,生成1mol气态非金属氧化物G和(气)组成的混合气体,混合气体的密度是的倍.请回答:
(1气体F的化学式是________________;
(2)列式计算确定金属氧化物E的化学式
(3)列式计算确定非金属氧化物G的化学式
(4)A的化学式是_________________,B的化学式是________________.
10.某复盐的组成可表示为:
,R为-2价含氧酸根.为了确定该盐的组成,进行如下实验:
(1)准确称取4.02g样品加热到失去全部结晶水,冷却后称量,质量为2.94g.
(2)将剩余固体溶于适量水,滴加盐酸,无现象,再滴加足量溶液,产生白色沉淀.过滤,将沉淀烘干,称质量为4.66g.
(3)向上述溶液中加入过量NaOH溶液,产生白色沉淀,过滤,将沉淀烘干,称质量为0.58g,再将固体高温灼烧后冷却,称得剩余固体质量是0.40g.
请通过计算回答下列问题:
(1)确定R的化学式. R的化学式______________.
(2)求x、y、z的值. x=________,y=________,z=_________.
(3)确定A是什么元素. A元素的名称是_____________.
(4)该复盐的化学式为______________.
(5)要确定某化合物是否含A元素,最简单方法是______________.
答案:
1.
(1)
(2)用作冶炼铝的原料;
用作耐火材料。
(3)2Al+3Cu2+=2Al3++3Cu
(4)Al—3e—+4OH—=AlO2—+2H2O
(5)bdf
(6)2Al(s)+3CuO(s)=Al2O3(s)+3Cu(s);
△H=—1206kJ/mol
2.
(1)r(Al3+)<
r(Cl�)(或Al3+<
Cl�);
(2)8HCl+Fe3O4=FeCl2+2FeCl3+4H2O;
2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)红褐色变浅;
(4)MnO2+H2O2+2H+=Mn2++O2↑+2H2O;
(5)10和(或)50;
3.
(1)
(2)N<
Al<
Na
(3)Al2O3+2OH-+3H2O=2[Al(OH)4]-
光
(4)酸c(OH-)<
c(H+)<
c(NH+)<
c(Cl-)
(5)4HNO3(浓)4NO2↑+O2↑+2H2O4.⑴H-O-O-H(2分),Fe2(SO4)3试卷
催化剂
4、
(1)⑵②⑤
△
⑶②2SO2+O22SO3试卷
④2Fe+6H2SO4(浓)Fe2(SO4)3+3SO2↑+6H2O
⑷32g
5
(I)H-O-O-H,铝热反应,焊接铁轨、冶炼金属;
(II)
(1)3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O
(2)6H2O+6e-=3H2↑+6OH-
(III)(3)②:
2SO2+O22SO3
③:
2Fe+6H2SO4(浓)Fe2(SO4)3+3SO2↑+6H2O)
(3)32g
6
(1)①铝②8A1十3Fe3O44A12O3+9Fe或2A1+Fe