中考化学试题分类汇编考点58与金属活动性顺序有关的图像题Word文档格式.docx
《中考化学试题分类汇编考点58与金属活动性顺序有关的图像题Word文档格式.docx》由会员分享,可在线阅读,更多相关《中考化学试题分类汇编考点58与金属活动性顺序有关的图像题Word文档格式.docx(9页珍藏版)》请在冰豆网上搜索。
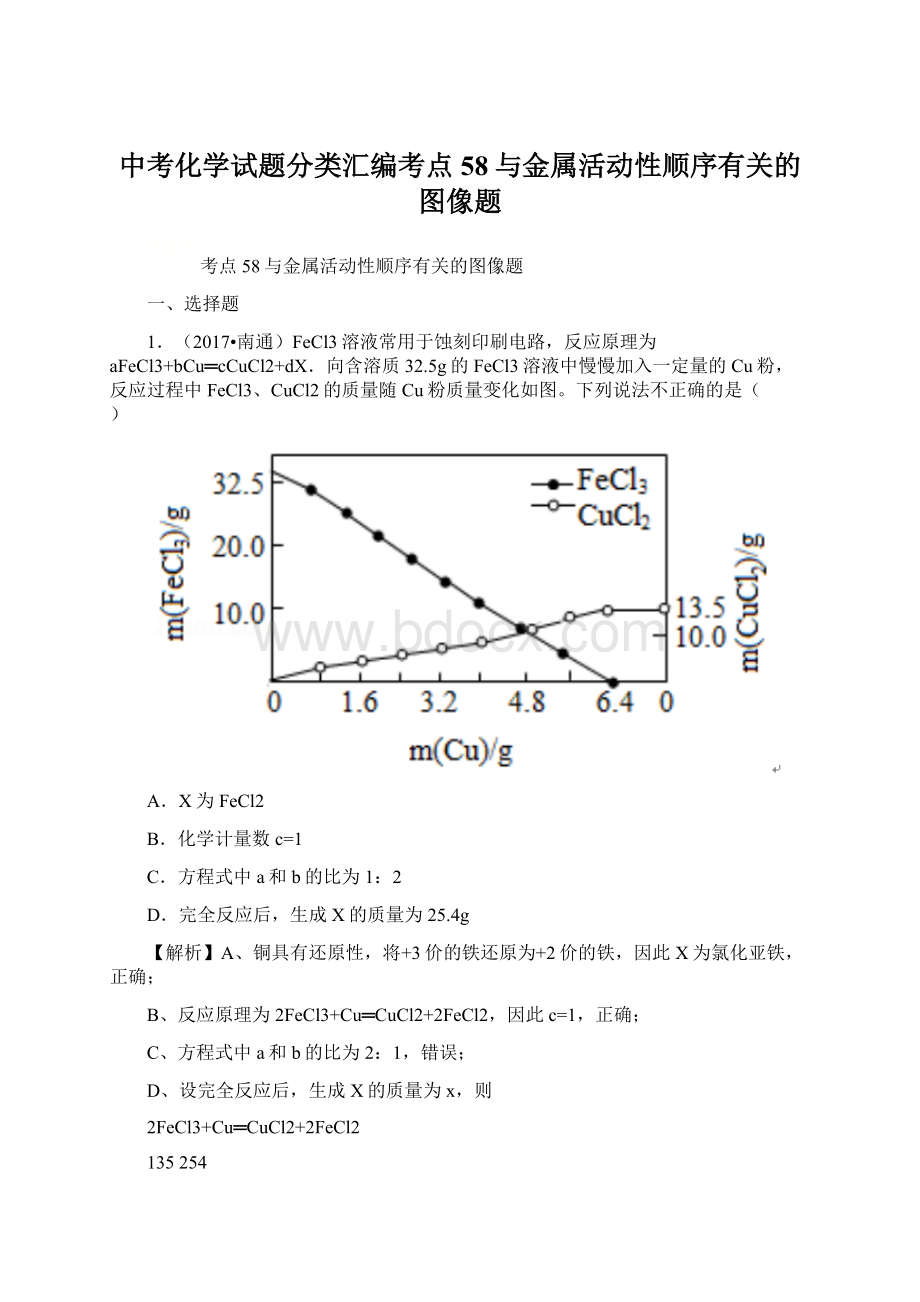
2FeCl3+Cu═CuCl2+2FeCl2
135254
13.5gx
=,x=25.4g
正确。
【答案】C
2.(2017·
牡丹江)向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示。
下列说法正确的是()
A.a点所得溶液中的溶质是硝酸铜、硝酸锌
B.向b点所得固体中加入盐酸有气泡产生
C.c点所得固体为银和铜
D.d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜
【解析】锌比铜活泼,铜比银活泼,向一定质量AgNO3和Cu(NO3)2的混合溶液中加入锌粉,锌先和硝酸银反应,如果反应后锌过量,则再和硝酸铜反应;
锌和硝酸银、硝酸铜反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,
65216
Zn+Cu(NO3)2=Zn(NO3)2+Cu,
6564
由以上质量关系可知,锌和硝酸银反应后溶液质量减小,和硝酸铜反应后溶液质量增大,即从开始反应至b点时,是锌和硝酸银反应,b-c点时是锌和硝酸铜反应。
A、a点时锌和部分硝酸银反应,溶液中的溶质有:
反应生成的硝酸锌、剩余的硝酸银和没有反应的硝酸铜,错误;
B、b点时锌和硝酸银恰好反应,固体中只有银一种物质,加入盐酸没有气泡产生,错误;
C、b~c段是锌和硝酸铜反应,c点表示锌和硝酸铜恰好反应,所得固体为银和铜,正确;
D、d点表示锌过量,所得溶液中溶质只有硝酸锌,错误。
3.(2017•通辽)向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
A.a点所得固体为银和铁
B.b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌
C.c点所得溶液中的溶质为硝酸亚铁和硝酸锌
D.d点所得固体为银、铁和锌
【解析】A、a点所得固体为硝酸银和锌反应生成的银,该选项说法不正确;
B、b点时硝酸银完全反应,所得溶液中的溶质是没有反应的硝酸亚铁和反应生成的硝酸锌,选项说法不正确;
C、c点时硝酸亚铁完全反应,所得溶液中的溶质为反应生成的硝酸锌,选项说法不正确;
D、d点所得固体为反应生成的银、铁和过量的锌,选项说法正确.
【答案】D
4.(2017浙江省义乌市,题号14,分值4)往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是()
A、c点对应溶液中含有的金属离子为Zn2+和Cu2+
B、bc段(不含两端点)析出的金属是Fe
C、ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+
D、若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,则m1>
m2
【解析】本题考查金属活动性顺序及其应用、金属和盐溶液的反应。
向一定量硝酸铜、硝酸银和硝酸亚铁的混合溶液中加入锌粉,锌先与硝酸银反应,把硝酸银反应完了,再与硝酸铜反应,最后与硝酸亚铁反应,ab之间是锌与一部分硝酸银反应,b点是锌与硝酸银刚好反应完,c点是锌与硝酸铜刚好反应完,cd点是继续加入锌粉,再进一步进行分析解答即可。
A、c点是锌与硝酸铜刚好反应完,溶液中不含Cu2+,A错误;
B、bc段锌与硝酸铜,析出金属为Cu,B错误;
C、ab之间是锌与一部分硝酸银反应,溶液中含有的金属离子为Zn2+、Ag+、Cu2+和Fe2+,C正确;
D、Cu的相对原子质量大于Fe,因此析出固体质量相等时,Cu的需要的锌小于Fe,故m1<m2,D错误。
5.(2017年山东省泰安市题号132分)现有等质量的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如下图所示(已知甲、乙、丙在生成物中的化合价均为+2价)。
则下列说法中不正确的是()
A.生成氢气的质量:
甲>
乙>
丙B.相对原子质量:
丙>
甲
C.金属活动性:
丙D.消耗硫酸的质量:
丙
【答案】B
【解析】A.由图像可知,三种金属完全反应后生成氢气的质量有多到少的顺序是:
丙,A正确;
B.根据化学方程式计算可得:
金属与稀酸反应生成氢气质量=金属质量×
金属的化合价/金属的相对原子质量,三种金属质量相等、生成物中三种金属的化合价均为+2价,由上式可知,生成氢气质量与金属的相对原子质量成反比例,由此可得三种金属的相对原子质量由大到小的顺序是:
甲,B错误;
C.金属越活泼,在相同时间内产生的氢气越多,由图可知,三种金属的活动性顺序为:
丙,C正确;
D.三种金属完全反应,生成的氢气质量越多,消耗的稀硫酸的质量就越多,所以消耗稀硫酸的质量是:
丙,D正确。
6.(2017浙江省绍兴市,14,4)往硝酸铜、硝酸银和硝酸亚铁的混合溶液中缓慢连续加入质量为m的锌粉,溶液中析出固体的质量与参加反应的锌粉质量关系如图所示,下列说法中正确的是()
A.c点对应溶液中含有的金属离子为Zn2+和Cu2+
B.bc段(不含两端点)析出的金属是Fe
C.ab段(不含两端点)对应溶液中含有的金属离子为Zn2+、Ag+、Cu2+、Fe2+
D.若bc段和cd段中析出固体质量相等,参加反应的锌粉质量分别为m1和m2,m1>
m2
【解析】本题主要考查金属活动性顺序及其应用;
因为四种金属的活动性锌>
铁>
铜>
银,活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来,在反应中,最不活泼的金属最先析出,以此类推,最活泼的金属留在溶液中,所以由图示可知,b点析出的金属是银,c点析出的金属铜,d点析出的是铁,所以c点状态时金属铜完全析出,溶液中含有的金属离子还有Zn2+和Fe2+,故A选项错误;
bc段(不含两端点)析出的金属是Cu,故B选项错误;
ab段(不含两端点)析出的金属是银,溶液含有的金属离子还有Zn2+、Ag+、Cu2+、Fe2+,C选项正确;
Zn+Fe(NO3)2=Zn(NO3)2+Fe,Zn+Cu(NO3)2=Zn(NO3)2+Cu
65566564
由方程式中等质量的锌完全反应置换出铜的质量多于铁可知,当置换出相等质量的铜和铁时消耗的锌质量是铁多余铜,所以m1<
m2,故D选项错误。
7.(2017遂宁市,题号7,分值3)向装有过量锌粉的烧杯中加入一定质量AgNO3,和Cu(NO3)2的混合溶液,烧杯中固体的质量随反应时间变化的情况如图所示。
下列说法正确的是
A.t1时,向溶液中滴加氯化钠溶液,没有白色沉淀产生
B.t3和t5时,溶质种类不同,金属单质种类也不同
C.若向溶液中插入铝丝,铝丝表面有红色固体析出,则时间t的取值范围是:
t2<
t<
t4
D.t2时,溶液中的金属离子有Zn2+、Cu2+,固体中的金属单质有Zn、Ag
【解析】此题考察金属活动性顺序及其应用,锌比铜活泼,铜比银活泼,所以锌先和硝酸银反应,硝酸银反完之后再和硝酸铜反应,锌和硝酸银反应固体质量增加,和硝酸铜反应固体质量减少,所以0到t2,在和硝酸银反应,t2到t4在和硝酸铜反应。
A.t1时硝酸银还没有反应完,所以加入氯化钠可以产生白色的氯化银沉淀,A选项错误;
B.t3时溶液中含有硝酸铜,t5时硝酸铜已经反应完,所以溶质种类不同,但是金属单质都是锌、铜、银,所以B选项错误;
C.铝丝表面有红色物质析出,说明此时溶液中有铜离子,所以时间为t2到t4之间,所以C选项正确;
D.t2时锌刚好和硝酸银反应完,所以溶液中只有锌离子和铜离子,没有银离子,另外此时又刚好开始和硝酸铜发生反应,所以固体中不仅有锌和银,还应有铜,所以D选项错误。
本题选择C。
二、填空题
1.(2017年山东省泰安市题号24每空1分共6分)金属材料在生产、生活中有着广泛的应用,人类的生产和生活都离不开金属。
(1)新型材料纳米级铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。
高温反应器中反应的化学方程式为________________。
反应前需向反应器中通入氮气,目的是___________;
(2)金属活动性顺序有重要的应用,铝、铜、铁为日常生活中常见的金属,某化学兴趣小组的同学在探究铝、铜、铁三种金属的有关性质时,进行了如下图的实验:
在A实验中发生反应的化学方程式为________________。
将A实验结束后①、②试管内的物质倒入烧杯中,发现烧杯中的红色固体物质明显增多,其原因是______________,一段时间后过滤,滤液中的溶质一定有_____(填化学式);
(3)某同学在一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,充分反应后,他对反应过程进行了分析,得到了以下几个图像(横坐标表示加入铁的质量),其中错误的是______________(填字母序号)。
【答案】
(1)氯化亚铁和氢气在高温的条件下反应生成氯化氢和纳米铁,反应的化学方程式为:
FeCl2+H2高温Fe+2HCl(1分);
氮气化学性质稳定,可作保护气,反应前向反应器中通入氮气的目的是排尽反应器中的空气,防止铁粉与氧气发生反应(1分);
(2)铁比铜活泼,铁能与硫酸铜溶液发生反应生成硫酸亚铁和铜,反应的化学方程式为:
Fe+CuSO4=FeSO4+Cu;
试管①中的铁与硫酸铝不反应,试管①和②混合后,铁与硫酸铜继续反应生成铜,使烧杯中的金属铜增多;
硫酸铝未发生反应,铁和硫酸铜溶液反应生成硫酸亚铁,硫酸铜溶液是否完全反应不能确定,所以,滤液中一定含有的溶质是硫酸铝[Al2(SO4)3]和硫酸亚铁(FeSO4);
(3)铁和硝酸银溶液先反应,刚开始没有铜生成,当硝酸银溶液完全反应后,铁和硫酸铜溶液反应生成铜,铜的质量逐渐增加,完全反应后,铜的质量不变,A图示正确;
开始时,铁和硝酸银溶液反应,所得溶液质量逐渐减小,所以,硝酸铜的溶质分数逐渐增大,当硝酸银完全反应后,铁与硝酸铜溶液反应,硝酸铜质量分数逐渐减小,直至完全反应,B图所示正确;
开始时,铁和硝酸银溶液反应,溶液质量减小的幅度要比后来铁与硝酸铜溶液反应溶液质量减小的幅度大,完全反应后溶液质量不变,C图示正确;
未加入铁粉前,混合液中溶质只有两种,D图示错误,选D。
三、计算题
1.(2017武汉市,32,6)钢是铁的合金,为测定某钢样中铁的质量分数,取11.4克钢样,向其中加入稀硫酸产生氢气的质量与加入稀硫酸的质量关系如图所示(不考虑钢样中其他成分与稀硫酸的反应)。
(1)钢(填“是”或“不是”)金属材料。
(2)计算此钢样中铁的质量分数。
(1)是(1分);
(2)98%(5分)
【解析】本题主要考查根据方程式的计算;
(1)钢是铁碳合金,属于金属材料;
(2)由图示可知反应中生成氢气0.4g,
解:
设钢样中含铁的质量为x,
Fe+H2SO4=FeSO4+H2↑
562
x