奥赛真题物理化学解析Word文件下载.doc
《奥赛真题物理化学解析Word文件下载.doc》由会员分享,可在线阅读,更多相关《奥赛真题物理化学解析Word文件下载.doc(11页珍藏版)》请在冰豆网上搜索。
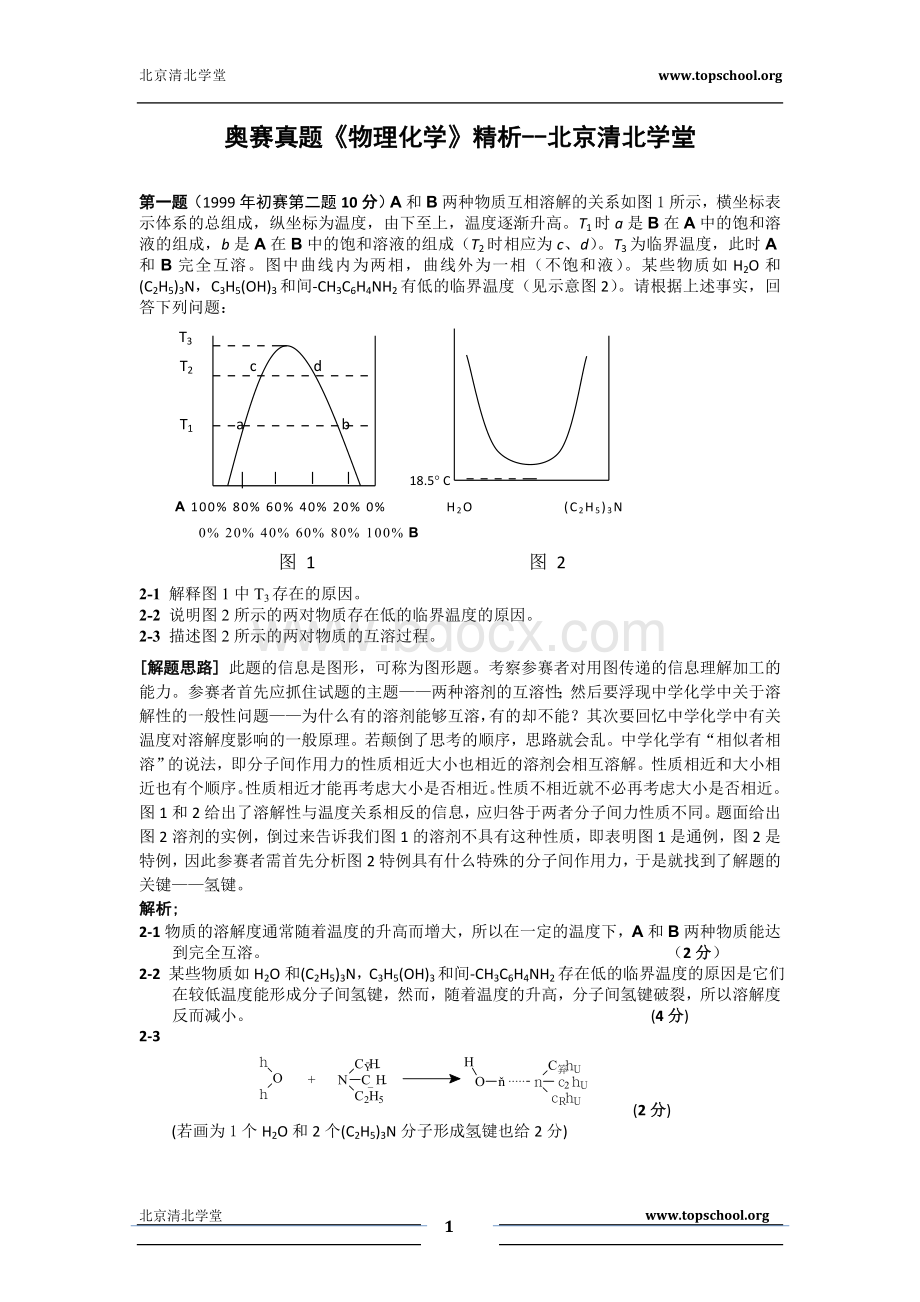
2-2说明图2所示的两对物质存在低的临界温度的原因。
2-3描述图2所示的两对物质的互溶过程。
[解题思路]此题的信息是图形,可称为图形题。
考察参赛者对用图传递的信息理解加工的能力。
参赛者首先应抓住试题的主题——两种溶剂的互溶性;
然后要浮现中学化学中关于溶解性的一般性问题——为什么有的溶剂能够互溶,有的却不能?
其次要回忆中学化学中有关温度对溶解度影响的一般原理。
若颠倒了思考的顺序,思路就会乱。
中学化学有“相似者相溶”的说法,即分子间作用力的性质相近大小也相近的溶剂会相互溶解。
性质相近和大小相近也有个顺序。
性质相近才能再考虑大小是否相近。
性质不相近就不必再考虑大小是否相近。
图1和2给出了溶解性与温度关系相反的信息,应归咎于两者分子间力性质不同。
题面给出图2溶剂的实例,倒过来告诉我们图1的溶剂不具有这种性质,即表明图1是通例,图2是特例,因此参赛者需首先分析图2特例具有什么特殊的分子间作用力,于是就找到了解题的关键——氢键。
解析;
2-1物质的溶解度通常随着温度的升高而增大,所以在一定的温度下,A和B两种物质能达到完全互溶。
(2分)
2-2某些物质如H2O和(C2H5)3N,C3H5(OH)3和间-CH3C6H4NH2存在低的临界温度的原因是它们在较低温度能形成分子间氢键,然而,随着温度的升高,分子间氢键破裂,所以溶解度反而减小。
(4分)
2-3
(2分)
(若画为1个H2O和2个(C2H5)3N分子形成氢键也给2分)
(2分)
(氢键位置不同、生成1、2、3个氢键或其它合理答案均给分)
第二题(2000年初赛第二题6分)今年是勒沙特列(LeChatelier1850-1936)诞生150周年。
请用勒沙特列原理解释如下生活中的常见现象:
打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。
解析:
(1)啤酒瓶中二氧化碳气体与啤酒中溶解的二氧化碳达到平衡:
CO2(气)CO2(溶液),打开啤酒瓶,二氧化碳气体的压力下降,根据勒沙特列原理,平衡向放出二氧化碳气体的方向移动,以减弱气体压力下降对平衡的影响。
(2)温度是保持平衡的条件,玻璃杯的温度比冰镇啤酒的温度高,根据勒沙特列原理,平衡应向减弱温度升高的方向移动,即应向吸热方向移动,从溶液中放出二氧化碳气体是吸热的,因而,应从溶液中放出二氧化碳气体。
注:
压力和温度各3分,不与勒沙特列原理挂钩不给分。
第二题(2001年初赛第十二题11分)设计出燃料电池使汽油氧化直接产生电流是对世纪最富有挑战性的课题之一。
最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。
回答如下问题:
12-1以丁烷代表汽油,这个电池放电时发生的化学反应的化学方程式是:
12-2这个电池的正极发生的反应是:
负极发生的反应是:
固体电解质里的O2-的移动方向是:
向外电路释放电子的电极是:
12-3人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:
12-4你认为在ZrO2晶体里掺杂Y2O3用Y3+代替晶体里部分的Zr4+对提高固体电解质的导电能力会起什么作用?
其可能的原因是什么?
答:
12-5汽油燃料电池最大的障碍是氧化反应不完全产生堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
12-12C4H10+13O2=8CO2+10H2O(1分)
(必须配平;
所有系数除2等方程式均应按正确论。
)
12-2O2+4e=2O2–(2分)(O2取其他系数且方程式配平也给满分。
C4H10+13O2––26e=4CO2+5H2O(2分)(系数加倍也满分。
向负极移动;
(1分;
答向阳极移动或向通入汽油蒸气的电极移动也得满分。
负极。
答阳极或通入汽油蒸气的电极也得满分)
12-3燃料电池具有较高的能量利用率。
(2分)(答内燃机能量利用率较低也满分;
用热力学第二定律解释等,得分相同。
12-4为维持电荷平衡,晶体中的O2–将减少(或导致O2–缺陷)从而使O2–得以在电场作用下向负极(阳极)移动。
(1分)(表述不限,要点是:
掺杂晶体中的O2–比纯ZrO2晶体的少。
12-5碳(或炭粒等)(1分)
第三题(2002年初赛第九题8分)Xe和F2反应,可得三种氟化物,视反应条件而定。
下图表述的是将0.125mol/LXe和1.225mol/LF2为始态得到的生成物在平衡体系内的分压与反应温度的关系。
1.应在什么温度下制备XeF6和XeF4?
2.Xe和F2生成XeF6和XeF4,哪个反应放热更多?
生成的反应放热更多。
理由:
3.为有效地制备XeF2,应在什么反应条件下为好?
简述理由。
【解析】1.约550K约850K(各1分)
2.XeF6若Xe与F2生成XeF4的反应放热多,反应XeF4+F2=XeF6将是吸热反应,温度升高应有利于XeF6的生成,而由附图可见,事实恰恰相反。
(4分)(或答:
反应XeF6=XeF4+F2发生在相对高的温度下;
或答:
上述正向反应是体积增大的反应,所以正向反应是吸热的)
3.在上图条件下必须在高温下才能制备XeF2,但高温要求的技术问题太多,因而,应降低投料中F2/Xe的比值,可有效制备XeF2。
第四题(2002年初赛第十题10分)某远洋船只的船壳浸水面积为4500m2,与锌块相连来保护,额定电流密度为150mA/m2,预定保护期限2年,可选择的锌块有两种,每块的质量分别为15.7kg和25.9kg,通过每块锌块的电流强度分别为0.92A和1.2A。
计算说明,为达到上述保护船体的目的,最少各需几块锌块?
用哪种锌块更合理?
为什么?
【解析】首先算出通过体系的总电量:
2×
365d×
24h/d×
60min/h×
60s/min=6.307×
107s(1分)0.0150A/m2×
4500m2=67.5A(1分);
67.5A×
6.307×
107s=4.257×
109C(1分);
其次计算总共需要多少锌:
电子的量为:
4.257×
109C/9.65×
104C/mol=4.411×
104mol(1分);
锌量:
4.411×
104mol×
65.4g/mol/2×
10-3kg/g=1443kg=1.44×
103kg(1分);
需质量为15.7kg/块的锌块数为:
1.44×
103kg/15.7kg/块=91.7块≈92块(1分);
92块×
0.92A/块=85A>67.5A,电流强度可以达到要求。
(1分);
25.9kg/块:
103kg/25.9kg/块=55.6块≈56块(1分);
56块×
1.2A/块=67.2A<67.5A,电流强度达不到要求,应当加1块,则57块×
1.2A/块=68.4A,电流强度才能达到要求。
(1分)选用较重的锌块更合理,因其电流强度较小,理论上可以保证2年保护期限,而用较轻的锌块因其电流强度太大,不到2年就会消耗光。
(1分)
第五题(2002年初赛第十一题5分)镅(Am)是一种用途广泛的锕系元素。
241Am的放射性强度是镭的3倍,在我国各地商场里常常可见到241Am骨密度测定仪,检测人体是否缺钙:
用241Am制作的烟雾监测元件已广泛用于我国各地建筑物的火警报警器(制作火警报警器的1片241Am我国批发价仅10元左右)。
镅在酸性水溶液里的氧化态和标准电极电势(Ey/V)如下,图中2.62是Am4+/Am3+的标准电极电势,-2.07是Am3+/Am的标准电极电势,等等。
一般而言,发生自发的氧化还原反应的条件是氧化剂的标准电极电势大于还原剂的标准电极电势。
试判断金属镅溶于过量稀盐酸溶液后将以什么离子形态存在。
附:
Ey(H+/H2)=0V;
Eø
(Cl2/Cl-)=1.36V;
(O2/H2O)=1.23V。
【解析】要点1:
Ey(Amn+/Am)<0,因此Am可与稀盐酸反应放出氢气转化为Amn+,n=2,3,4;
但Ey(Am3+/Am2+)<0,Am2+一旦生成可继续与H+反应转化为Am3+。
(1分)(或答:
Ey(Am3+/Am)<0,n=3)要点2:
Ey(Am4+/Am3+)>Ey(AmO2+/Am4+),因此一旦生成的Am4+会自发歧化为AmO2+和Am3+。
(2分)要点3:
AmO2+是强氧化剂,一旦生成足以将水氧化为O2,或将Cl-氧化为Cl2,转化为Am3+,也不能稳定存在。
(1分)相反,AmO2+是弱还原剂,在此条件下不能被氧化为AmO22+。
要点4:
Am3+不会发生歧化(原理同上),可稳定存在。
(1分)结论:
镅溶于稀盐酸得到的稳定形态为Am3+。
第六题(2003年初赛第五题6分)下图是一种正在投入生产的大型蓄电系统。
左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;
放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4和NaBr。
5-1左、右储罐中的电解质分别为;
5-2写出电池充电时,阳极和阴极的电极反应。
5-3写出电池充、放电的反应方程式。
5-4指出在充电过程中钠离子通过膜的流向。
【解析】:
左:
NaBr3/NaBr(1分;
只写一种也可)右:
Na2S2/Na2S4(1分;
只写一种也可)
阳极:
3NaBr