高一有机复习Word文档格式.docx
《高一有机复习Word文档格式.docx》由会员分享,可在线阅读,更多相关《高一有机复习Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
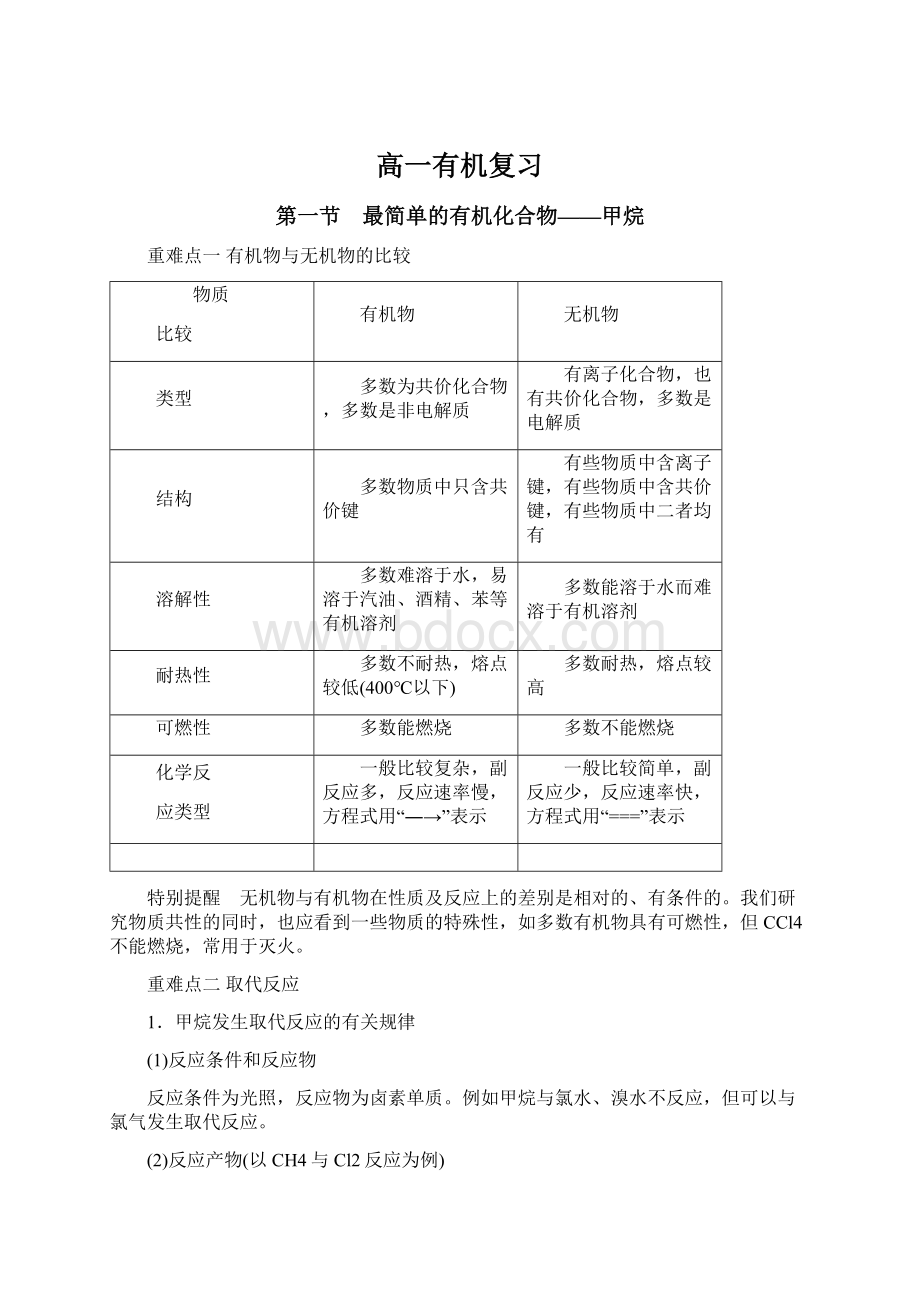
一般比较复杂,副反应多,反应速率慢,方程式用“―→”表示
一般比较简单,副反应少,反应速率快,方程式用“===”表示
特别提醒 无机物与有机物在性质及反应上的差别是相对的、有条件的。
我们研究物质共性的同时,也应看到一些物质的特殊性,如多数有机物具有可燃性,但CCl4不能燃烧,常用于灭火。
重难点二取代反应
1.甲烷发生取代反应的有关规律
(1)反应条件和反应物
反应条件为光照,反应物为卤素单质。
例如甲烷与氯水、溴水不反应,但可以与氯气发生取代反应。
(2)反应产物(以CH4与Cl2反应为例)
反应生成的产物是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与氯化氢形成的混合物,虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不一,但很难出现全部是某一种产物的现象。
(3)物质的量的关系
CH4与Cl2发生取代反应时,每1molH原子被取代,消耗1molCl2分子,同时生成1mol的HCl分子。
特别提醒
(1)有机反应比较复杂,常伴随很多副反应发生,因此有机反应方程式常用“―→”。
(2)CH4与Cl2的反应逐步进行,应分步书写。
(3)当n(CH4)∶n(Cl2)=1∶1时,反应并不只发生CH4+Cl2CH3Cl+HCl,其他反应仍同时发生。
2.取代反应与置换反应的区别
类别
取代反应
置换反应
实例
CH4+Cl2CH3Cl+HCl
Zn+H2SO4===
ZnSO4+H2↑
定义
有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应
一种单质跟一种化合物反应,生成另一种单质和另一种化合物的反应
反应物
一种化合物和另一种化合物或单质
一种单质和一种化合物
生成物
一般生成两种化合物
另一种化合物和另一种单质
反应中
电子得失
不一定发生电子转移,因此不一定是氧化还原反应
一定发生电子转移,一定是氧化还原反应
反应是
否可逆
有不少是可逆反应
一般是不可逆反应
反应
条件
大多需加热、光照、催化剂
一般只需常温或加热
特别提醒 利用取代反应和置换反应的特点来判断所给的反应类型时,一要看反应物,即参加反应的是有机物还是无机物,若反应物均为无机物,则一定不属于取代反应;
二要看生成物,若生成物中有单质,一般也不属于取代反应。
重难点三同系物的判断
1.判断标准
(1)分子结构相似即两种物质均属于同一类物质;
(2)分子组成上相差一个或若干个CH2原子团。
2.互为同系物的有机化合物的组成与结构特点
(1)同系物的结构相似,主要指化学键类型相似,分子中各原子的结合方式相似。
对烷烃而言就是指碳原子之间通过共价单键相连,其余价键全部结合氢原子。
同系物的结构相似,并不是相同。
例如,和CH3CH2CH3,前者有支链,而后者无支链,结构不尽相同,但两者的碳原子均以单键结合成链状,结构相似,故为同系物。
(2)同系物的组成元素必相同。
(3)同系物必符合同一通式。
但符合同一通式,且分子组成上相差一个或若干个CH2原子团的物质也不一定是同系物,如CH2===CH2(乙烯)和(环丙烷)。
(4)同系物一定具有不同的分子式。
特别提醒 根据物质的结构简式判断物质是不是属于同系物,要注意所给的物质是不是分子式相同,若分子式相同则不属于同系物,如CH3CH2CH2CH3和属于同分异构体,不属于同系物。
重难点四同分异构体
1.同分异构体的判断依据
(1)分子式必须相同。
相对分子质量相同、结构不同的化合物不一定是同分异构体。
如C2H4O和CO2;
C2H4和CO;
C8H18和C17H14O等。
(2)结构不同。
注意从两个方面考虑,一是原子或原子团的连接顺序不同,二是原子的空间排列不同。
特别提醒 同分异构体可以是同类物质,也可以是不同类物质。
2.烷烃同分异构体的书写
(1)烷烃的同分异构体的书写一般采用“减链法”,其书写技巧如下:
(2)烷烃同分异构体书写的一般步骤:
①先写出碳原子数最多的主链。
②写出少一个碳原子的主链,另一个碳原子作为甲基接在主链某碳原子上。
③写出少两个碳原子的主链,另两个碳原子作为乙基或两个甲基接在主链碳原子上,以此类推。
(3)实例分析:
现以C6H14为例,基本步骤如下:
a.将分子中全部碳原子连成直链作为母链
b.从母链一端取下一个碳原子作为支链(即甲基),依次连在主链中心对称线一侧的各个碳原子上,此时碳架有两种:
注意 不能连在①位和⑤位上,否则会使碳链变长,②位和④位等效,只能用一个,否则重复。
c.从母链上取下两个碳原子作为一个支链(即乙基)或两个支链(即2个甲基)依次连在主链中心对称线一侧的各个碳原子上,此时碳架结构有两种:
②位或③位上不能连乙基,否则会使主链上有5个碳原子,使主链变长。
所以C6H14共有5种同分异构体。
特别提醒 书写同分异构体时一定要做到“有序”和“等效”,即思维的有序性和碳原子的等效性,避免遗漏和重复。
同时要注意总结规律,如:
①烃的一元取代物种类数等于烃中等效氢原子的种类数,②一种烃如果有m个氢原子,那么它的n元取代物与(m-n)元取代物种类相等。
重难点五“四同”的比较
概念
内容
同位素
同素异形体
同系物
同分异
构体
适用
对象
原子
单质
有机物、无机物
判断
依据
质子数相同,中子数不同
同一种元素的不同单质
①结构相似②通式相同③相对分子质量不同(相差14n)
①分子式相同
②结构不同
电子层结构相同,原子核结构不同
单质的组成和结构不同
相似
不同
性质
化学性质几乎一样,物理性质有差异
化学性质相似,物理性质差别较大
化学性质相似,熔、沸点、密度呈规律性变化
化学性质
可能相似
也可能不
同,物理
性质不同
H、D与T,16O与18O
氧气与臭氧,金刚石与石墨
甲烷与丁烷,乙烷与丙烷
戊烷有正
戊烷、异戊
烷、新戊烷
3种
特别提醒 H2、D2和T2是氢元素的三种核素形成的结构相同的三种单质,它们既不是同位素也不是同素异形体。
重难点六烃的燃烧规律
1.同温同压下,气态烃完全燃烧前后气体体积变化规律
(1)若燃烧后生成的水为液态:
CxHy+(x+)O2xCO2+H2O
(1)
1x+x
ΔV=V前-V后=1+x+-x=1+>0
由此可见,若燃烧后生成的水为液态,燃烧后气体的体积一定减小,燃烧前后气体体积减小值只与烃分子中的氢原子数有关,与碳原子数无关。
(2)若燃烧后生成的水为气态:
CxHy+(x+)O2xCO2+H2O(g)
1x+x
ΔV=V后-V前=x+-1-x-=-1
则烃分子中氢原子数
由此可见,若燃烧后生成的水为气态,气体总体积只与氢原子数有关,可能增大,可能不变,也可能减少。
2.烃完全燃烧时耗氧量规律
烃燃烧通式为CxHy+(x+)O2xCO2+H2O
依上式可得如下规律:
(1)物质的量相同的烃,(x+)越大,耗氧量越多,若两种烃(x+)相等,则耗氧量相同。
(2)质量相同的烃,越大(含氢量越大),则耗氧量越多,若两种烃的相等,质量相等,则耗氧量相同。
(3)质量相同的烃,越大(含碳量越大),则生成的CO2越多,若两种烃的相等,质量相同,则生成的CO2和H2O的量均相等。
特别提醒 烃燃烧通式可用于混合烃平均分子式的计算。
第二节 来自石油和煤的两种基本化工原料
重难点一乙烯的氧化反应和加成反应
1.氧化反应
(1)空气中若含3.4%~34%的乙烯,遇火极易发生爆炸,所以点燃乙烯时要验纯。
(2)当温度高于100℃时,乙烯燃烧前后的混合气体体积相等。
(3)乙烯完全燃烧生成的CO2和H2O的物质的量之比为1∶1。
(4)乙烯使酸性KMnO4溶液褪色,可用于区别CH4(烷烃)和C2H4(烯烃)。
(5)酸性KMnO4溶液可将CH2===CH2最终氧化为CO2,因此当CH4中混有CH2===CH2时,不能用通过酸性KMnO4溶液的办法除去乙烯。
2.加成反应
(1)当乙烯与Br2反应时,一般用溴水或溴的四氯化碳溶液(甲烷需要在光照条件下与溴蒸气反应),且生成的1,2-二溴乙烷是无色液体。
(2)利用乙烯能使溴水褪色而甲烷(或烷烃)不能使溴水褪色,既可以区别乙烯和甲烷(或烷烃),也可以除去甲烷(或烷烃)中混有的乙烯气体以提纯甲烷(或烷烃)。
(3)为制得纯净的氯乙烷,应用乙烯和HCl的加成反应而不宜用乙烷与Cl2的取代反应。
因为乙烯与HCl的加成产物只有一种,而乙烷与Cl2的取代产物是多种氯代烷的混合物。
(4)通常条件下,烯烃不和水反应(可用排水法收集乙烯),但在一定条件下烯烃可以和水反应生成醇(工业上水化法制乙醇的原理)。
(5)乙烯自身的加聚反应可以得到聚乙烯。
应用指南 以上现象经常用作烯烃和其他物质的鉴别或除杂,在高考中经常考查。
在应用时要理解溴水和溴的四氯化碳溶液的区别。
重难点二取代反应和加成反应的比较
名称
加成反应
概念
有机物分子中不饱和碳原子和其他原子或原子团直接结合生成新的化合物的反应
反应前后
分子数目
一般相等
减少
反应特点
①可发生分步取代反应②一上一下
只上不下
特别提醒 取代反应和加成反应是两类重要的有机反应,饱和烃的特征反应是取代反应,不饱和烃的特征反应是加成反应。
重难点三苯的独特结构与性质
1.结构的独特性
(1)苯的分子式
苯的分子式为C6H6,是一种高度不饱和烃。
(2)苯的分子结构
苯分子是一种平面正六边形结构的分子,六个碳原子和六个氢原子位于同一平面上。
(3)苯分子中的碳碳键
苯分子中不存在碳碳单键,也不存在碳碳双键,而是一种介于单键和双键之间的独特的共价键。
2.苯的化学性质方面的体现
(1)苯不能使酸性KMnO4溶液和溴水褪色,由此可知苯在化学性质上与烯烃有很大差别。
(2)苯在催化剂(Fe或FeBr3)作用下与液溴发生取代反应,说明苯具有类似烷烃的性质。
(3)苯又能与H2或Cl2分别在催化作用下发生加成反应,说明苯具有烯烃的性质。
总之,苯易发生取代反应,能发生加成反应,难被氧化,其化学性质不同于烷烃、烯烃。
特别提醒 因苯的凯库勒式为,往往误认为苯分子是单双键交替的结构,其实苯分子中6个碳碳键完全相同,只是一种习惯写法。
重难点四几种烃的性质比较
甲烷
乙烯
苯
结构简式
CH4
CH2===CH2
成键特点
碳碳单键饱和烃
碳碳双键不饱和烃
特殊共价键
化学性质(现象)
燃烧
火焰呈淡蓝色
火焰明亮有黑烟
火焰明亮有大量黑烟
酸性KMnO4溶液
不反应
褪色
溴水
分层,上层呈橙红色,下层为无色
重难点五共线、共面问题
1.典型空间结构
(1)甲烷型:
正四面体凡是碳原子与4个原子形成4个共价键时,其空间结构都是四面体5个原子中最多有3