最新中考化学复习综合计算题试题Word下载.docx
《最新中考化学复习综合计算题试题Word下载.docx》由会员分享,可在线阅读,更多相关《最新中考化学复习综合计算题试题Word下载.docx(6页珍藏版)》请在冰豆网上搜索。
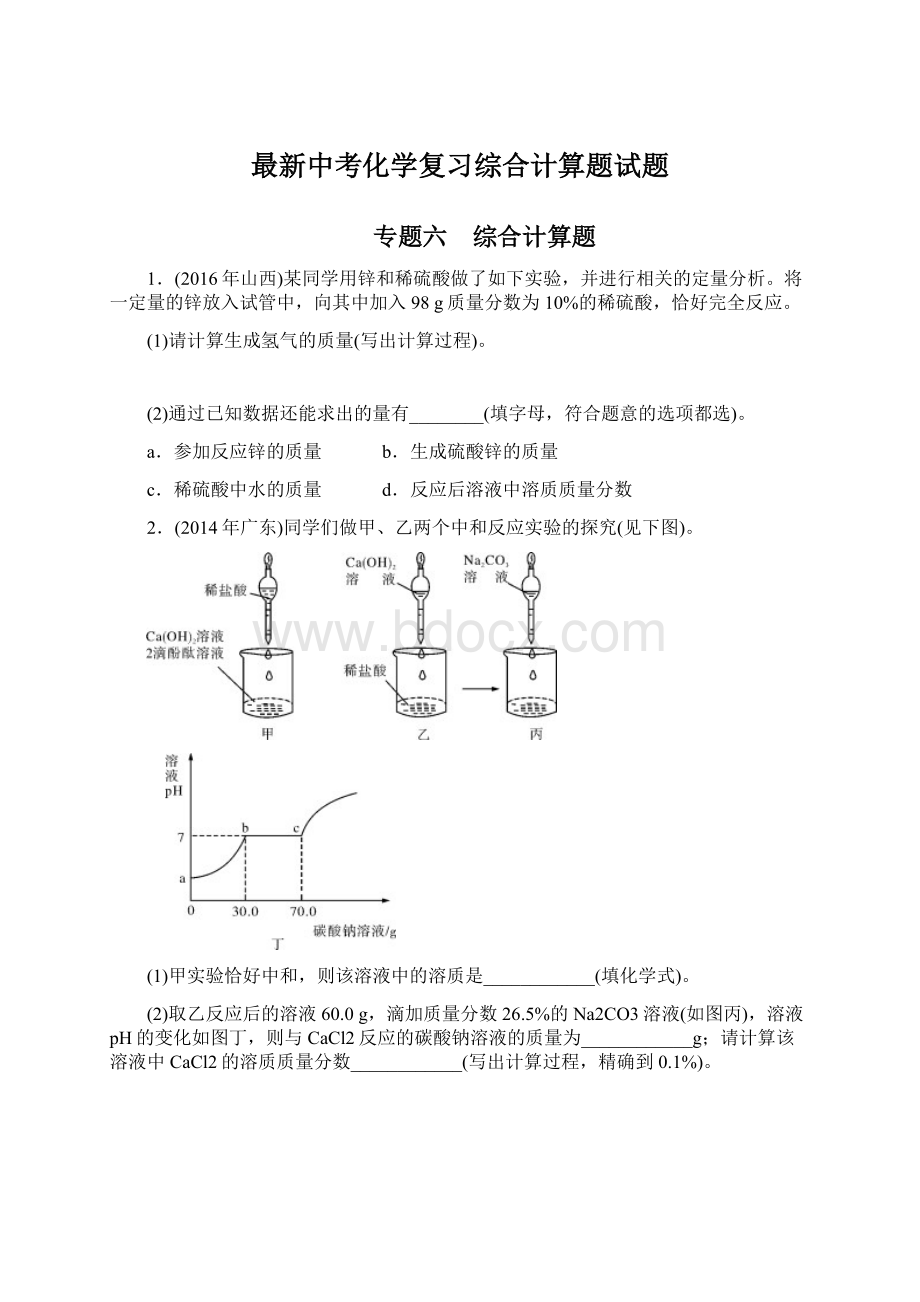
(2)取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液(如图丙),溶液pH的变化如图丁,则与CaCl2反应的碳酸钠溶液的质量为____________g;
请计算该溶液中CaCl2的溶质质量分数____________(写出计算过程,精确到0.1%)。
戊
(3)根据计算所得数据在图戊中画出产生沉淀的曲线。
(4)乙组的中和反应实验设计存在的不足是____________________________。
3.(2016年邵阳)某化学兴趣小组参观了一个石灰厂时,带回了一些石灰石样品,同学们利用这些石灰石样品做了如下实验:
取样品10g放入烧杯中,将50g稀盐酸分5次加入,实验过程所得的数据如表所示(已知石灰石样品中的杂质不参与反应,也不溶于水),根据实验数据计算:
实验次数
加入稀盐酸的质量/g
剩余固体的质量/g
1
10
8
2
6
3
4
5
2
(1)第______次加入稀盐酸充分反应,CaCO3恰好完全反应。
(2)石灰石样品中CaCO3的质量分数=________。
(3)所用稀盐酸中溶质的质量分数(写出计算过程,结果精确到0.1%)。
4.(2016年南昌)小新用20g含碳酸钠53%的天然碱制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应)。
操作过程如下:
请计算:
(1)20g样品中碳酸钠的质量为________g。
(2)反应后所得滤液中氢氧化钠的质量分数为多少?
(写出计算过程)
(3)将200g滤液浓缩成制作“叶脉书签”所需质量分数为10%的氢氧化钠溶液,需蒸发水________g。
5.(2015年揭阳)某铝制品的主要成分是Al和Cu,课外小组将200gNaOH溶液不断地加到50g铝制品中得到如下数据(已知金属铝既可以与强酸反应也可以与强碱反应,而金属铜不能与强碱反应,铝与NaOH溶液反应的化学方程式为:
2Al+2NaOH+2H2O===2NaAlO2+3H2↑)。
实验次数
第一次
第二次
第三次
第四次
加入氢氧化钠溶液的质量/g
50
剩余固体的质量/g
36.5
23
9.5
请回答以下问题:
(1)该50g铝制品中含有____________g铜。
(2)求所用氢氧化钠溶液的溶质质量分数为多少?
6.(2015年茂名)某氢氧化钙粉末中含有碳酸钙杂质。
现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。
(1)生成二氧化碳的质量是____________g。
(2)加入60g稀盐酸后所得溶液中含有的溶质是____________、____________(填化学式)。
(3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%)。
【演练·
专项提升】
1.
(1)98g稀硫酸中含有硫酸的质量=98g×
10%=9.8g。
设生成氢气的质量为x。
Zn+H2SO4===ZnSO4+H2↑
98 2
9.8g x
=
x=0.2g
答:
生成氢气的质量为0.2g。
(2)abcd
2.
(1)CaCl2
(2)由图可知,丙实验中,加入的碳酸钠溶液先与HCl反应,再与CaCl2反应,与CaCl2反应消耗碳酸钠溶液的质量为70.0g-30.0g=40.0g。
设参加反应的CaCl2的质量为x,则
CaCl2+Na2CO3===CaCO3↓+2NaCl
111 106
x 40.0g×
26.5%
解得x=11.1g
该CaCl2溶液的溶质质量分数为:
×
100%≈18.5%。
(3)
(4)无法验证是否恰好中和
解析:
(3)设滴加质量分数26.5%的Na2CO3溶液70.0g时(此时与CaCl2溶液反应的Na2CO3溶液质量为40.0g),生成沉淀的质量为y,则
CaCl2+Na2CO3===CaCO3↓+2NaCl
106 100
40.0g×
26.5% y
解得y=10.0g
由此可绘制生成沉淀的曲线图。
(4)乙组的中和反应实验中没有加酚酞试液,无法验证是否恰好中和。
3.
(1)4
(2)80%
(3)设盐酸的质量分数为x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 73
8g 40g×
x
x=14.6%
盐酸的质量分数为14.6%。
(1)通过分析表中的数据可知,第4次和第5次所得剩余固体的质量相等,说明第4加入稀盐酸与CaCO3恰好完全反应;
(2)石灰石中杂质的质量为2g,则石灰石样品中CaCO3的质量分数为:
100%=80%。
4.
(1)10.6
(2)设滤液中氢氧化钠的质量分数为x。
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
106 80
10.6g 200g×
x=4%
滤液中氢氧化钠的质量分数为4%。
(3)120
(3)设需要蒸发水的质量为y。
200g×
4%=(200g-y)×
10%
y=120g
5.
(1)9.5
(2)50g氢氧化钠溶液消耗金属Al的质量为50g-36.5g=13.5g。
设50g氢氧化钠溶液的溶质质量为x。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑
54 80
13.5g x
= 解得x=20g
则,所用氢氧化钠溶液的溶质质量分数为:
100%=40%
所用氢氧化钠溶液的溶质质量分数为40%。
6.
(1)2.2
(2)CaCl2 HCl
(3)设样品中碳酸钙的质量分数为x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 44
15g×
x 2.2g
= 解得x=33.3%
样品中碳酸钙的质量分数为33.3%。