备战安徽中考化学专题五 实验探究题Word格式文档下载.docx
《备战安徽中考化学专题五 实验探究题Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《备战安徽中考化学专题五 实验探究题Word格式文档下载.docx(31页珍藏版)》请在冰豆网上搜索。
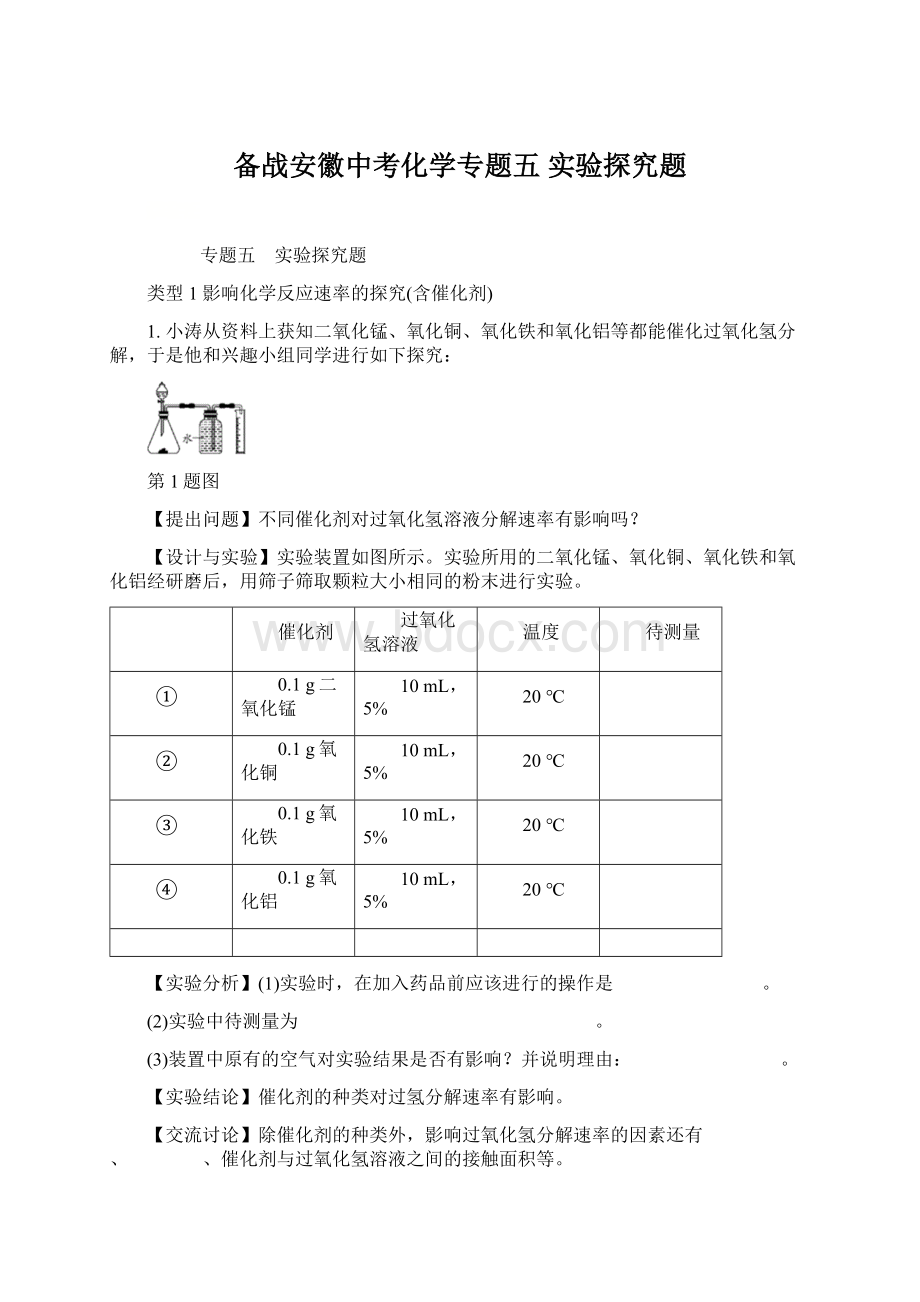
(1)实验时,在加入药品前应该进行的操作是 。
(2)实验中待测量为 。
(3)装置中原有的空气对实验结果是否有影响?
并说明理由:
。
【实验结论】催化剂的种类对过氢分解速率有影响。
【交流讨论】除催化剂的种类外,影响过氧化氢分解速率的因素还有 、 、催化剂与过氧化氢溶液之间的接触面积等。
【拓展反思】下列关于催化剂的认识正确的是 。
A.同一反应可能有不同的催化剂B.催化剂只能是金属氧化物
C.一种物质只能是一个反应的催化剂D.使用催化剂可使不反应的物质间发生反应
2.实验室常用过氧化氢溶液与二氧化锰混合物制取氧气,写出有关反应的化学方程式_____。
【查阅资料】过氧化氢制氧气的催化剂有很多种,如金属氧化物,过氧化氢酶和某些盐类物质等。
【提出问题】硫酸铜溶液能作过氧化氢制氧气的催化剂吗?
如果可以,影响其催化效果的因素有哪些?
【猜想与验证】硫酸铜溶液能作过氧化氢制氧气的催化剂,且其酸碱性对催化效果有影响。
【完成实验】本实验在常温下进行
实验编号
反应物
10mL5%H2O2溶液
无
10mL5%H2O2溶液CuSO4溶液
10滴0.1%
10mL5%H2O2溶液+少量HCl溶液CuSO4溶液
10mL5%H2O2溶液+少量NaOH溶液CuSO4溶液
【分析数据、得出结论】
(1)若证明CuSO4能够加速过氧化氢分解,其验证的实验现象是____________。
(2)若要证明CuSO4是该反应的催化剂,还要验证它在化学反应前后质量和 不变。
第2题图
(3)实验②③④中,测得生成氧气的体积随时间变化的关系如图所示。
分析该图能够得出的实验结论是__________________________________________。
(4)请你再写出一种影响硫酸铜催化效果的因素 。
3.(素材来源:
高中选修1P50)化学兴趣小组的同学对“影响铁钉锈蚀快慢的因素”展开了如下探究:
【提出问题】溶液的酸碱性对铁钉生锈的快慢是否有影响?
溶液中的阴离子种类对铁钉锈蚀的快慢是否有影响?
【设计实验】按图1装置进行实验,测得装置中氯化铵、硫酸铵溶液上方氧气浓度的变化曲线如图2。
图1图2
第3题图
(1)铁钉生锈的条件是__________________________________________。
(2)将规格、材质相同的打磨过的铁钉放入下列不同溶液中,测得有关数据如下表:
溶液中的溶质
氯化铵
硫酸铵
氯化钠
硫酸钠
氢氧化钠
0min时氧气浓度/%
20.8
500min时氧气浓度/%
15.8
17.0
18.6
19.0
19.8
实验前溶液pH
5.31
5.53
7.0
13.6
实验后溶液pH
7.37
7.99
10.5
10.4
13.8
铁钉锈蚀情况
大量铁锈
少量铁锈
几乎无锈
【结论与拓展】①实验中溶液上方氧气浓度变化越大,证明铁锈蚀速率 。
②根据表中数据可知,铁钉在 (填“酸”、“碱”或“中”)性溶液中更易锈蚀,其中铁钉在含有 (填“氯离子”或“硫酸根离子”)的溶液中锈蚀更快。
③图2曲线先陡后平说明铁生锈速率的规律是 。
【拓展应用】化学是把双刃剑,铁制品在使用过程中常常会出现不同程度的锈蚀,会造成 ;
但将铁生锈的原理用于食品脱氧时,要求铁能快速生锈从而达到脱氧的目的,因此食品脱氧剂中除了加入铁粉、炭粉外,还要加入 。
4.某化学兴趣小组为研究石灰石与稀盐酸反应快慢的因素,于是进行了以下探究:
(1)小明设计的实验方案:
取从不同地点取来的石灰石放入等体积不同浓度的稀盐酸中,观察反应的现象。
写出石灰石与稀盐酸反应的化学方程式 。
班级同学对小明设计的实验方案提出质疑,原因是_________________________________________。
【提出猜想】
猜想1:
可能与温度有关;
猜想2:
可能与石灰石颗粒大小有关。
【设计并实验】
小明按照如图实验装置进行实验,并比较20s收集二氧化碳的体积:
温度(℃)
石灰石(1g)颗粒大小
稀盐酸浓度(%)
20s收集二氧化
碳的体积(mL)
20
粉状
10%
56
块状
32
30
89
57
第4题图
(2)实验装置还要增加一个 (填写仪器名称)。
(3)实验中小明通过排出集气瓶中的水来测出二氧化碳的体积,为了减少二氧化碳溶解在水中,还应该在水中倒入少量 。
【得出结论】
(4)通过实验中①②对比,得出的结论是 ;
若比较温度对该反应的影响,可以通过实验 (写实验编号)对比。
[注意:
若答对(5)(6)两小题奖励4分,化学试卷总分不超过60分。
]
【交流与反思】
(5)除了上述比较的方法外,还有比较快慢的方法是___________________。
(6)石灰石与稀盐酸反应的快慢可能还受哪些因素影响?
设计实验验证。
_______________________________。
5.(2019合肥市瑶海区二模)为研究“影响金属与盐酸反应剧烈程度的因素”,兴趣小组同学进行如下探究。
(1)
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出假设】Ⅰ.可能与金属本身的性质有关;
Ⅱ.可能与盐酸的浓度有关;
Ⅲ. (请你填写一个合理的猜想)。
(2)
【实验探究】实验所用金属均已用砂纸打磨。
①实验一:
为探究猜想Ⅰ,小红同学分别在两支试管中放入相同质量的锌和铁,然后分别加入同体积、同浓度的稀盐酸,观察到放锌的试管中立即产生大量气泡,放铁的试管中只产生少量气泡,由此得出结论:
金属活动性Zn>
Fe。
你认为实验一方案是否合理 ,理由是_____________ 。
②实验二:
为探究猜想Ⅱ,小军同学利用下列图1装置进行对照实验,做了等质量且过量的锌片分别与等体积、浓度为5%、15%的稀盐酸反应。
其中注射器的作用是 ;
该装置气密性的检查方法是 。
图1图2 图3
第5题图
③实验三:
小军同学还用压强传感器替换注射器进行数字化实验,测得两次实验压强随时间的变化关系曲线如上述图2所示。
请你根据该图中信息得出两条合理结论:
;
。
【拓展延伸】[注意:
若答对下列小题奖励4分,化学试卷总分不超过60分。
(3)已知一种金属加入到比它弱的两种金属盐溶液的混合液中,先置换出最弱的金属。
小敏同学向一定质量的硝酸银和硝酸铜的混合溶液中加入锌粉,溶质质量与加入锌的质量关系如图3所示。
那么,在A点时,溶液里含有盐有 种;
BC段发生的化学反应方程式为 ;
D点得到的固体的成分为 。
类型2 反应后物质成分的探究
6.实验室常用加热氯酸钾和二氧化锰的混合物制备氧气。
某兴趣小组在实验时发现了一个奇怪的现象——有刺激性气味的气体产生。
请你一起参与探究。
(1)请你写出用氯酸钾和二氧化锰制氧气的化学方程式 。
【提出问题】刺激性气味是什么?
【猜想与假设】猜想一:
臭氧(O3)猜想二:
氯气(Cl2)猜想三:
HCl
(2)有位同学说猜想 不需要设计实验验证就可以判断是错误的,请你说明理由 。
【查阅资料】a.氯气通入水中会发生反应:
Cl2+H2O===HCl+HClO(次氯酸);
b.臭氧在二氧化锰存在的情况下极易分解产生氧气;
c.酸性气体可以使湿润的蓝色石蕊试纸变红。
(3)通过分析查阅资料可以得出猜想 错误。
第6题图
【实验探究】
(4)取氯酸钾和二氧化锰的混合物放入试管中加热,如图所示。
将蘸有硝酸银溶液的玻璃棒伸入试管口,看到 现象,再将湿润的蓝色石蕊试纸伸到试管口,试纸变为 色。
【得出结论】猜想二成立。
7.(2019自贡)某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②白色无水CuSO4粉末遇水变蓝色;
③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
CO2、H2O猜想二:
CO、H2O猜想三:
CO2、CO、H2O
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
第7题图
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想 成立。
(2)实验过程中B装置的作用是 ;
该反应的化学方程式是 。
(3)D装置中发生反应的化学方程式是 。
(4)实验过程中用纯净O2而不用空气的原因是 。
(5)实验过程中B、C装置的顺序不能颠倒,原因是 。
【反思与交流】日常生活中,使用含碳燃料一定要注意通风,防止 中毒。
8.(素材来源:
高中必修2P89)如图所示,“铝热反应”指铝和氧化铁的反应:
2Al+Fe2O3Al2O3+2Fe,常用于焊接铁轨。
过程:
引燃镁条,漏斗内物质熔化,大量熔融物落下。
第8题图1
(1)氧化铁和铝都用粉末状的,目的是 。
(2)某学习兴趣小组对所得熔融物的成分进行了探究。
【查阅资料】①铝能和氢氧化钠溶液反应产生偏铝酸钠(NaAlO2)和氢气;
②铁可以被磁铁吸引,铝不能被磁铁吸引。
【猜想假设】同学们猜测铝热反应所得到的熔融物中的金属是:
假设一:
铁 假设二:
铁和铝的混合物
(3)
【进行实验】同学们设计以下实验方案验证猜想。
实验步骤
实验现象
实验结论
取少量冷却后的熔融物于石棉网上,用磁铁吸引
熔融物能够被吸引
假设二正确
取少量冷却后的熔融物于试管中,加入
请写出铝与氢氧化钠溶液反应的化学方程式为 。
(4)
【拓展延伸】为进一步了解铝的化学性质。
如图2是小铭将一根铝丝与过量的稀盐酸混合在一密闭容器内,利用压强和温度传感器测出的反应变化过程(