中考化学试题分类汇编工艺流程题Word文档下载推荐.docx
《中考化学试题分类汇编工艺流程题Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《中考化学试题分类汇编工艺流程题Word文档下载推荐.docx(37页珍藏版)》请在冰豆网上搜索。
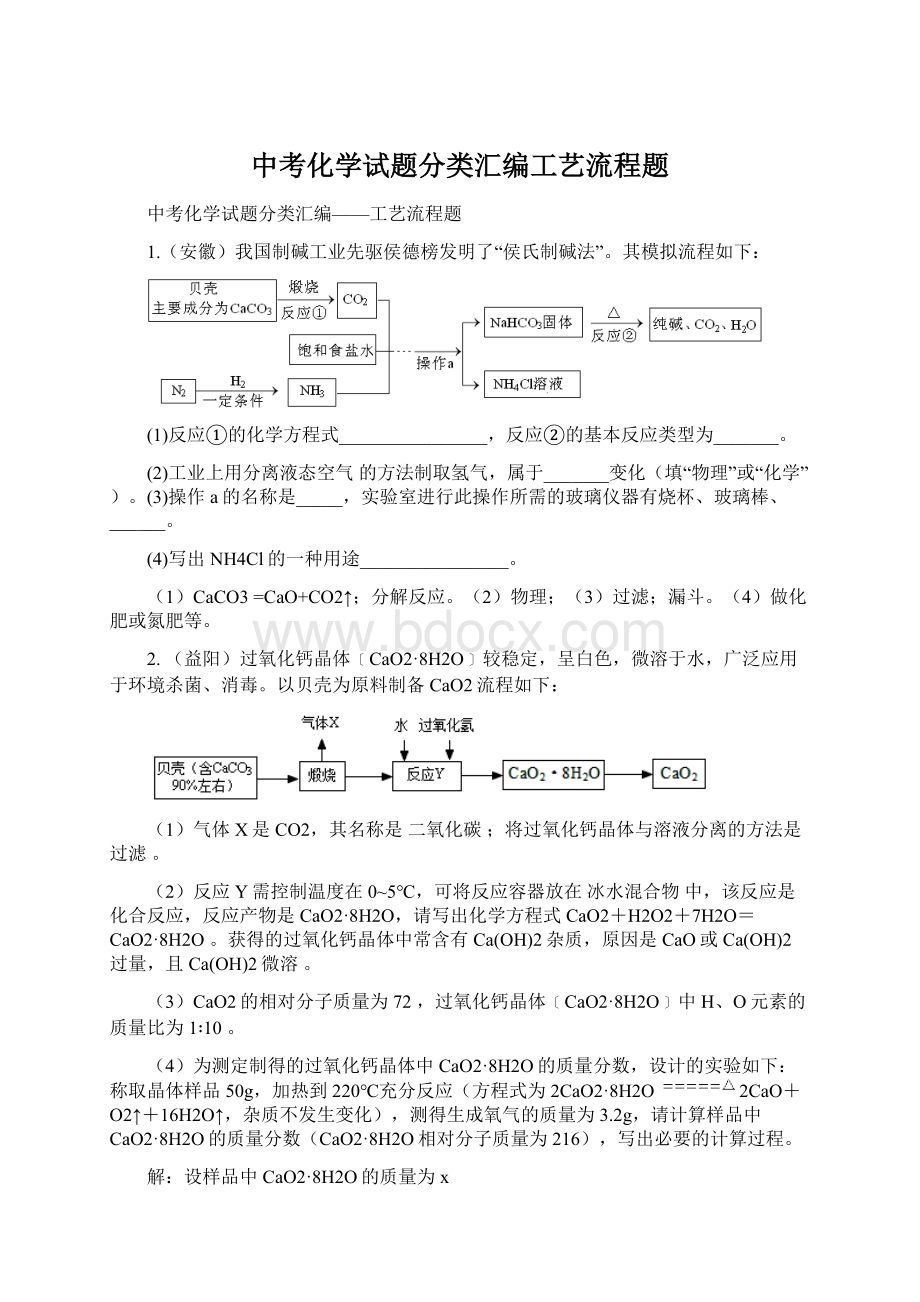
8H2O,请写出化学方程式CaO2+H2O2+7H2O=CaO2·
8H2O。
获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是CaO或Ca(OH)2过量,且Ca(OH)2微溶。
(3)CaO2的相对分子质量为72,过氧化钙晶体﹝CaO2·
8H2O﹞中H、O元素的质量比为1∶10。
(4)为测定制得的过氧化钙晶体中CaO2·
8H2O的质量分数,设计的实验如下:
称取晶体样品50g,加热到220℃充分反应(方程式为2CaO2·
8H2O2CaO+O2↑+16H2O↑,杂质不发生变化),测得生成氧气的质量为3.2g,请计算样品中CaO2·
8H2O的质量分数(CaO2·
8H2O相对分子质量为216),写出必要的计算过程。
解:
设样品中CaO2·
8H2O的质量为x
2CaO2·
8H2O2CaO+O2↑+16H2O↑
43232
x3.2
∴x=43.2(g)
∴样品中CaO2·
8H2O的质量分数为=86.4%
答:
样品中CaO2·
3.(呼和浩特)空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。
下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。
请按要求回答下列问题:
(1)步骤①中发生的是________变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的化学方程式_________________________________。
硝酸铵
化学式:
NH4NO3
含氮量:
≥30%
注意事项:
密封储存
防潮防晒
隔绝热源
……
(3)上述化学反应中属于化合反应的有________个。
(4)右图是化肥硝酸铵包装袋上的部分说明:
硝酸铵应具有的性质是 (填字母)。
A.易溶于水B.有挥发性C.受热易分解
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与
熟石灰反应的化学方程式__________________________________。
1)物理
(2)4NH3+5O2=4NO+6H2O
(3)3
(4)AC2NH4NO3+Ca(OH)2=Ca(NO3)2+2H2O+2NH3↑
4.(宜宾)黄铜是Zn以主要添加元素的铜合金。
黄铜渣中约含Zn
7%、ZnO
31%、Cu
50%、CuO
5%,其余为杂质。
处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
已知:
ZnO+H2SO4=ZnSO4+H2O;
CuO+H2SO4=CuSO4+H2O
(1)
步骤Ⅰ中产生气体的化学方程式为
。
(2)
溶液A中的金属阳离子有
(填化学式)
(3)
步骤Ⅰ、Ⅱ中均包含的操作名称为
,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是
(4)溶液A
(填“大于”、“小于”或“等于”)溶液C的质量。
5.(南昌)炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如下,下列有关说法错误的是()
A.操作1中粉碎的目的是增大反应物的接触面积
高温
B.操作2中,CuS、NaCl和O2在高温条件下反应生产CuCl2和Na2SO4
化学方程式为CuS+2NaCl+2O2===CuCl2+Na2SO4
C.操作3的名称是过滤
D.流程图中能循环利用的物质是NaCl和Na2SO4
6.(扬州)醋酸钙[Ca(AC)2]是国家允许使用的补钙制剂之一。
以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如下。
写出煅烧时的化学方程式。
CO2的任意排放会引发的环境问题是。
CO2与CH4一定条件下化合生成甲醛(HCHO),则此反应中与最佳质量比是。
下列做法能减少二氧化碳排放的是。
(填序号)
在反应中制备石灰乳,而不是制备澄清石灰水的目的是。
写出熟石灰的一种用途
在反应中醋酸过量的目的是。
写出反应的化学方程式。
膜分离时,盐酸不能过量的主要原因是。
根据煅烧产生的CO2和蛋壳的主要成分为CaCO3,可以确定化学方程式。
CO2的任意排放会引发温室效应;
根据,计算CO2与CH4的质量比是44:
16=11:
4。
石灰乳中的Ca(OH)2含量比澄清石灰水中多,更利于提高醋酸钙的产量;
保证与Ca(OH)2完全反应,提高醋酸钙的含量;
加入盐酸就是为了将蛋壳与膜分开,过量的话会与CaCO3反应,会使制作醋酸钙的原料量减少。
7.(扬州)含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途
.以含锌废渣(主要成分为ZnO,杂质为FeO﹑CuO)为原料制备七水硫酸锌(ZnSO4·
7H2O)的流程如下。
粉碎的目的是。
若实验室用质量分数为98%的硫酸配制200g25%的硫酸,需要的玻璃仪器有胶头滴管﹑玻璃棒﹑和,此处玻璃棒的作用是。
物质X是,滤渣中含有的金属单质有,除铜时发生的反应属于反应(填基本反应类型)
流程中获得七水硫酸锌前省略的操作是﹑冷却结晶﹑洗涤和低温烘干。
某温度下,Fe(OH)3分解得到一种铁﹑氧质量比21:
8的氧化物,该氧化物的化学式。
除铁过程中,温度pH对除铁效果的影响分别对如图所示。
由图可知,除铁时温度应控制在℃为宜,pH应控制在为宜。
.以某菱锌矿(ZnCO3含量为62.5%)为原料制备锌的原理如下(假设杂质不参加反应):
则100吨这样的菱锌矿理论上最多制得锌多少吨?
(写出计算过程)
固体的表面积越大,化学反应速率越快。
含锌废渣粉碎的目的是增大接触面积,加快反应速率,充分反应。
浓硫酸稀释过程中需用用到:
量筒、滴管、细口瓶、玻璃棒和烧杯,通过比较可知,还缺少烧杯和量筒。
此处玻璃棒的作用是搅拌,将热量及时地扩散。
加入过量的X,目的是除去铜,本小题实质是物质的除杂,既要除去杂质又要避免引入新的杂质,考虑到金属活动性顺序,故X可以是锌,滤渣含有锌和置换的铜,这个反应过程是置换反应。
这是分离可溶性固体和液体的方法:
先将热的饱和溶液冷却,晶体就会析出,将此有晶体析出的饱和溶液,过滤,用少量的水洗涤,再低温烘干。
所以操作的步骤是:
加热浓缩,冷却结晶,过滤,洗涤和低温烘干
Fe(OH)3分解得到一种铁﹑氧质量比21:
8的氧化物,铁的氧化物有三种,Fe2O3,FeO,Fe3O4.比较铁氧的质量比21:
8只有Fe3O4符合题意。
关键看懂两张图的X轴和Y轴代表的含义,为了除铁效果最佳,我们需要找出最高除铁率对应的温度和pH.
.题目要求求出理论上最多制得锌多少吨
故设理论上最多制得锌的质量为X,
根据题意可知ZnCO3的质量是=100t×
62.5%=62.5t
由两个方程式可知道
ZnCO3~Zn
12565
62.5tXx=32.5t
8.(雅安)绿矾又名七水硫酸亚铁(FeSO4·
7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等。
绿矾(FeSO4·
7H2O)的一种综合利用工艺如下:
(1)细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式。
(2)绿矾与NH4HCO3在溶液中反应,有CO2生成,反应的化学方程式为。
隔绝空气进行“焙烧”,铁元素的转化途径是,实际作还原剂的是CO。
写出“焙烧”过程中各步反应的化学方程式:
A.;
B.____________________________________________;
C.____________________________________________。
4.母液“除杂”后,欲得到(NH4)2SO4粗产品,操作步骤依次为蒸发浓缩、____________、过滤、洗涤、干燥。
(1)3Fe+2O2Fe3O4(2分)
(2)FeSO4·
7H2O+2NH4HCO3=FeCO3
+(NH4)2SO4
+CO2↑+8H2O(2分)
(3)CO2+C2CO(2分)FeO+COFe+CO2(2分)
(4)降温结晶(或冷却热的饱和溶液)(2分)
9.(厦门)黄铜矿(主要万分CuFeS2)经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4。
某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。
主要步骤如图7所示:
(1)Fe2(SO4)3与铁反应的化学方程式:
xFe2(SO4)3+yFe=zFeSO4,其中x、y、z为化学计量数,z的值为_____________。
(2)步骤Ⅰ中,生成铜的化学方程式:
__________________________。
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是__________________
__________________________________。
(4)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是_____________(填化学式)。
(5)步骤Ⅲ回收铜的方法为_______________________________________。
(1)3
(2)Fe+CuSO4=Cu+FeSO4(3)铁锈与硫酸反应生成硫酸铁(2分)
(4)Na2CO3(或其他合理答案,2分)(5)加入过量的稀硫酸,过滤、洗涤、干燥
10.(广东)现有工厂丢弃的废铜屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。
课外活动小
组同学欲利用其制取胆矾,他们设计了下面的两种制取流程。
已知Cu+Fe2(SO4)3=2FeSO4+CuSO4,请回答:
(1)铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称,操作①所用到的玻璃仪器有:
烧杯、玻璃棒和。
(2)溶液A的溶质有(只写一种);
铁锈与稀硫酸反应的化学方程式为:
。
(3)两种方法比较,符合绿色化学要求的是方法;
方法II的化学方程式为:
2Cu+2H2SO4+=2CuSO4+,操作②实验步骤为:
,降温结晶。
11.(佛山)现代循环经济要求综合考虑环境污染和经济效益。
高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:
[(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解]。
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、等。
(2)滤液Ⅰ中主要