中考化学专题训练卷气体的制取净化与干燥详解.docx
《中考化学专题训练卷气体的制取净化与干燥详解.docx》由会员分享,可在线阅读,更多相关《中考化学专题训练卷气体的制取净化与干燥详解.docx(18页珍藏版)》请在冰豆网上搜索。
中考化学专题训练卷气体的制取净化与干燥详解
2015年中考化学专题训练卷:
气体的制取、净化与干燥
一、选择题(共5小题,每小题3分,满分15分)
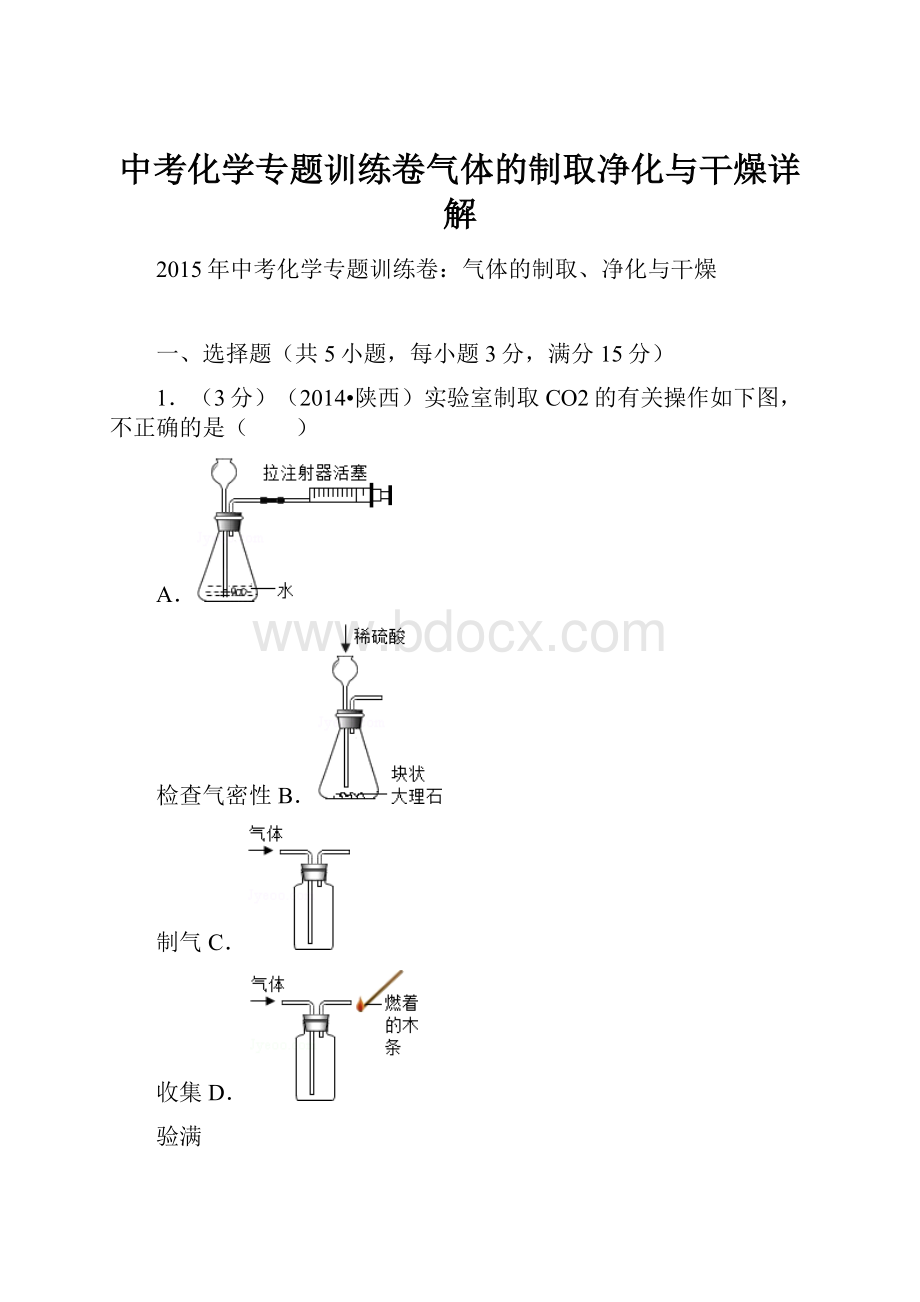
1.(3分)(2014•陕西)实验室制取CO2的有关操作如下图,不正确的是( )
A.
检查气密性B.
制气C.
收集D.
验满
2.(3分)(2014•南昌)实验室可用于氯酸钾制取氧气的装置组合是( )
A.①④B.②③C.①⑤D.②⑤
3.(3分)(2014•益阳)下面是实验室依次制备,收集,验证、验满CO2的装置,其中正确的是( )
A.
B.
C.
D.
4.(3分)(2014•厦门)已知氨气是极易溶于水、密度比空气小的气体,用试管收集氨气,可选用的装置是( )
A.
B.
C.
D.
5.(3分)(2015•聊城)如图所示装置(不可倒置)有多种用途,下列叙述正确的是( )
A.若用排空气法收集CO2(密度比空气大)时,气体应从A端通入
B.若用排空气法收集氧气时,气体从B端通入
C.若用排空气法收集H2时,气体应从A端通入
D.若用水将此装置中的O2排出,水应从B端进入
二.填空题
6.(3分)(2015•巴彦淖尔一模)化学实验是进行科学探究的重要方式.某化学小组选用下图装置和药品进行探究实验.
(1)A中反应的化学方程式为______
(2)若将A、B连接,A中产生的气体并不能使B中的溶液变浑浊,原因是______
(3)若要制取一瓶纯净、干燥的CO2,所选用装置的导管连接口从左到右的正确连接顺序为:
a接______、______接______、______接______.
7.(3分)(2014•东营)如图1是实验室制取氧气或二氧化碳时经常用到的仪器,请回答有关问题.
(1)写出编号仪器名称:
①______;⑧______.
(2)当制取较多量CO2时,制取装置的仪器组合是______(选填序号).
(3)阅读材料回答问题.资料:
1氨气是有刺激性气味的无色气体,密度比空气小,极易溶于水,其水溶液显碱性.
2加热熟石灰和氯化铵的固体混合物生成氨气.
3湿润的红色石蕊试纸遇到氨气变蓝色;氨气遇到浓盐酸时冒白烟(生成NH4Cl固体)
I、制取氨气的装置与实验室用______(选填“高锰酸钾”或“双氧水”)制氧气的装置相同,还缺少的仪器名称是______,检查该装置气密性的方法是______.
Ⅱ、若用如图2装置收集氨气,进气口应为______端(选填“m”或“n”),检验氨气集满的方法是______.
(4)加热是最常见的反应条件,用酒精灯给试管中的固体加热时,试管口稍向下倾斜的原因是______.
8.(3分)(2014•菏泽)实验室制取气体时需要的一些装置如图所示,请回答下列问题:
(1)实验室里用A装置制取氧气的化学方程式为:
______,可选择的收集装置有______,若要得到干燥的氧气,所选择的连接顺序为______→______→______.
(2)某同学利用上述B装置,用贝壳和盐酸反应生成了一种无色气体,请你设计实验方案,应用化学方法检验生成的气体为二氧化碳.(要求写出操作过程、使用试剂和实验现象)______.
9.(3分)(2014•安徽)某化学兴趣小组设计了一组“吹气球”实验,三套装置如图:
(1)甲装置:
①仪器a的名称为______;
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性______.
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是______.
②若生成H2使气球胀大,则反应的化学方程式为______.
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是______.
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是______.
2015年中考化学专题训练卷:
气体的制取、净化与干燥
参考答案与试题解析
一、选择题(共5小题,每小题3分,满分15分)
1.(3分)(2014•陕西)实验室制取CO2的有关操作如下图,不正确的是( )
A.
检查气密性B.
制气C.
收集D.
验满
【分析】A、要熟悉各种仪器的名称、用途和使用方法;
B、实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
C、根据根据气体的密度可以选择收集的方法;
D、二氧化碳不能燃烧,不支持燃烧.
【解答】解:
A、检查装置气密性时,拉动注射器时,如果长颈漏斗末端产生气泡,说明装置不漏气,反之则漏气,该选项正确;
B、实验室不能用稀硫酸和大理石制取CO2,因为产物CaSO4是微溶物,会附着在大理石表面,阻止了反应的进一步进行,该选项不正确;
C、二氧化碳的密度比空气大,进气导管应该接近集气瓶底部,该选项正确;
D、因为二氧化碳不能燃烧,不支持燃烧,可以用燃烧的木条验满,该选项正确.
故选:
B.
【点评】实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.
2.(3分)(2014•南昌)实验室可用于氯酸钾制取氧气的装置组合是( )
A.①④B.②③C.①⑤D.②⑤
【分析】依据反应物的状态和反应条件选择发生装置,依据氧气的密度和溶解性选择收集装置.
【解答】解:
氯酸钾晶体和二氧化锰粉末制取氧气需要加热,属于固体加热型,故选发生装置①;氧气的密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,收集装置为③或⑤.
故选C.
【点评】本考点主要考查气体的制取装置和收集装置的选择,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.
3.(3分)(2014•益阳)下面是实验室依次制备,收集,验证、验满CO2的装置,其中正确的是( )
A.
B.
C.
D.
【分析】实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大,能使澄清石灰水变浑浊,不能燃烧,不支持燃烧.
【解答】解:
A、装置中的长颈漏斗末端在液面以上,会导致生成的二氧化碳从长颈漏斗逸出,该选项不正确;
B、二氧化碳的密度比空气大,不能用向下排空气法收集,该选项不正确;
C、验证二氧化碳时,应该把气体通入澄清石灰水中,如果澄清石灰水变浑浊,说明是二氧化碳,不能把燃烧的木条伸入集气瓶中,因为氮气、氦气等气体都能够使燃烧的木条熄灭,该选项不正确;
D、把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满二氧化碳,该选项正确.
故选:
D.
【点评】实验室制取、收集气体时,要根据反应物的性质、生成气体的性质合理选择发生装置和收集装置及其验满方法.
4.(3分)(2014•厦门)已知氨气是极易溶于水、密度比空气小的气体,用试管收集氨气,可选用的装置是( )
A.
B.
C.
D.
【分析】从氨气是极易溶于水,所以不能用排水法收集、密度比空气小的气体,所以可用向下排空气法收集去分析解答.
【解答】解:
由于氨气是极易溶于水,所以不能用排水法收集、密度比空气小的气体,所以可用向下排空气法收集.
A、收集氨气不能用向上排空气法,同时导管也没有伸到试管底部;故A错误;
B、收集氨气不能用排水法收集;故B错误;
C、收集氨气不能用向上排空气法,故C错误;
D、氨气能用向下排空气法收集;故D正确.
故答案为:
D.
【点评】实验室制取气体时,收集装置的选择取决于水溶性和气体的密度.
5.(3分)(2015•聊城)如图所示装置(不可倒置)有多种用途,下列叙述正确的是( )
A.若用排空气法收集CO2(密度比空气大)时,气体应从A端通入
B.若用排空气法收集氧气时,气体从B端通入
C.若用排空气法收集H2时,气体应从A端通入
D.若用水将此装置中的O2排出,水应从B端进入
【分析】根据已有的知识进行分析解答,使用此瓶采用排空气法收集气体,若是密度大于空气的气体,从长管进,若是密度小于空气的气体,从短管进,只要是将瓶内的水排出,则从短管进;用水将瓶内的气体排出,则从长管进水,据此解答.
【解答】解:
A、二氧化碳的密度大于空气,若用排空气法往装置内收集CO2时,气体应从A端通入,正确;
B、氧气的密度大于空气,若用排空气法往装置内收集O2时,气体应从A端通入,错误;
C、氢气的密度小于空气,若用排空气法往装置内收集H2时,气体应从B端通入,错误;
D、若用水将此装置中的O2排出,水应从A端进入,错误;
故选A.
【点评】本考点考查了气体的收集方法,要记忆常用气体的性质,理解应用.本考点考查了学生的实验设计能力、分析能力和实验评价能力,希望同学们认真把握.
二.填空题
6.(3分)(2015•巴彦淖尔一模)化学实验是进行科学探究的重要方式.某化学小组选用下图装置和药品进行探究实验.
(1)A中反应的化学方程式为 CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)若将A、B连接,A中产生的气体并不能使B中的溶液变浑浊,原因是 浓盐酸易挥发,因此生成的CO2中混有HCl气体,使B中不能生成CaCO3沉淀
(3)若要制取一瓶纯净、干燥的CO2,所选用装置的导管连接口从左到右的正确连接顺序为:
a接 g 、 f 接 e 、 d 接 h .
【分析】
(1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据浓盐酸具有挥发性进行分析;
(3)根据浓硫酸具有吸水性,碳酸氢钠溶液能吸收氯化氢气体等知识进行分析.
【解答】解:
(1)石灰石中的碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:
CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)浓盐酸具有挥发性,导致制取的二氧化碳中混有氯化氢气体,氯化氢能与氢氧化钙反应;
(3)先用碳酸氢钠溶液除去二氧化碳中混有的氯化氢气体,再用浓硫酸除去二氧化碳的水蒸气,最后用向上排空气法来收集,注意气体的长进短出.
故答案为:
(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)浓盐酸易挥发,因此生成的CO2中混有HCl气体,使B中不能生成CaCO3沉淀;
(3)gfedh.
【点评】本题综合性较强,既考查了仪器使用的注意事项、实验室制取二氧化碳的过程,又考查了废液的处理、根据化学方程式的计算,难度适中.
7.(3分)(2014•东营)如图1是实验室制取氧气或二氧化碳时经常用到的仪器,请回答有关问题.
(1)写出编号仪器名称:
① 集气瓶 ;⑧ 长颈漏斗 .
(2)当制取较多量CO2时,制取装置的仪器组合是 ①②⑦⑧ (选填序号).
(3)阅读材料回答问题.资料:
1氨气是有刺激性气味的无色气体,密度比空气小,极易溶于水,其水溶液显碱性.
2加热熟石灰和氯化铵的固体混合物生成氨气.
3湿润的红色石蕊试纸遇到氨气变蓝色;氨气遇到浓盐酸时冒白烟(生成NH4Cl固体)
I、制取氨气的装置与实验室用 高锰酸钾 (选填“高锰酸钾”或“双氧水”)制氧气的装置相同,还缺少的仪器名称是 酒精灯 ,检查该装置气密性的方法是 仪器组装好后,将导管的一端放入水中,再用双手握住试管,若导管口有气泡冒出,说明装置的气密性良好 .
Ⅱ、若用如图2装置收集氨气,进气口应为 n 端(选填“m”或“n”),检验氨气集满的方法是 将湿润的红色石蕊试纸放在m管口,若变蓝则已满 .
(4)加热是最常见的反应条件,用酒精灯给试管中的固体加热时,试管口稍向下倾斜的原因是 防止加热产生的水蒸气在管口处冷凝成水,倒流造成试管炸裂 .
【分析】
(1)要熟悉各种仪器的名称、用途和使用方法;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(4)用酒精灯给试管中的固体加热时,试管口稍向下倾斜能够防止水蒸气冷凝回流.
【解答】解:
(1)①是集气瓶,常用来收集气体;⑧是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品.
故填:
集气瓶;长颈漏斗.
(2)当制取较多量CO2时,应该用锥形瓶作为反应容器,制取装置的仪器组合是:
利用集气瓶①收集二氧化碳,利用带导管的双孔橡皮塞②、锥形瓶⑦和长颈漏斗⑧制取二氧化碳.
故填:
①②⑦⑧.
(3)I、制取氨气的装置与实验室用高锰酸钾制氧气的装置相同,这是因为反应物都是固体,都需要加热;
还缺少的仪器名称是酒精灯,酒精灯用作热源;
检查该装置气密性的方法是:
仪器组装好后,将导管的一端放入水中,再用双手握住试管,若导管口有气泡冒出,说明装置的气密性良好.
故填:
高锰酸钾;酒精灯;仪器组装好后,将导管的一端放入水中,再用双手握住试管,若导管口有气泡冒出,说明装置的气密性良好.
II、若用如图2装置收集氨气,因为氨气的密度比空气小,所以进气口应为n;
检验氨气集满的方法是:
将湿润的红色石蕊试纸放在m管口,若变蓝则已满.
故填:
n;将湿润的红色石蕊试纸放在m管口,若变蓝则已满.
(4)用酒精灯给试管中的固体加热时,试管口稍向下倾斜的原因是:
防止加热产生的水蒸气在管口处冷凝成水,倒流造成试管炸裂.
故填:
防止加热产生的水蒸气在管口处冷凝成水,倒流造成试管炸裂.
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.
8.(3分)(2014•菏泽)实验室制取气体时需要的一些装置如图所示,请回答下列问题:
(1)实验室里用A装置制取氧气的化学方程式为:
2KClO3
2KCl+3O2↑ ,可选择的收集装置有 C、E ,若要得到干燥的氧气,所选择的连接顺序为 A → F → E .
(2)某同学利用上述B装置,用贝壳和盐酸反应生成了一种无色气体,请你设计实验方案,应用化学方法检验生成的气体为二氧化碳.(要求写出操作过程、使用试剂和实验现象) 把生成的气体通入到盛有少量澄清石灰水的试管中(或洗气瓶中),若溶液变浑浊(或有白色沉淀生成),证明生成的气体是二氧化碳. .
【分析】
(1)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;氧气的密度比空气的密度大,不易溶于水;浓硫酸具有吸水性,可以用来干燥氧气;
(2)贝壳的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊.
【解答】解:
(1)实验室里用A装置制取氧气时,试管口没有塞一团棉花,应该是利用氯酸钾制取氧气,反应的化学方程式为:
2KClO3
2KCl+3O2↑;
因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集;
若要得到干燥的氧气,所选择的连接顺序为:
通过A装置产生的氧气进入F装置中,通过浓硫酸干燥的氧气再通过E装置收集起来.
故填:
2KClO3
2KCl+3O2↑;C、E;A;F;E.
(2)应用化学方法检验生成的气体为二氧化碳的实验步骤、实验现象、实验结论分别为:
把生成的气体通入到盛有少量澄清石灰水的试管中(或洗气瓶中),若溶液变浑浊(或有白色沉淀生成),证明生成的气体时二氧化碳.
故填:
把生成的气体通入到盛有少量澄清石灰水的试管中(或洗气瓶中),若溶液变浑浊(或有白色沉淀生成),证明生成的气体是二氧化碳.
【点评】实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.
9.(3分)(2014•安徽)某化学兴趣小组设计了一组“吹气球”实验,三套装置如图:
(1)甲装置:
①仪器a的名称为 长颈漏斗 ;
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性 良好 .
(2)乙装置:
①若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是 二氧化锰 .
②若生成H2使气球胀大,则反应的化学方程式为 Zn+H2SO4═ZnSO4+H2↑ .
③若锥形瓶中装有NaOH固体,分液漏斗中加入少量水,则气球胀大的主要原因是 NaOH固体溶于水放热,空气受热膨胀 .
(3)丙装置:
若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是 NaOH溶液 .
【分析】
(1)根据仪器的名称和检查气密性的方法进行分析;
(2)根据氧气的实验室制法、氢气的实验室制法以及氢氧化钠的性质进行分析;
(3)丙中CO2气体被吸收时,装置内压强减小,内部的气球就会胀大,据此分析.
【解答】解:
(1)①仪器a的名称为长颈漏斗;
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性良好.
(2)①该装置是固液在常温下制取气体的装置,若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是催化剂二氧化锰,倒入的液体是过氧化氢溶液;
②锌和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
③氢氧化钠溶于水放出大量的热,装置内气压增大,气球胀大.
(3)丙中CO2气体被吸收时,装置内压强减小,内部的气球就会胀大,氢氧化钠溶液可吸收二氧化碳气体.
故答案为:
(1)①长颈漏斗;②良好;
(2)①二氧化锰;②Zn+H2SO4=ZnSO4+H2↑;③NaOH固体溶于水放热,空气受热膨胀;(3)NaOH溶液.
【点评】此题的难度不大,掌握实验室制取氧气、氢气的原理以及氢氧化钠的性质等即可顺利解答此题.
参与本试卷答题和审题的老师有:
fqk;sdlbsh;200808;xiaoxi;947423253;起点线(排名不分先后)
菁优网
2016年10月4日