FDA批准的激酶小分子抑制剂类药物及分类一览.docx
《FDA批准的激酶小分子抑制剂类药物及分类一览.docx》由会员分享,可在线阅读,更多相关《FDA批准的激酶小分子抑制剂类药物及分类一览.docx(11页珍藏版)》请在冰豆网上搜索。
FDA批准的激酶小分子抑制剂类药物及分类一览
FDA批准的激酶小分子抑制剂类药物及分类一览
蛋白激酶
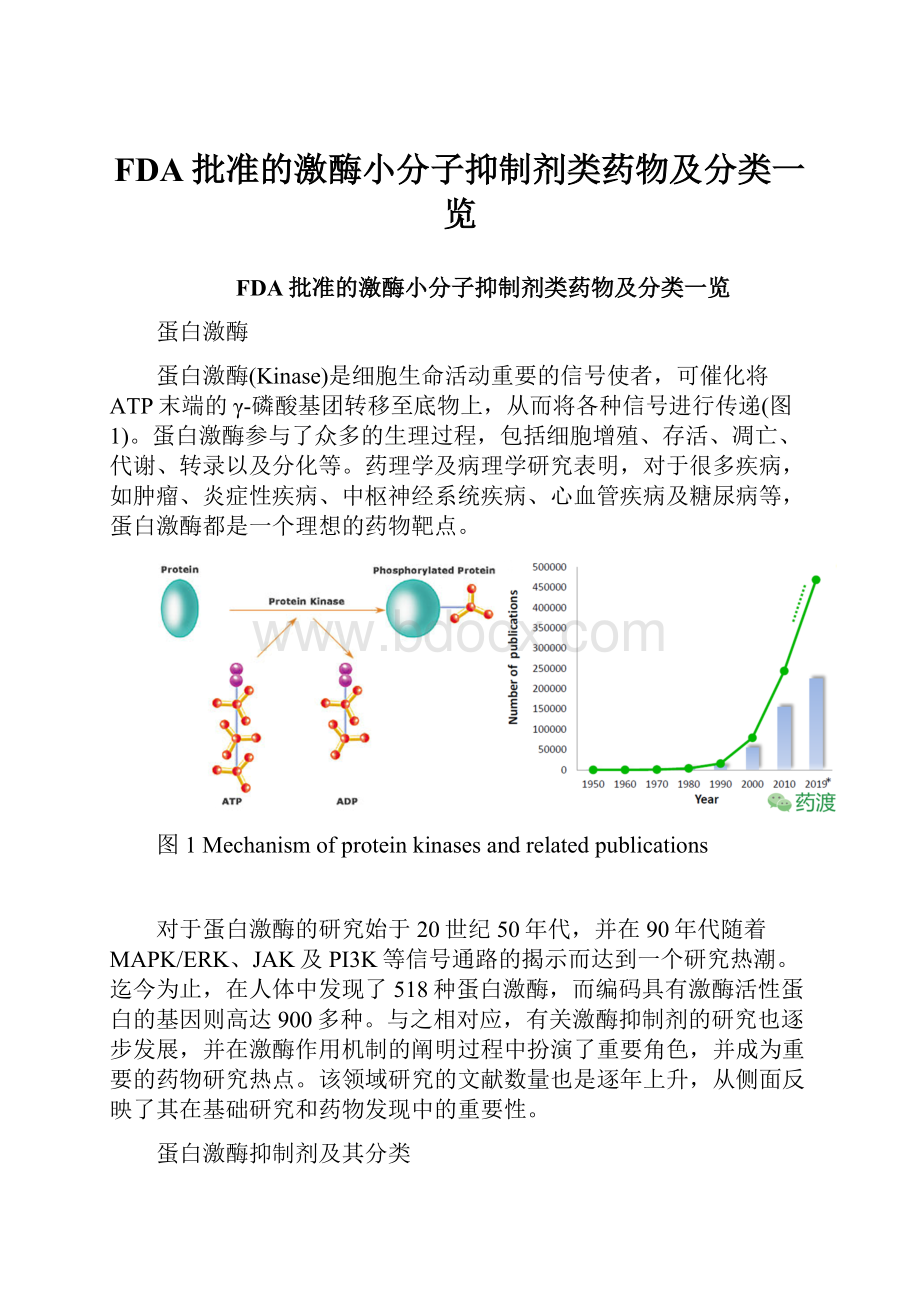
蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1Mechanismofproteinkinasesandrelatedpublications
对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类
过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。
蛋白激酶尽管在一级序列上有所差异,但在三维结构上却具有高度的保守性,特别是在催化活性结构域附近。
该区域存在一个β-折叠构成的N-lobe区域及α-螺旋构成的C-lobe区域,而ATP结合在两者构成的沟状区,也是很多激酶抑制剂的结合位点。
活性位点附近还存在一条Activation-Loop,通常末端存在一个保守的Asp-Phe-Gly(DFG)结构基序(图2A)。
图2Kinasestructureanddifferenttypesofreversiblesmall-moleculekinaseinhibitor
根据结合模式的不同,激酶抑制剂可分为不可逆及可逆两大类。
前者指化合物通过与Cys反应形成共价键结合在ATP结合位点上,从而封闭ATP的结合空间,该过程具有不可逆转性。
后者根据结合口袋区域及DFG基序构象的不同,可分为四种主要的不同亚型(图2B)。
类型Ⅰ为ATP竞争性抑制剂,结合与活性形式激酶DFG基序上的Asp残基。
类型Ⅱ抑制剂结合与非活性状态的激酶中,其上DFG基序上的Asp残基朝向分子外侧。
而类型Ⅲ的抑制剂结合在ATP附近别构位点上,但同ATP结合口袋没有相互作用。
类型Ⅳ抑制剂结合在远离ATP结合位点的别构作用区域。
还有些激酶抑制剂,如双底物类抑制剂,可以统一划分在类型Ⅴ里面,作用模式与上述四类有所不同。
图3SmallmolecularkinaseinhibitorsapprovedbyFDAin2001-2016
在获批的31中小分子激酶抑制剂类药物中(图3),绝大多数为酪氨酸激酶抑制剂,还有些属于丝氨酸/苏氨酸激酶抑制剂,只有2014年七月获批的Idelalisib属于脂激酶类抑制剂。
根据靶点蛋白及药物属性的不同,分类整理如下:
1. FDA批准的可逆NRTK(非受体型酪氨酸激酶)抑制剂类药物
图4ReversibleNITKinhibitors
2. FDA批准的可逆RTK(受体型酪氨酸激酶)抑制剂类药物
图5ReversibleRTKinhibitors-1
图6ReversibleRTKinhibitors-2
3. FDA批准的不可逆蛋白激酶抑制剂类药物
图7Inreversibleproteinkinaseinhibitor
4.FDA批准的丝氨酸/苏氨酸激酶抑制剂类药物
图8Serine/Threoninekinaseinhibitors
5.FDA批准的脂激酶抑制剂类药物
图9Lipidkinaseinhibitor
挑战与展望
在过去的15年里,基于蛋白激酶的药物发现取得了巨大进步。
相比于GPCR,膜通道与转运蛋白及蛋白酶等传统药物靶点领域,激酶抑制剂代表了一类年轻而又充满活力的药物发现空间,并取代GPCR成为癌症领域最火热的细胞治疗靶点。
尽管在短短十五年时期内已有31种药物获得批准,但在2016年,近五年的快速增长势头没能继续延续。
激酶小分子抑制剂类药物研究领域仍面临诸多挑战。
首先,人体内激酶家族中只有少数成员获得了详尽研究。
绝大多数抑制剂研究集中于酪氨酸激酶及类酪氨酸激酶家族,如CDK、MAPK、GSK3、CMGC、PKA、PKG及PKC等。
这一不平衡还体现在现有获批药物数量上,针对BCR-Abl、ErbBs及VEGFRs三类酪氨酸激酶开发的药物占到了总数的三分之二以上。
而在另一分类体系中,脂激酶只有一种抑制剂类药物上市,尽管这类酶的抑制剂早在20世纪90年代就早已有报道,且开展了很多临床及临床前研究。
以上现状表明,人体激酶组中的很多成员还处于被冷落状态。
我们需要开发出新型的研究方法或筛选探针,以便更好的揭示这些激酶的作用机制,并有效开发其作为药物靶点的潜力。
令人鼓舞的是,最近几年有数个激酶成员的抑制剂类药物首次获得批准,如2013年MEK抑制剂Trametinib、BTK的抑制剂Ibrutinib及2015年获批的CDK抑制剂Palbociclib。
其次,尽管激酶的梯级调控信号调节着众多的生理过程,如炎症反应、中枢神经系统异常、心血管疾病、糖尿病及癌症等,但现有获批药物超过90%以上集中在癌症治疗领域。
针对激酶的小分子抑制剂类药物应用领域亟待拓展。
目前,Tofacitinib已被批准用于关节炎治疗。
即便是在肿瘤治疗领域,也有很多问题有待进一步深入研究,如肿瘤的耐药性问题以及同其他药物的联合用药等。
第三,现有的很多激酶抑制剂药物存在较多相似性,大多是在已批准药物基础上设计优化而成,如针对ErbB的五种抑制剂均包含相同的核心结构模块。
从这个角度讲,现有药物的结构多样性不够丰富,亟需增加药物研发初始阶段高通量筛选(HTS)所用化合物库的结构多样性。
而天然产物库,通常包含不同于绝大多数化学合成抑制剂库的药效团及分子骨架,有望成为拓展HTS库结构多样性的新资源。
第四,具有新的作用机制及特异性的激酶抑制剂类药物有待开发。
由于激酶ATP结合口袋区域附近结构的保守型,绝大多数抑制剂为可逆性抑制剂。
这也导致了绝大多数小分子抑制剂存在不止一个作用靶点分子,导致脱靶现象以及副作用的产生。
与之相随,具有绝对选择性的抑制剂分子极为稀少。
未来工作中,我们需要探索具有新型作用机制的抑制剂分子。
而激酶抑制剂的选择性则是一个略带争议的特性。
早期研究中,具有交叉抑制活性或广谱选择性的抑制剂是肿瘤学研究的得力方法。
而当前,选择性抑制剂更适合于肿瘤治疗的理论逐步被广泛认同。
研究结论表明,激酶抑制剂类药物并不需要绝对的选择性,而是要有适当的选择性以便在药效与毒性间达到某个平衡点。
本文所引用资料:
1.SmallMoleculeKinaseInhibitorsasAnti-CancerTherapeutics.Mini-ReviewsinMedicinalChemistry,2012,12,399-411
2.Kinaseinhibitorsandmonoclonalantibodiesinoncology:
clinicalimplications.NatureReviewsClinicalOncology,2016,13,209–227
3.TyrosineKinaseInhibitors:
ViewsofSelectivity,SensitivityandClinicalPerformance.2013,53,161-185
4.Small-moleculekinaseinhibitors:
ananalysisofFDA-approveddrugs.DrugDiscovToday.2016Jan;21
(1):
5-10
5.FDA-approvedsmall-moleculekinaseinhibitors.TrendsinPharmacologicalSciences2015,36,422-439
6.http:
//www.fda.gov/Drugs/default.htm
7. http:
//www.accessdata.fda.gov/scripts/cder/daf/index.cfm
8.部分药物信息查询自药渡网-药物数据。