新人教版九年级化学上学期寒假作业含答案解析 机构辅导培优5.docx
《新人教版九年级化学上学期寒假作业含答案解析 机构辅导培优5.docx》由会员分享,可在线阅读,更多相关《新人教版九年级化学上学期寒假作业含答案解析 机构辅导培优5.docx(25页珍藏版)》请在冰豆网上搜索。
新人教版九年级化学上学期寒假作业含答案解析机构辅导培优5
新人教版九年级(上)化学寒假作业(5)
一、解答题(共5小题,满分6分)
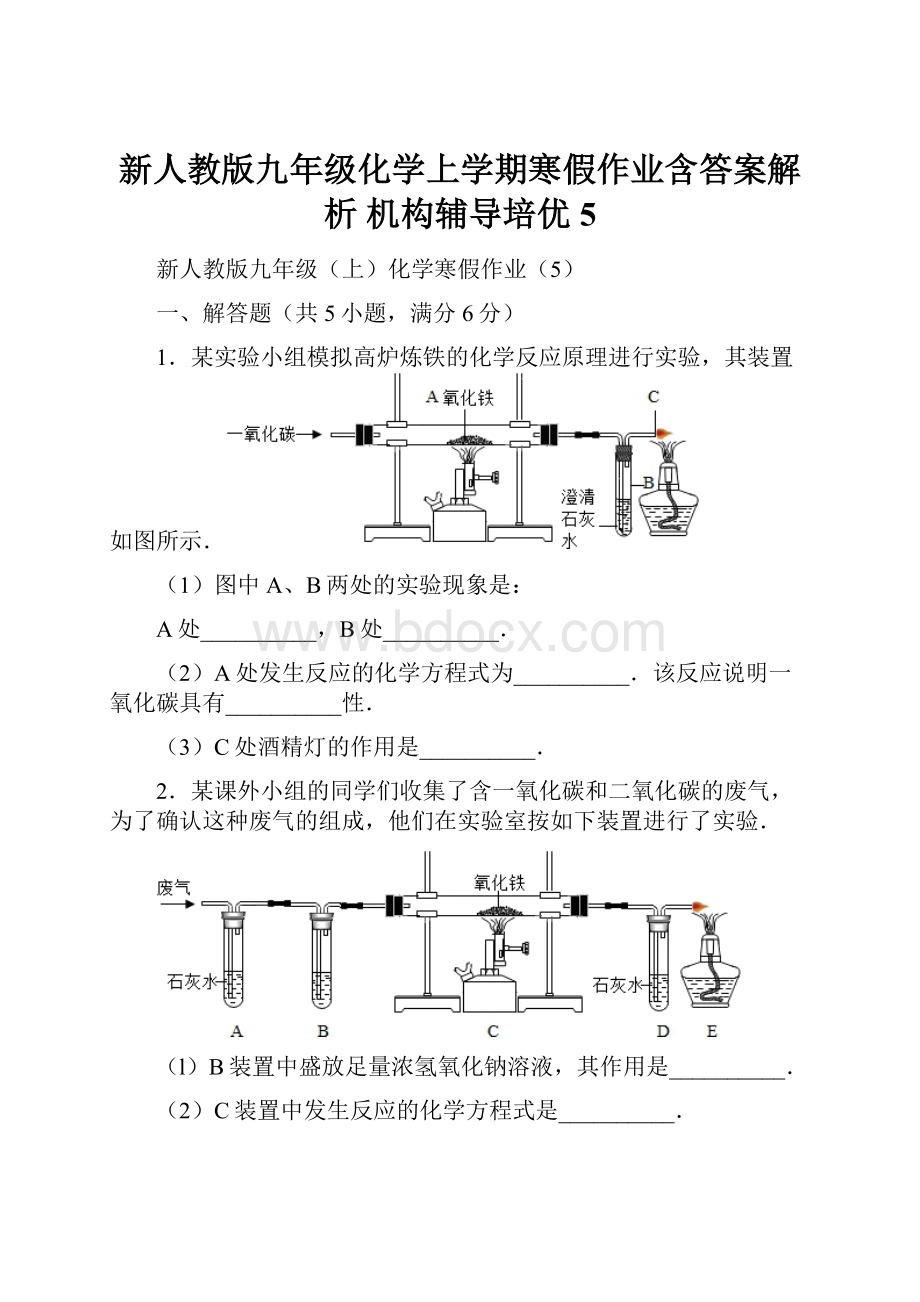
1.某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如图所示.
(1)图中A、B两处的实验现象是:
A处__________,B处__________.
(2)A处发生反应的化学方程式为__________.该反应说明一氧化碳具有__________性.
(3)C处酒精灯的作用是__________.
2.某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验.
(l)B装置中盛放足量浓氢氧化钠溶液,其作用是__________.
(2)C装置中发生反应的化学方程式是__________.
(3)A装置和D装置完全相同,其作用的不同之处是__________.
(4)该小组同学认为废气中的一氧化碳可以利用,于是设计如下装置除去废气中的二氧化碳,并收集一瓶一氧化碳,准备进行后续地探究.其中最合理的装置是__________(填序号,瓶内为氢氧化钠溶液).
3.氧气、氢气、二氧化碳、一氧化碳的检验:
检验方法
现象
氧气
氢气
二氧化碳
一氧化碳
4.正确连接如图所示的装置进行实验,可以验证某混合气体的成分是CO2和CO(每套装置限用一次).
请回答下列问题:
(1)连接装置导管口的顺序:
混合气体→__________→尾气处理(填导管接口代号).
(2)证明原混合气体中CO2存在的实验现象是__________;证明CO存在的有关反应的化学方程式是__________,__________.
5.某实验小组探究火锅烟气中CO2、CO分别对人体血液供氧能力的影响.设计装置如图所示(试管中均为稀释的新鲜鸡血):
实验记录:
操作步骤
现象
Ⅰ
分别向试管①、②、③中通入氧气
鸡血颜色为鲜红色
Ⅱ
向试管①中通入气体A;
停止通入A,向试管①中通入氧气
鸡血颜色由鲜红色变为桃红色
鸡血颜色不变
Ⅲ
向试管③中通入气体B;
停止通入B,向试管③中通入氧气
鸡血颜色由鲜红色变为暗红色
鸡血颜色由暗红色变为鲜红色
(1)向试管①中通入气体时,气体从导管口(填装置图中的序号)__________处通入.
(2)试管②的作用是__________.
(3)气体A为__________.判断的依据是__________.
(4)从安全和环保的角度来看,本实验需要改进的地方是__________.
(5)通过实验可以得出结论,火锅烟气中对人体血液供氧量有影响的是(填具体物质)__________.
二、选择题(共2小题,每小题3分,满分6分)
6.CO和CO2相比较,下列说法错误的是()
A.它们都是纯净物,又都是氧化物
B.组成元素种类相同,但碳元素的化合价不同
C.它们均能通过碳与氧气反应得到
D.常温常压下都是气体,都有毒,都能致人死亡
7.不能用于鉴别二氧化碳和氧气的是()
A.燃着的木条B.颜色、气味C.紫色石蕊溶液D.澄清石灰水
三、解答题(共6小题,满分0分)
8.下面是某学习小组对Cu、Fe、Mg、Ag、Al五种金属相关知识的学习与探究.请你参与并回答问题:
(1)下列制品中,主要利用金属导电性的是__________(填序号).
(2)铝的原子结构示意图为
,该原子在化学反应中易__________(填“得”或“失”)电子.
(3)铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,反应的化学方程式为:
Cu+2H2SO4(浓)
CuSO4+X↑+2H2O,则X的化学式为__________.
(4)所给五种金属分别放入到相同盐酸中,写出有气泡生成的反应化学方程式:
__________.
(5)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生.根据上述现象,能得出的结论是__________.
A.滤渣中一定有AgB.滤渣中可能有Cu和Fe
C.滤液中一定有Fe(NO3)2D.滤液中一定有AgNO3和Cu(NO3)2.
9.下列四个实验中,铁钉最易生锈的是()
A.
B.
C.
D.
10.小明同学设计了如图所示的A、B两个实验(已将铁丝和银丝表面打磨).
①A实验的主要现象是__________,该现象说明在金属活动顺序中,__________排在氢前面.
②B实验中,当烧杯内盛有__________溶液时,可验证Fe、Cu、Ag三种金属活动性强弱.
11.向铜粉和铁粉的混合物中加入一定量的盐酸,充分反应后过滤.以下判断不正确的是()
A.滤纸上可能没有铜B.滤纸上可能含有铁
C.滤液中可能含有盐酸D.滤液中一定含有氯化亚铁
12.做完“铁在氧气里燃烧”的实验后,小名同学有两个疑惑不解的问题,于是他进行了以下探究活动.
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液.
【实验探究】将冷却后的黑色物质碾碎,装入试管,加入__________溶液,观察到的现象是__________,说明铁燃烧时溅落下来的黑色物质中还含有铁.
Fe3O4
Fe2O3
铁
分解温度/℃
1538
1400
﹣
熔点/℃
﹣
﹣
1535
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4.
【理论探讨】
结合表中数据,可推知铁在氧气里燃烧时产生的高温应在__________之间,在此温度范围内__________已分解,所以铁在氧气里燃烧的产物是__________.
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须__________;
(2)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色__________,就说明包装盒破损进气,这样售货员就能及时发现并处理.
(3)下列铁的氧化物中,铁元素的质量分数由大到小的顺序是__________(填字母).
A.FeOB.Fe2O3C.Fe3O4.
13.某小组利用实验数据,求算金属M的相对原子质量.已知金属M和硫酸反应的化学方程式为:
M+H2SO4═MSO4+H2↑.
现取20g该金属样品于烧杯中,然后向其中加入稀硫酸,实验数据记录如下:
实验编号
1
2
3
4
5
加入硫酸的质量/g
100
200
300
400
500
烧杯中剩余物质量/g
119.8
219.6
319.4
419.4
519.4
第5次实验后,烧杯中还有0.5g剩余固体.计算该金属的相对原子质量.
新人教版九年级(上)化学寒假作业(5)
一、解答题(共5小题,满分6分)
1.某实验小组模拟高炉炼铁的化学反应原理进行实验,其装置如图所示.
(1)图中A、B两处的实验现象是:
A处红色粉末逐渐变黑,B处澄清石灰水变浑浊.
(2)A处发生反应的化学方程式为Fe2O3+3CO
2Fe+3CO2.该反应说明一氧化碳具有还原性.
(3)C处酒精灯的作用是点燃尾气,防止污染空气.
【考点】一氧化碳还原氧化铁;书写化学方程式、文字表达式、电离方程式.
【专题】化学学习中的实验思想;金属与金属材料.
【分析】
(1)根据一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
(2)一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,写出反应的化学方程式即可.
(3)根据一氧化碳有毒,能污染环境,进行分析解答.
【解答】解:
(1)一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,会观察到A处红色粉末逐渐变黑.
生成的二氧化碳能与澄清石灰水反应生成碳酸钙沉淀和水,故可以观察到B处澄清石灰水变浑浊.
(2)一氧化碳与氧化铁在高温下反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2;一氧化碳夺取了氧化铁中的氧,该反应说明一氧化碳具有还原性.
(3)一氧化碳有毒,直接排放会污染空气,C处酒精灯的作用是点燃尾气,防止污染空气.
故答案为:
(1)红色粉末逐渐变黑;澄清石灰水变浑浊;
(2)Fe2O3+3CO
2Fe+3CO2;还原;(3)点燃尾气,防止污染空气.
【点评】本题难度不大,掌握一氧化碳还原氧化铁的反应原理、注意事项等是正确解答本题的关键.
2.某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验.
(l)B装置中盛放足量浓氢氧化钠溶液,其作用是吸收二氧化碳气体.
(2)C装置中发生反应的化学方程式是Fe2O3+3CO
2Fe+3CO2.
(3)A装置和D装置完全相同,其作用的不同之处是A是检验废气中是否含有二氧化碳,D装置用来检验反应中是否有二氧化碳生成,进而推断出废气中是否含有一氧化碳.
(4)该小组同学认为废气中的一氧化碳可以利用,于是设计如下装置除去废气中的二氧化碳,并收集一瓶一氧化碳,准备进行后续地探究.其中最合理的装置是③(填序号,瓶内为氢氧化钠溶液).
【考点】二氧化碳的化学性质;二氧化碳的检验和验满;一氧化碳的化学性质;一氧化碳还原氧化铁;书写化学方程式、文字表达式、电离方程式.
【专题】物质的性质与用途.
【分析】一氧化碳是一种中性气体,不与酸或碱反应,而二氧化碳是一种酸性气体,能与碱反应.所以我们在除去一氧化碳中的二氧化碳气体时,可以选择碱性溶液.
【解答】解:
(1)为了确定废气的组成,我们利用澄清的石灰水来检验二氧化碳气体,然后再利用氢氧化钠溶液来吸收二氧化碳,然后再利用一氧化碳的还原性,来检验生成的气体是二氧化碳.
(2)一氧化碳具有还原性,所以能使红色固体逐渐变为黑色
(3)A装置用来检验原气体中含有二氧化碳,而D装置用来检验一氧化碳反应的产物二氧化碳.
(4)我们利用洗气瓶来除去二氧化碳并收集一氧化碳气体时,应长管进气.同时需要收集CO,所以还是储气瓶,所以液体还应该是从长管出,所以两个管都应该通到底部.
故答案为:
(1)充分吸收废气中的二氧化碳;
(2)Fe2O3+3CO
2Fe+3CO2
(3)A装置用来检验废气中是否含有二氧化碳;D装置用来检验反应中是否有二氧化碳生成,进而推断出废气中是否含有一氧化碳.
(4)③
【点评】我们在检验一氧化碳气体时,利用一氧化碳的还原性,然后检验是否有二氧化碳生成,所以我们在检验一氧化碳时,先将二氧化碳气体吸收干净.
3.氧气、氢气、二氧化碳、一氧化碳的检验:
检验方法
现象
氧气
氢气
二氧化碳
一氧化碳
【考点】常见气体的检验与除杂方法.
【专题】物质的检验、鉴别与推断.
【分析】根据氧气能使带火星的木条复燃,氢气具有可燃性,产生水雾,二氧化碳能使澄清的石灰水变浑浊,一氧化碳具有可燃性,产生使石灰水变浑浊的气体进行回答.
【解答】解:
氧气能使带火星的木条复燃,氢气具有可燃性,产生水雾,二氧化碳能使澄清的石灰水变浑浊,一氧化碳具有可燃性,产生使石灰水变浑浊的气体;
故答案为:
检验方法
现象
氧气
将带火星的木条伸入集气瓶内
木条复燃
氢气
将气体点燃,在火焰的上方罩一个冷而干燥的烧杯
气体燃烧,发出淡蓝色的火焰,烧杯内壁有水雾出现
二氧化碳
将气体通入适量的石灰水
石灰水变浑浊
一氧化碳
将气体点燃,并将产生的气体通入石灰水
气体燃烧,发出蓝色的火焰,产生的气体能使澄清的石灰水变浑浊
【点评】物质的检验是初中化学的难重点,也是中考的热点之一,了解物质的物理性质和化学性质,明确相似物质间的性质差别是解题的关键.
4.正确连接如图所示的装置进行实验,可以验证某混合气体的成分是CO2和CO(每套装置限用一次).
请回答下列问题:
(1)连接装置导管口的顺序:
混合气体→④③⑤⑥①②→尾气处理(填导管接口代号).
(2)证明原混合气体中CO2存在的实验现象是B中澄请石灰水变浑浊;证明CO存在的有关反应的化学方程式是Fe2O3+3CO
2Fe+3CO2,Ca(OH)2+CO2=CaCO3↓+H2O.
【考点】常见气体的检验与除杂方法;混合物的分离方法.
【专题】压轴实验题;实验装置连接题;常见气体的实验室制法、检验、干燥与净化.
【分析】装置A用于检验CO的存在,把混合气体中CO2完全处理后,气体通入A装置,若玻璃管内粉末由红色变黑色同时试管中的澄清石灰变浑浊,说明混合气体中含CO;
装置B用于检验混合气体中含CO2,混合气体通入装置B,澄清石灰水变浑浊,说明混合气体中含有CO2;
装置C用于处理混合气体中的CO2,检验过二氧化碳是否存在后的混合气体通入装置C,CO2全部被吸收.
【解答】解:
(1)混合气体选通入装置B检验CO2气体是否存在,气体应由④通入从③排出B装置;然后通入装置C,处理混合气体中的气体CO2,由⑤通入从⑥排出;接下来气体通入装置A,检验CO气体的存在,气体由①进入从②排出.
故答:
④③⑤⑥①②;
(2)B中澄请石灰水变浑浊,说明混合气体中有CO2存在;玻璃管内粉末由红变黑,说明氧化铁被还原成铁,试管内澄清石灰水变浑浊,说明生成二氧化碳气体;两处现象综合,说明混合气体中含有CO气体.
故答:
B中澄请石灰水变浑浊;Fe2O3+3CO
2Fe+3CO2;Ca(OH)2+CO2=CaCO3↓+H2O.
【点评】点燃可燃性气体时,由于可燃性气体与空气混合可能发生爆炸,所以点燃前要检验气体的纯度.如果设计更严谨的实验,可以将B在C后再次使用用来验证二氧化碳无残留.
5.某实验小组探究火锅烟气中CO2、CO分别对人体血液供氧能力的影响.设计装置如图所示(试管中均为稀释的新鲜鸡血):
实验记录:
操作步骤
现象
Ⅰ
分别向试管①、②、③中通入氧气
鸡血颜色为鲜红色
Ⅱ
向试管①中通入气体A;
停止通入A,向试管①中通入氧气
鸡血颜色由鲜红色变为桃红色
鸡血颜色不变
Ⅲ
向试管③中通入气体B;
停止通入B,向试管③中通入氧气
鸡血颜色由鲜红色变为暗红色
鸡血颜色由暗红色变为鲜红色
(1)向试管①中通入气体时,气体从导管口(填装置图中的序号)a处通入.
(2)试管②的作用是作对照实验.
(3)气体A为CO.判断的依据是通入A后鸡血颜色由鲜红色变为桃红色,再通入氧气,鸡血颜色不变的现象说明气体A使血红蛋白(血液)不能很好的与氧气结合,体现CO的毒性.
(4)从安全和环保的角度来看,本实验需要改进的地方是增加CO尾气处理装置.
(5)通过实验可以得出结论,火锅烟气中对人体血液供氧量有影响的是(填具体物质)CO2和CO.
【考点】一氧化碳的毒性;实验探究物质的性质或变化规律;化学实验方案设计与评价;常见气体的检验与除杂方法.
【专题】化学与生活健康;简单实验方案的设计与评价;科学探究.
【分析】根据CO和二氧化碳的化学性质解答.一氧化碳有剧毒,能与血红蛋白很好的结合,使氧失去与血红蛋白结合的机会.
【解答】解:
(1)向试管①中通入气体时,气体从导管口a处通入;
(2)试管②的作用是作对照实验;
(3)向试管①中通入气体A,停止通入A,向试管①中通入氧气,通入A后鸡血颜色由鲜红色变为桃红色,再通入氧气,鸡血颜色不变的现象说明气体A使血红蛋白(血液)不能很好的与氧气结合,体现CO的毒性.
(4)由于CO有毒,不能直接排放到空气中,所以要增加尾气处理装置.
(5)由实验Ⅲ可知该气体通入时鸡血颜色由鲜红色变为暗红色,再通入氧气鸡血颜色由暗红色变为鲜红色,说明CO2
对人体供氧也有影响,故答案为CO2和CO.
故答案为:
(1)a
(2)作对照实验(答出对比的意思就给分)
(3)CO
通入A后鸡血颜色由鲜红色变为桃红色,再通入氧气,鸡血颜色不变的现象说明气体A使血红蛋白(血液)不能很好的与氧气结合,体现CO的毒性(建议同时答出现象和结论;结论答气体A影响血液供氧能力给分)
(4)增加CO尾气处理装置(不答CO不给分;答剩余CO直接排放、未处理等给分)
(5)CO2和CO
【点评】本题是实验探究题,解答本题要充分理解一氧化碳和二氧化碳的性质方面的知识,根据实验现象能分析出原因,只有这样才能对相关方面的问题做出正确的判断.
二、选择题(共2小题,每小题3分,满分6分)
6.CO和CO2相比较,下列说法错误的是()
A.它们都是纯净物,又都是氧化物
B.组成元素种类相同,但碳元素的化合价不同
C.它们均能通过碳与氧气反应得到
D.常温常压下都是气体,都有毒,都能致人死亡
【考点】一氧化碳的物理性质;二氧化碳的物理性质;从组成上识别氧化物;纯净物和混合物的判别;碳的化学性质;有关元素化合价的计算.
【专题】结构决定性质;碳单质与含碳化合物的性质与用途.
【分析】A、根据CO和CO2组成和类别分析;
B、根据CO和CO2组成和碳元素的化合价分析;
C、根据碳与氧气反应的产物分析;
D、二氧化没有毒,但不能供给呼吸.
【解答】解:
A、CO和CO2都是有一种物质组成的属于纯净物;都含有两种元素,其中一种元素是氧元素,属于氧化物.故A说法正确;
B、CO和CO2都是由碳、氧元素组成的化合物,在CO中碳显+2价,在CO2中碳显+4价.故B说法正确;
C、碳与氧气在充分燃烧时生成了二氧化碳,在不充分燃烧时生成了一氧化碳.故C说法正确;
D、常温常压下都是气体,一氧化碳有毒,能致人死亡;二氧化碳没有毒,但不能供给呼吸,二氧化碳浓度高了也能使人窒息死亡.故D说法错误.
故选D.
【点评】本题主要考查物质的组成、种类和性质等方面的知识,解答时要理解虽然一氧化碳和二氧化碳的组成元素相同,但是性质不同.
7.不能用于鉴别二氧化碳和氧气的是()
A.燃着的木条B.颜色、气味C.紫色石蕊溶液D.澄清石灰水
【考点】二氧化碳的检验和验满;常见气体的检验与除杂方法;氧气的检验和验满.
【专题】结合课本知识的信息.
【分析】区分氧气和二氧化碳时利用氧气和二氧化碳的化学性质就可以了.如可利用氧气的助燃的性质.也可利用二氧化碳的灭火的性质.或利用二氧化碳能使澄清的石灰水变浑浊的性质.
【解答】解:
A、燃着的木条放入两集气瓶内时,木条燃烧更旺的是氧气,木条熄灭的是二氧化碳.可区分二者,故不可选;
B、二氧化碳和氧气都是无色无味的气体,所以用闻气味、看颜色的方法不能将两者区分开来.不可区分二者,故可选;
C、将紫色石蕊溶液分别倒入气体中,使紫色石蕊溶液变红色的是二氧化碳气体,不变化的是氧气.可区分二者,故不可选;
D、将澄清的石灰水分别倒入气体中,使澄清的石灰水变浑浊的气体是二氧化碳,不变化的是氧气.可区分二者,故不可选.
故选B.
【点评】在区分两种不同的物质时,选择的药品与这两种物质反应,出现两个不同的现象,利用这两个不同的现象,将这两种物质分开.
三、解答题(共6小题,满分0分)
8.下面是某学习小组对Cu、Fe、Mg、Ag、Al五种金属相关知识的学习与探究.请你参与并回答问题:
(1)下列制品中,主要利用金属导电性的是B(填序号).
(2)铝的原子结构示意图为
,该原子在化学反应中易失(填“得”或“失”)电子.
(3)铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,反应的化学方程式为:
Cu+2H2SO4(浓)
CuSO4+X↑+2H2O,则X的化学式为SO2.
(4)所给五种金属分别放入到相同盐酸中,写出有气泡生成的反应化学方程式:
Fe+2HCl═FeCl2+H2↑,Mg+2HCl═MgCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑.
(5)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生.根据上述现象,能得出的结论是AC.
A.滤渣中一定有AgB.滤渣中可能有Cu和Fe
C.滤液中一定有Fe(NO3)2D.滤液中一定有AgNO3和Cu(NO3)2.
【考点】金属的化学性质;金属的物理性质及用途;原子结构示意图与离子结构示意图;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
【专题】实验方法和过程的探究;金属与金属材料.
【分析】金属具有良好的导电性、导热性和延展性;
最外层电子数少于4个电子的原子在反应中一般容易失去电子;
反应前后元素种类不变,原子总个数不变;
铁和稀盐酸反应生成氯化亚铁和氢气,镁和稀盐酸反应生成氯化镁和氢气,铝和稀盐酸反应生成氯化铝和氢气;
铁比铜活泼,铜比银活泼.
【解答】解:
(1)下列制品中,主要利用金属导电性的是铜用作导线.
故填:
B.
(2)铝的原子结构示意图为
,该原子在化学反应中易失电子.
故填:
失.
(3)铜与浓硫酸在一定条件下可以反应,反应的化学方程式为:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O.
故填:
SO2.
(4)铁和稀盐酸反应生成氯化亚铁和氢气,镁和稀盐酸反应生成氯化镁和氢气,铝和稀盐酸反应生成氯化铝和氢气,反应的化学方程式为:
Fe+2HCl═FeCl2+H2↑,Mg+2HCl═MgCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑.
故填:
Fe+2HCl═FeCl2+H2↑,Mg+2HCl═MgCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑.
(5)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,说明铁没有剩余,
A.因为铁先和硝酸银反应生成硝酸亚铁和银,因此滤渣中一定有Ag,该选项说法正确;
B.因为铁没有剩余,因此滤渣中不含有铁,该选项说法不正确;
C.因为铁先和硝酸银反应生成硝酸亚铁和银,因此滤液中一定有硝酸亚铁,该选项说法正确;
D.当铁恰好和硝酸银、硝酸铜完全反应时,滤液中不含有AgNO3和Cu(NO3)2,该选项说法不正确.
故填:
AC.
【点评】要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
9.下列四个实验中,铁钉最易生锈的是()
A.
B.
C.
D.
【考点】金属锈蚀的条件及其防护.
【专题】金属与金属材料.
【分析】根据铁生锈的条件进行分析,铁在有水和氧气并存时易生锈.
【解答】解:
A、此试管中铁钉与水和氧气同时接触,易生锈,故A正确;
B、此试管中铁只与水接触,不易生锈,故B错误;
C、此试管中铁只与氧气接触,不易生锈,故C错误;
D、此试管中铁与水和氧气都不接触,不易生锈,故D错误.
故选A.
【点评】本题考查了铁生锈的条件,完成此题,可以依据已有的知识进行.
10.小明同学设计了如图所示的A、B两个实验(已将铁丝和银丝表面打磨).
①A实验的主要现象是铁丝表面产生气泡,该现象说明在金属活动顺序中,铁排在氢前面.
②B实验中,当烧杯内盛有硫酸铜溶液时,可验证Fe、Cu、Ag三种金属活动性强弱.
【考点】金属的化学性质.
【专题】结论探究;金属与金属材料.
【分析】铁能和