高考专题复习工艺流程.docx
《高考专题复习工艺流程.docx》由会员分享,可在线阅读,更多相关《高考专题复习工艺流程.docx(22页珍藏版)》请在冰豆网上搜索。
高考专题复习工艺流程
【例1】【2015·天津】(18分)废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。
湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。
某化学小组模拟该
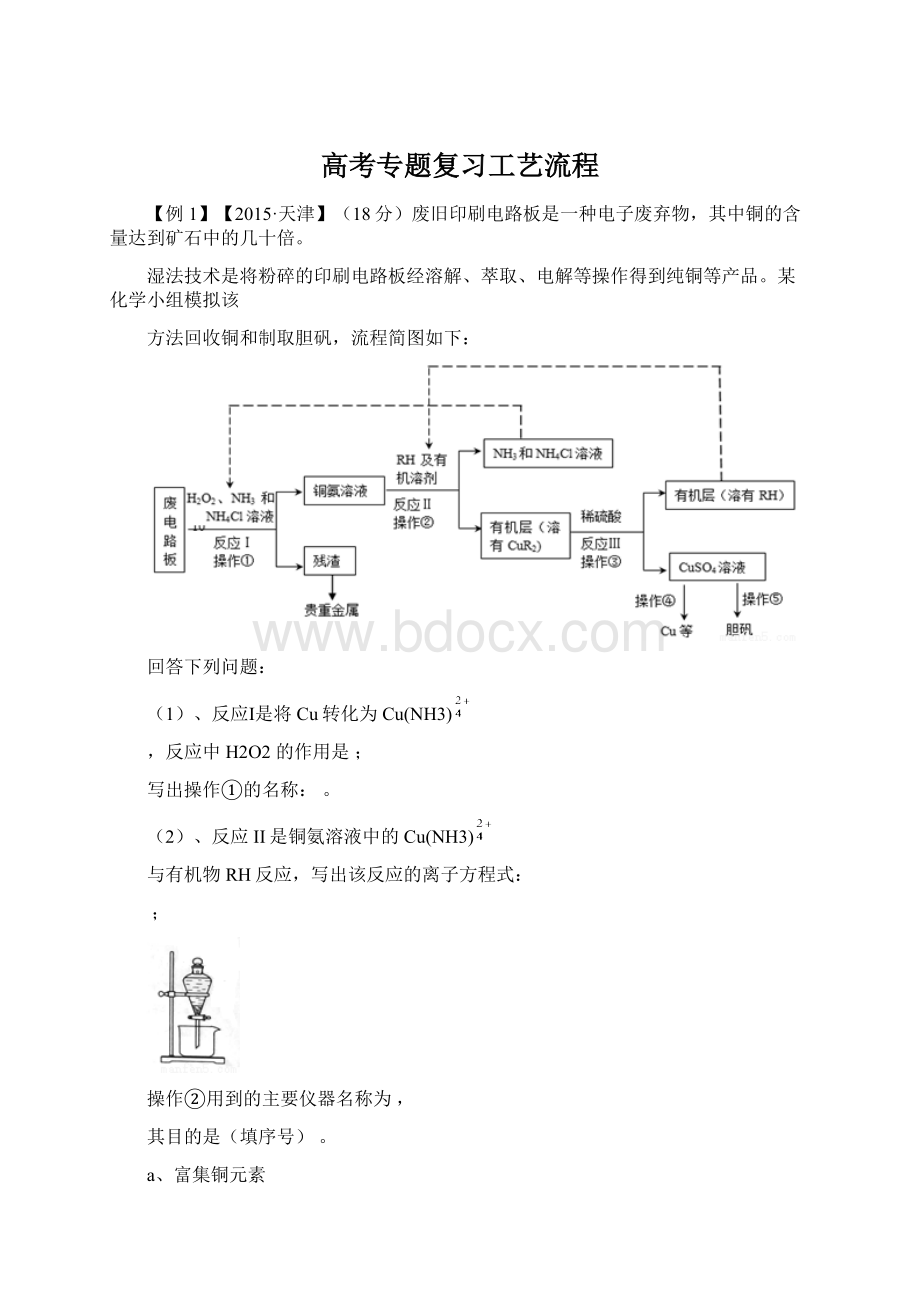
方法回收铜和制取胆矾,流程简图如下:
回答下列问题:
(1)、反应Ⅰ是将Cu转化为Cu(NH3)
,反应中H2O2的作用是;
写出操作①的名称:
。
(2)、反应II是铜氨溶液中的Cu(NH3)
与有机物RH反应,写出该反应的离子方程式:
;
操作②用到的主要仪器名称为,
其目的是(填序号)。
a、富集铜元素
b、使铜元素与水溶液中的物质分离
c、增加Cu
在水中的溶解度
(3)、反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和;
若操作③使用上图装置,图中存在的错误是。
(4)、操作④以石墨作电极电解CuSO4溶液。
阴极析出铜,阳极产物是;
操作⑤由硫酸铜溶液制胆矾的主要步骤是。
(5)、流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是;
循环使用的NH4Cl在反应Ⅰ中的主要作用是。
【例1】【2016·北京】(12分)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和
H2SO4为原料,制备高纯PbO,实现铅的再生利用。
其工作流程如下:
(1)、过程Ⅰ中,在Fe
催化下,Pb和PbO2反应生成PbSO4的化学方程式是;
(2)、过程Ⅰ中,Fe
催化过程可表示为:
ⅰ:
2Fe
+PbO2+4H
+SO
===2Fe
+PbSO4+2H2O;
ⅱ:
……
①、写出ⅱ的离子方程式:
;
②、下列实验方案可证实上述催化过程。
将实验方案补充完整。
a、向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b、;
(3)、PbO溶解在NaOH溶液中,存在平衡:
PbO(s)+NaOH(aq)
NaHPbO2(aq)。
其溶解度曲线如图所示:
①、过程Ⅱ的目的是脱硫。
滤液1经处理后可在过程Ⅱ中重复使用,其目的是(填序号)。
A、减少PbO的损失,提高产品的产率
B、重复利用NaOH,提高原料的利用率
C、增加Na2SO4浓度,提高脱硫效率
②、过滤Ⅲ的目的是提纯,综合上述溶解度曲线,简述过程Ⅲ的操作。
1、【2016·江苏】(12分)以电石渣(主要成分为Ca(OH)2和CaCO3)为原料制备KClO3的流程如下:
(1)、氯化过程控制电石渣过量,在75℃左右进行。
氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2
的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①、生成Ca(ClO)2的化学方程式为;
②、提高Cl2转化为Ca(ClO3)2的转化率的可行措施有(填序号)。
A、适当减缓通入Cl2速率B、充分搅拌浆料C、加水使Ca(OH)2完全溶解
(2)、氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为:
6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。
①、滤渣的主要成分为(填化学式);
②、滤液中Ca(ClO3)2与CaCl2的物质的量之比:
(填“>”、“<”或“=”)。
(3)、向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为
100g/L。
从该溶液中尽可能多地析出KClO3固体的方法是:
。
2、【2016·四川】(16分)资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。
磷尾矿
主要含Ca5(PO4)3F和CaCO3·MgCO3。
某研究小组提出了磷尾矿综合利用的研究方案,制备具有重
要工业用途的CaCO3、Mg(OH)2、P4和H2,其简化流程如下:
已知:
①、Ca5(PO4)3F在950℃不分解;
②、4Ca5(PO4)3F+18SiO2+30C
2CaF2+30CO+18CaSiO3+3P4。
请回答下列问题:
(1)、950℃煅烧磷尾矿生成气体的主要成分是;
(2)、实验室过滤所需的玻璃仪器是;
(3)、NH4NO3溶液能从磷矿I中浸取出Ca
的原因是。
(4)、在浸取液II中通入NH3,发生反应的化学方程式是。
(5)、工业上常用磷精矿【Ca5(PO4)3F】和硫酸反应制备磷酸。
已知25℃,101kPa时:
CaO(s)+H2SO4(l)===CaSO4(s)+H2O(l);
H=-271kJ/mol;
5CaO(s)+H3PO4(l)+HF(g)===Ca5(PO4)3F(s)+5H2O(l);
H=-937kJ/mol。
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是。
(6)、在一定条件下CO(g)+H2O(g)
CO2(g)+H2(g),当CO与H2O(g)的起始物质的
量之比为1︰5,达平衡时,CO转化了
。
若akg含Ca5(PO4)3F(相对分子质量为504)的质量
分数为10%的磷尾矿,在上述过程中有b%的Ca5(PO4)3F转化为P4,将产生的CO与H2O(g)
按起始物质的量之比1︰3混合,则相同条件下达平衡时能产生H2kg。
3、【2015·四川】(16分)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸
的硫铁矿烧渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。
活化硫铁矿还原Fe
的主要反应为:
FeS2+7Fe2(SO4)3+8H2O===15FeSO4+8H2SO4。
不考虑其他反应。
请回答下列问题:
(1)、第Ⅰ步H2SO4与Fe2O3反应的离子方程式是;
(2)、检验第Ⅱ步中Fe
是否完全还原,应选择(填字母编号)。
A、KMnO4溶液B、K3[Fe(CN)6]溶液C、KSCN溶液
(3)、第Ⅲ步加FeCO3调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH降到5.2,此时Fe
不沉淀,滤液中铝、硅杂质除尽。
通入空气引起溶液pH降低的原因是。
(4)、FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25℃,101kPa时:
4Fe(s)+3O2(g)===2Fe2O3(s);
H=-1648kJ/mol
C(s)+O2(g)===CO2(g);
H=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)===2FeCO3(s);
H=-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式为。
(5)、FeSO4在一定条件下可制得FeS2(二硫化亚铁)纳米材料。
该材料可用于制造高容量锂电池,
电池放电时的总反应为:
4Li+FeS2===Fe+2Li2S,正极反应式为。
(6)、假如烧渣中的铁全部视为Fe2O3,其含量为50%。
将akg质量分数为b%的硫酸加入到ckg烧
渣中浸取,铁的浸取率为96%,其他杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的
硫酸忽略不计。
按上述流程,第Ⅲ步应加入FeCO3kg。
4、【2015·山东】(19分)毒重石的主要成分BaCO3(含Ca
、Mg
、Fe
等杂质),实验室利用毒重
石制备BaCl2·2H2O的流程如下:
(1)、毒重石用盐酸浸取前需充分研磨,目的是;
实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的;
a、烧杯b、容量瓶c、玻璃棒d、滴定管
(2)、已知:
Ksp(BaC2O4)=1.6×10
;Ksp(CaC2O4)=2.3×10
。
Ca
Mg
Fe
开始沉淀时的pH
11.9
9.1
1.9
完全沉淀时的pH
13.9
11.1
3.2
加入NH3·H2O调节pH=8可除去(填离子符号),滤渣Ⅱ中含
(填化学式)。
加入H2C2O4时应避免过量,原因是。
(3)、利用简洁酸碱滴定法可测定Ba
的含量,实验分两步进行。
已知:
2CrO
+2H
===Cr2O
+H2O;Ba
+CrO
===BaCrO4↓。
步骤Ⅰ:
移取xmL一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用bmol/L盐酸标
准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:
移取ymLBaCl2溶液于锥形瓶中,加入xmL与步骤Ⅰ相同浓度的Na2CrO4溶液,待
Ba
完全沉淀后,再加入酸碱指示剂,用bmol/L盐酸标准液滴定至终点,测得滴加
盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的(填“上方”
或“下方”)。
BaCl2溶液的浓度为mol/L,若步骤Ⅱ中滴加盐酸时有少量
待测液溅出,Ba
浓度测量值将(填“偏大”或“偏小”)。
5、【2015·福建】(15分)无水AlCl3在生产、生活中应用广泛。
(1)、AlCl3在水中形成具有净水作用的Al(OH)3胶体,其反应的离子方程式为;
(2)、工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水AlCl3的一种工艺流
程示意如下:
已知:
物质
SiCl4
AlCl3
FeCl3
FeCl2
沸点/℃
57.6
180(升华)
300(升华)
1023
①、步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是(只要求写出一种);
②、步骤Ⅱ中若不通入Cl2和O2,则反应生成相对原子质量比硅大的单质是;
③、已知:
Al2O3(s)+3C(s)===2Al(s)+3CO(g);
H1=+1344.1kJ/mol;
2AlCl3(g)===2Al(s)+3Cl2(g);
H2=+1169.2kJ/mol。
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为;
④、步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式
分别为;
⑤、结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是。
6、【2015·安徽】(14分)硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼
酸钠NaBO2为主要原料制备NaBH4,其流程如下:
已知:
NaBH4常温下能与水反应,可溶于异丙酸(沸点:
13℃)。
(1)、在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是
,原料中的金属钠通常保存在中,实验室取用少
量金属钠需要用到的实验用品有,,玻璃片和小刀等。
(2)、请配平第①步反应的化学方程式:
()NaBO2+()SiO2+()Na+()H2——()NaBH4+()Na2SiO3
(3)、第②步分离采用的方法是;
第③步分离(NaBH4)并回收溶剂,采用的方法是。
(4)、NaBH4(s)与水(l)反应生成NaBO2(s)和H2(g),在25℃,101KPa下,已知每消耗3.8g
NaBH4(s)放热21.6kJ,该反应的热化学方程式是。
7、【2014·天津·T10】(14分)合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)
2NH3(g);
H=-92.4kJ/mol。
一种工业合成氨的简易流程图如下:
(1)、天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。
一定条件下向NH4HS溶液中通入空
气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:
。
(2)、步骤II中制H2原理如下:
①、CH4(g)+H2O(g)
CO(g)+3H2(g);
H1=+206.4kJ/mol
②、CO(g)+H2O(g)
CO2(g)+H2(g);
H2=-41.2kJ/mol
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是;
a、升高温度b、增大水蒸气浓度c、加入催化剂d、降低压强
利用反应②将CO进一步转化,可提高H2产量。
若1molCO和H2的混合气体(CO体积分数为
20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为。
(3)、图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。
根据图中a点
数据计算N2的平衡体积分数:
。
(4)、依据温度对合成氨反应的影响,在图2坐标系中,画出一定条件下的密闭容器内,从通入原料气
开始,随温度不断升高,NH3物质的量变化的曲线示意图。
【图1】【图2】
(5)、上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号),
简述本流程中提高合成氨原料总转化率的方法:
。
8、【2014·江苏·T16】(12分)烟气脱硫能有效减少SO2的排放。
实验室用粉煤灰(主要含有Al2O3、
SiO2等)制备碱式硫酸铝【Al2(SO4)x(OH)6﹣2x】溶液,并用于烟气脱硫研究。
(1)、酸浸时反应的化学方程式为;
滤渣Ⅰ的主要成分为(填化学式)。
(2)、加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为
Al2(SO4)x(OH)6﹣2x。
滤渣Ⅱ的主要成分为(填化学式);若溶液的pH偏高,
将会导致溶液中铝元素的含量降低,其原因是(用离子方程式表示)。
(3)、上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是
;与吸收SO2前的溶液相比,热分解后循环利用的
溶液的pH将(填“增大”、“减小”或“不变”)。
1、【2016·湖南六校联考】(14分)一种工业制备SrCl2·6H2O的生产流程如下:
已知:
①、M(SrCl2·6H2O)=267g/mol;
②、Ksp(SrSO4)=3.3×10
;Ksp(BaSO4)=1.1×10
;
③、经盐酸浸取后,溶液中除含有Sr
和Cl
外,还含有少量Ba
杂质。
(1)、隔绝空气高温焙烧,若2molSrSO4中只有S被还原,转移了16mol电子。
写出该反应的化学方程式:
;
(2)、过滤2后还需进行的两步操作是、;
(3)、加入硫酸的目的是;为了提高原料的利用率,滤液
中Sr
的浓度应不高于mol/L(注:
此时滤液中Ba
浓度为1×10
mol/L)。
(4)、产品纯度检测:
称取1.000g产品溶解于适量水中,向其中加入含AgNO31.100×10
mol的
AgNO3溶液(溶液中除Cl
外,不含其它与Ag
反应的离子),待Cl
完全沉淀后,用含Fe
的溶液作指示剂,用0.2000mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag
以
AgSCN白色沉淀的形式析出。
①、滴定反应达到终点的现象是;
②、若滴定过程用去上述浓度的NH4SCN溶液20.00mL,则产品中SrCl2·6H2O的质量百分含
量为(保留4位有效数字)。
2、【2016·河南八市重点4月模拟】(15分)硫酸亚铁铵【(NH4)2Fe(SO4)2】是一种重要的工业原料,
能溶于水,不溶于乙醇,其工业制法如下。
请回答:
(1)、步骤①中碱液洗涤的目的是:
;
若将碱液换为酸液,可能产生的问题是:
。
(2)、步骤②中B可以是(填字母),加入少量B的目的是。
a、CuCl2b、CuOc、Cu(NO3)2d、CuSO4
(3)、步骤⑥中要用到少量乙醇洗涤,其目的是。
(4)、用硫酸亚铁按晶体配制溶液时,需加入一定量硫酸,目的是。
工业上常用酸性KMnO4溶液通过滴定的方法测定硫酸亚铁铵样品的纯度,反应的离子方程式
为。
准确量取硫酸亚铁铵溶液时,
硫酸亚铁铵溶液应盛放于(填“酸式”或“碱式”)滴定管中。
(5)、硫酸亚铁铵晶体的样品中可能含有的杂质离子是,实验室的检验
方法是。
3、【2016·唐山二模】(14分)利用酸性含锰废水(主要含Mn
、Cl
、H
、Fe
、Cu
)可制备高
性能磁性材料(MnCO3)及纯净的氯化铜晶体(CuCl2·2H2O)。
工业流程如下:
已知:
几种金属离子沉淀的pH如表下:
金属离子
Fe
Fe
Cu
Mn
开始沉淀的pH
7.5
3.2
5.2
8.8
完全沉淀的pH
9.7
3.7
6.4
10.4
回答下列问题:
(1)、过程①中,MnO2在酸性条件下可将Fe
氧化为Fe
,反应的离子方程式为:
。
(2)、过程②中,所得滤渣W的成分是。
(3)、过程③中,调pH=6.4目的是。
(4)、过程④中,若生成的气体J可使澄清的石灰水变浑浊,则生成MnCO3反应的离子方程式是:
。
(5)、将滤渣Q溶解在过量的盐酸中,经过,过滤、洗涤、低温烘干,即可获得纯净的
氯化铜晶体(CuCl2·2H2O)。
(6)、过程④中,298K、c(Mn
)为1.05mol/L时,实验测得
MnCO3的产率与溶液pH、反应时间关系如图所示:
据图中信息,你选择的最佳pH是;
理由是。
(7)、从滤液C可得到的副产品是(填化学式)。
4、【2015·陕西西安交大附中高三(上)期中】(11分)铬是一种银白色的坚硬金属,铬的工业用途很
广,主要有金属加工、电镀、制革行业,这些行业排放的废水和废气是环境中的主要污染源。
请回答下列问题:
(1)、工业上冶炼铬的主要步骤如上图所示。
①、已知步骤II的反应方程式为:
8Na2CrO4+6Na2S+23H2O===8Cr(OH)3↓+3Na2S2O3+
22NaOH。
该反应中氧化剂是(填物质的化学式),生成lmolCr(OH)3时转
移电子的物质的量为mol;
②、步骤IV冶炼制铬的化学方程式为:
。
(2)、某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示
意如图所示:
,A为电源的(填“正极”或“负极”),阳极区溶
液中发生的氧化还原反应为:
。
(3)、化学需氧量(COD)可量度水体受有机物污染的程度。
它是在强酸并加热条件下,用K2Cr2O7作
强氧化剂处理水样时所消耗的K2Cr2O7的量,换算成相当于O2的含量(以mg/L计)。
某研究性
学习小组测定某水样的化学需氧量,过程如下:
ⅰ、取VamL水样于锥形瓶,加入l0.00mL0.2500mol/LK2Cr2O7溶液;
ⅱ、加碎瓷片少许,然后慢慢加入少量硫酸,混合均匀,加热;
ⅲ、反应完毕后,冷却,加指示剂,用cmol/L的(NH4)2Fe(SO4)2溶液滴定。
终点时消耗硫酸亚
铁铵溶液VbmL(此步操作的目的是用Fe
把多余的Cr2O
反应成Cr
)。
①、ⅰ中,量取K2Cr2O7溶液的仪器是;
②、ⅱ中,碎瓷片的作用是;
③、该水样的化学需氧量(COD)=(用含c、Va、Vb的表达式表示)。
5、【2014·浙江金丽衢十二校高三第一次联考】(15分)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝
于一体的新型多功能水处理剂。
高铁酸钾为暗红色粉末状晶体,干燥的晶体80℃以下十分稳定,它极
易溶于水,难溶于异丙醇。
实验室模拟生产工艺流程如下:
已知:
①、2KOH+Cl2===KCl+KClO+H2O(条件:
较低温度)
②、6KOH+3Cl2===5KCl+KClO3+3H2O(条件:
较高温度)
③、K2FeO4 在水溶液中易水解:
4FeO
+10H2O
4Fe(OH)3(胶体)+8OH
+3O2↑
实验室可利用右图装置完成流程①和②。
回答下列问题:
(1)、仪器a的名称是,恒压滴液漏斗支管的作用是,
两水槽中的水为(填“热水”或“冷水”)。
(2)、反应一段时间后,停止通氯气,再往仪器a中加入浓KOH溶液的目的是;
判断浓KOH溶液已过量的实验依据是。
(3)、从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生反应的离子方程
式为:
。
(4)、用重结晶法提纯粗产品:
将粗产品先用KOH稀溶液溶解,再加入饱和KOH溶液,冷却结晶,
过滤,用少量异丙醇洗涤,最后低温真空干燥。
①、粗产品用KOH溶解的目的是。
②、如何判断K2FeO4晶体已经洗涤干净。
(5)、从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如右图所示。
电解过程中阳极
的电极反应式为:
。
6、【江苏省南通中学2014~2015年度第一学期期中考试】(13分)钡盐行业生产中排出大量的钡泥,主要
含有BaCO3、BaSiO3、BaSO3、Ba(FeO2)2等。
某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡
泥制取Ba(NO3)2,其部分工艺流程如下(已知溶液中Fe
沉淀完全的pH=3.7):
(1)、酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为:
;
(2)、酸溶时通常控制反应温度不超过70℃,且不使用浓硝酸,原因是:
;
(3)、该厂结合本厂实际,选用的X为(填化学式);中和Ⅰ使溶液中
(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)。
7、【2015·福建莆田一中、漳州一中、泉州五中高三三校联考】(13分)工业上用重晶石(BaSO4)制备
其他钡盐的常用方法主要有高温煅烧还原法、沉淀转化法等。
Ⅰ、高温煅烧还原法——工业上利用重晶石高温煅烧还原法制备BaCl2的工艺流程图如下:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。
查表得:
BaSO4(s)+4C(s)
4CO(g)+BaS(s);
H1=+571.2kJ/mol①
BaSO4(s)+2C(s)
2CO2(g)+BaS(s);
H2=+226.2kJ/mol②
(1)、气体用过量NaOH溶液吸收,得到硫化钠。
Na2S水解的离子方程式为:
。
(2)、反应C(s)+CO2(g)
2CO(g)的
H=kJ/mol。
(3)、实际生产中必须加入过量的炭,同时还要通入空气,其目的可能是。
Ⅱ、沉淀转化法
(4)、已知Ksp(BaSO4)=1.0×10
,Ksp(BaCO3)=2.5×1