药品储存条件.docx
《药品储存条件.docx》由会员分享,可在线阅读,更多相关《药品储存条件.docx(17页珍藏版)》请在冰豆网上搜索。
药品储存条件
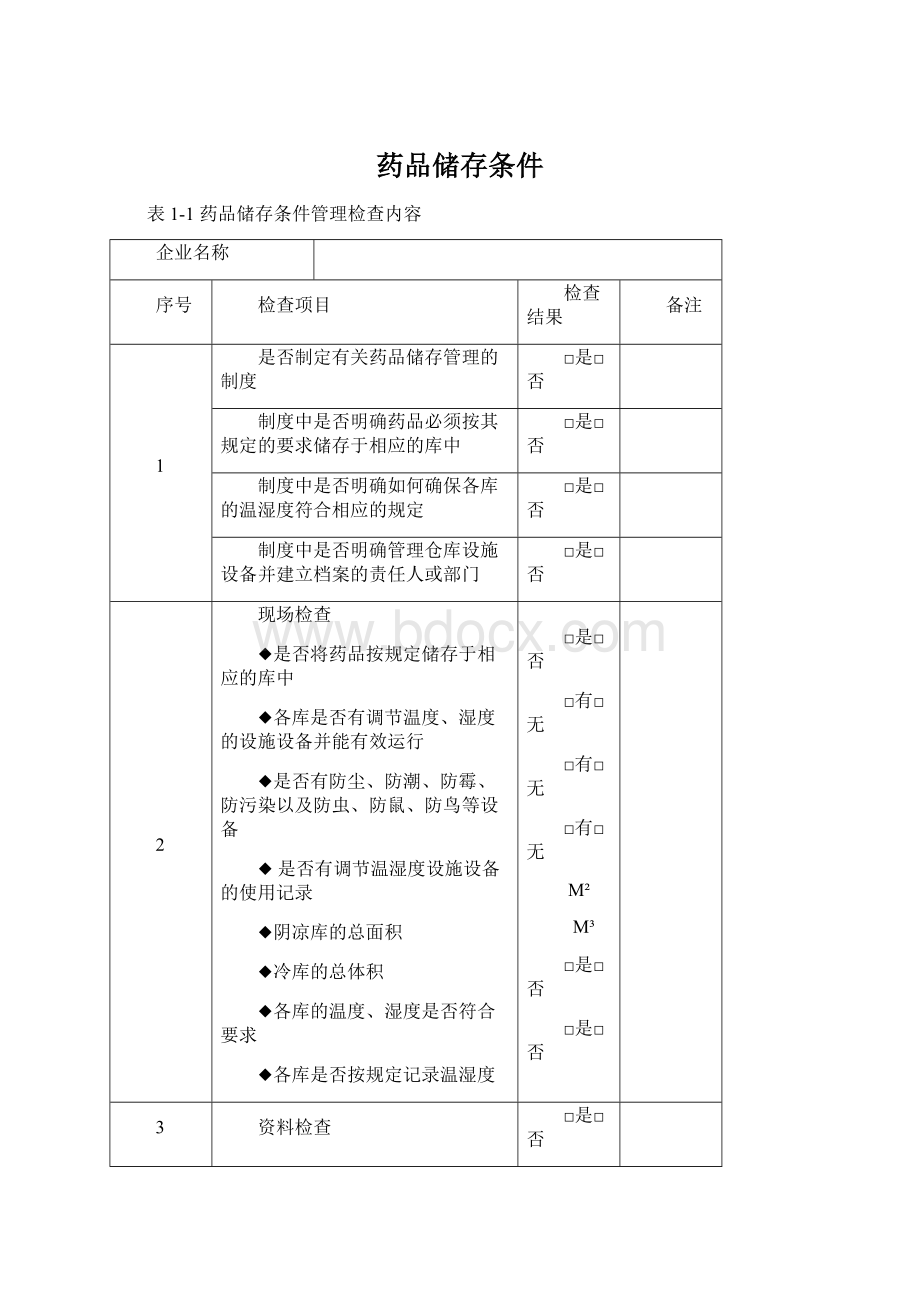
表1-1药品储存条件管理检查内容
企业名称
序号
检查项目
检查结果
备注
1
是否制定有关药品储存管理的制度
□是□否
制度中是否明确药品必须按其规定的要求储存于相应的库中
□是□否
制度中是否明确如何确保各库的温湿度符合相应的规定
□是□否
制度中是否明确管理仓库设施设备并建立档案的责任人或部门
□是□否
2
现场检查
◆是否将药品按规定储存于相应的库中
◆各库是否有调节温度、湿度的设施设备并能有效运行
◆是否有防尘、防潮、防霉、防污染以及防虫、防鼠、防鸟等设备
◆是否有调节温湿度设施设备的使用记录
◆阴凉库的总面积
◆冷库的总体积
◆各库的温度、湿度是否符合要求
◆各库是否按规定记录温湿度
□是□否
□有□无
□有□无
□有□无
M²
M³
□是□否
□是□否
3
资料检查
◆认证后是否建立各库的温湿度记录档案
◆随机抽查上年7~8月的温湿度记录,如温度或湿度超出规定,是否采取有效措施并有记录
◆是否对仓库所用的调节温度湿度的设施设备及其它设备定期进行检查、维修、保养并建立档案
□是□否
□是□否
□是□否
4
其它需要说明的问题:
年月日
表1-2药品储存条件管理检查内容
企业名称
阴凉库名称
面积
制冷设备名称
型号/功率
台数
生产企业
温湿度是否
符合要求
冷库名称
体积
制冷设备名称
型号/功率
台数
生产企业
温湿度是否符合要求
需要说明的其它问题:
年月日
表2药品质量档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关药品质量档案管理的内容
□是□否
制度中是否明确质量管理机构应负责建立企业所经营药品的质量档案
□是□否
制度中是否明确药品质量档案应包括的具体内容及要求
□是□否
2
是否建立药品质量档案的目录
建立药品质量档案的药品总数
其中:
首营品种建档数
主营品种建档数
发生过质量问题药品的建档数
质量不稳定药品的建档数
其它药品建档数
□是□否
个
个
个
个
个
个
3
药品质量档案表填写情况:
◆品名规格
◆生产企业
◆建档时间
◆药品质量标准及变更情况
◆药品合法性证明文件(生产批件及其变更情况)
◆药品包装、说明书的批件及其变更情况
◆药品动态质量状况记录,内容应包括:
药品进货批次
药品验收质量状况
药品养护质量状况
药品销货退回批次
药品销货退回质量状况
◆出现不合格情况药品的确认及处理凭证是否齐全
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□是□否
4
是否根据药品动态质量状况记录对药品质量情况进行阶段性的分析汇总
□是□否
5
◆列出所抽查药品质量档案表的品种名称(不得少于5个):
◆检查组认为企业在药品质量档案管理方面存在的主要问题:
◆请将现场检查中所看到的质量档案表样式复印一份随资料带回
检查组成员签名
年月日
表3药品养护档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关药品养护档案管理的内容
□是□否
制度中是否明确质量管理机构应定期确定并下发重点养护品种名单
□是□否
制度中是否明确重点养护品种应建立药品养护档案
□是□否
制度中是否明确质量管理机构应负责指导养护员建立有关药品的养护档案
□是□否
2
质量管理机构下发的重点养护品种名单的内容应包括:
◆品名规格
◆生产企业
◆确定时间
◆确定理由
◆养护重点
□有□无
□有□无
□有□无
□有□无
□有□无
3
是否建立药品养护档案的目录
建立药品养护档案的药品总数
其中:
首营品种建档数
发生过质量问题药品的建档数
质量不稳定药品的建档数
其它药品建档数
□是□否
个
个
个
个
个
4
药品养护档案表填写情况:
◆品名规格
◆批准文号
◆生产企业
◆建档时间
◆药品质量标准及变更情况
◆药品性状
◆药品检查项目
◆储存要求
◆包装情况
◆药品养护情况记录(是否按月养护),内容应包括:
药品养护检查时间
生产批号
药品养护质量状况
◆出现质量问题药品的处理措施及凭证是否齐全
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□是□否
序号
检查项目
检查结果
备注
5
是否根据药品养护档案表对药品质量情况进行阶段性的分析汇总
□是□否
6
质量管理机构是否根据企业业务经营活动的变化和药品的质量情况,及时调整重点养护药品品种名单
□是□否
7
◆列出所抽查药品养护档案表的品种名称(不得少于5个):
◆检查组认为企业在药品养护档案管理方面存在的主要问题:
◆请将现场检查中所看到的养护档案表样式复印一份随资料带回
◆如有阶段性分析汇总,请复印一份随资料带回
年月日
表4每年进货质量情况评审档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关企业每年进货质量评审档案管理的内容
□有□无
制度中是否明确质量管理机构应负责组织企业每年进货质量情况的评审并建立档案
□是□否
制度中是否明确评审的具体要求及档案内容
□是□否
2
是否每年对进货质量情况按规定进行评审并建立档案
认证后建档数
档案内容是否包括:
◆每年进货质量情况评审报告
◆评审依据
药品入库验收总批次
质量情况(合格率或不合格率)
药品养护总批次
质量情况(合格率或不合格率)
药品销货退回总批次
质量情况(合格率或不合格率)
监督抽查批次
质量情况(合格率或不合格率)
以上数据是否由相关岗位的人员提供
是否对以上出现不合格药品的供货单位的质量信誉情况进行分析
其它情况分析
□是□否
个
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□是□否
□是□否
□有□无
3
每年进货质量评审报告
◆是否有结论性意见(如停止从哪家企业继续购进药品或供货单位的药品质量情况符合要求等)
◆是否经参加评审的各部门有关人员签字
□有□无
□是□否
4
其它需要说明的问题:
请将检查时看到的年进货质量评审报告复印一份带回。
年月日
表5实施GSP情况内部评审档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关企业应定期对实施GSP情况进行内部评审的内容
□有□无
制度中是否明确质量管理领导小组应负责组织开展实施GSP内部评审并建立档案
□是□否
制度中是否明确内部评审的程序和具体要求并建立档案
□是□否
2
每年是否至少一次开展GSP内部评审并建立档案
认证后建档数/内部评审档案总数
档案内容:
◆是否有每次内部评审报告
◆内部评审是否按制订的程序要求和规范的内容对实施GSP的情况进行全面自查评审并有记录
◆记录是否有检查人签字
次/年
个/个
□有□无
□是□否
□是□否
3
内部评审报告
◆是否明确自查发现的缺陷项目并确定整改措施
◆整改措施是否落实到人(或部门)
□有□无
□是□否
4
◆每次整改是否按整改措施要求进行并整改到位并有整改报告
◆通过每次内部评审,企业质量管理体系是否进一步完善、经营质量管理水平上一台阶
□是□否
□是□否
5
其它需要说明的问题:
年月日
表6企业培训档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关企业培训档案管理的内容
□是□否
制度中是否明确质量管理机构应协助开展对企业职工药品质量管理方面的教育和培训
□是□否
制度中是否明确质量管理机构应协助企业培训档案的建立
□是□否
制度中是否明确企业培训档案应包括的具体内容和要求
□是□否
2
是否建立企业培训教育档案,内容应包括:
◆是否制定企业年度培训计划
◆培训记录是否完整,内容包括:
培训时间
培训对象
培训讲师
培训内容(教材)
培训方式
培训目的
参加培训人员签到表
考核方式
考核结果
外部培训(岗前培训、继续教育等)有无培训证书或证明
□是□否
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
3
是否建立关键岗位员工个人培训教育档案,内容应包括:
姓名
工作部门
职位(职称)
任职时间
培训时间
授课方式
课时
考核方式
考核成绩
培训证书
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
4
自认证后企业每年组织各类人员进行内部培训的次数,其中:
第一年:
第二年:
第三年:
次
次
次
5
通过现场检查和对企业各类人员的现场考核(随机抽查若干名关键岗位的工作人员),判定企业组织各类培训的效果如何
□良好
□一般
□无效
6
其它需要说明的问题:
◆列出所抽查的关键岗位工作人员档案的姓名、职称(职务)、工作岗位(不得少于3个):
◆通过现场检查及考核,认为企业在培训档案管理方面主要存在的问题,以及企业组织的各类培训是否到位,有何欠缺:
年月日
表7质量信息档案检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否涉及有关药品质量信息档案管理的内容
□有□无
制度中是否明确质量管理机构应负责收集和分析药品质量信息并建立企业的质量信息档案
□是□否
制度中是否明确质量信息档案应包括的具体内容及要求
□是□否
2
◆是否建立质量信息档案的目录
◆认证后建立药品质量信息档案的总数
其中:
国家局药品质量公告的信息档案数
省局药品质量公告的信息档案数
企业内部发生质量问题的药品信息档案数
其它与药品经营有关的国家及省局相关文件的信息档案数
其它
□是□否
个
个
个
个
个
个
3
质量信息档案中是否有按信息内容填写的信息传递反馈表,其内容是否包括:
◆质量管理部门填写
信息来源
下发时间
信息接收部门或相关人员
信息内容及要求
◆接收部门按要求处理信息的记录
是否及时反馈本部门对信息处理的结果
◆质量管理部门根据各部门的信息反馈情况汇总后提出处理意见
◆是否能查到信息处理结果相关凭证
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□是□否
□有□无
□是□否
4
质量管理部门是否定期汇总、分析药品质量信息
□是□否
5
其它需要说明的问题:
年月日
表8拆零药品管理检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否包括拆零药品的管理规定
□是□否
制度中是否规定质量管理机构应指导各门店做好拆零药品的销售及管理工作
□是□否
2
通过现场检查,判定门店拆零药品的管理是否规范,具体内容包括:
◆拆零药品的概念(范围)是否确切
◆是否设置拆零药品专柜
◆是否配备必要的拆零工具(药匙、医用手套、拆零药袋等)
◆破坏最小包装单元的拆零药品是否集中存放于拆零药品专柜
◆拆零药品是否保留原包装的标签
◆拆零药品记录的内容应包括:
品名规格
生产企业
批号及有效期
拆零起止日期
剩余数量
质量状况
经手人
◆销售时在拆零药袋上应写明的内容包括:
品名规格
用法用量
批号及有效期
拆零药店
□是□否
□是□否
□是□否
□是□否
□是□否
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
3
◆列出所抽查拆零药品的品种名称(不得少于3个):
◆在拆零药品管理方面存在的主要问题:
年月日
表9药品陈列管理检查内容
企业名称
序号
检查项目
检查结果
备注
1
企业质量管理制度中是否包括药品陈列的管理规定
□是□否
制度中是否规定质量管理机构应指导各门店做好药品的陈列工作
□是□否
2
检查组通过现场检查,判定门店对陈列药品的管理是否规范,具体内容包括:
◆处方药与非处方是否分柜摆放(非处方药以标识为依据)
◆处方药是否未采用开架自选的销售方式
◆特殊药品是否按国家有关规定管理和存放
◆危险品是否不陈列,如需陈列是否只陈列代用品或空包装
◆拆零药品是否集中存放于拆零专柜
◆店堂内陈列药品的质量和包装是否符合规定
◆是否做好店堂内的温湿度记录
◆陈列药品的货柜及橱窗是否保持清洁和卫生
◆陈列药品是否按品种、规格、剂型或用途分类整齐摆放
◆类别标签是否放置准确、字迹清晰
◆中药饮片斗前是否写正名正字
◆陈列药品是否按月进行检查并记录,内容应包括:
品名规格
生产企业
批号及有效期
数量
质量状况
处理意见
检查人
◆对近效期药品是否按月填写“近效期药品报表”
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□是□否
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□有□无
□是□否
3
其它需要说明的问题:
年月日