第二阶段达标题.docx
《第二阶段达标题.docx》由会员分享,可在线阅读,更多相关《第二阶段达标题.docx(27页珍藏版)》请在冰豆网上搜索。
第二阶段达标题
第二阶段达标题
(1)
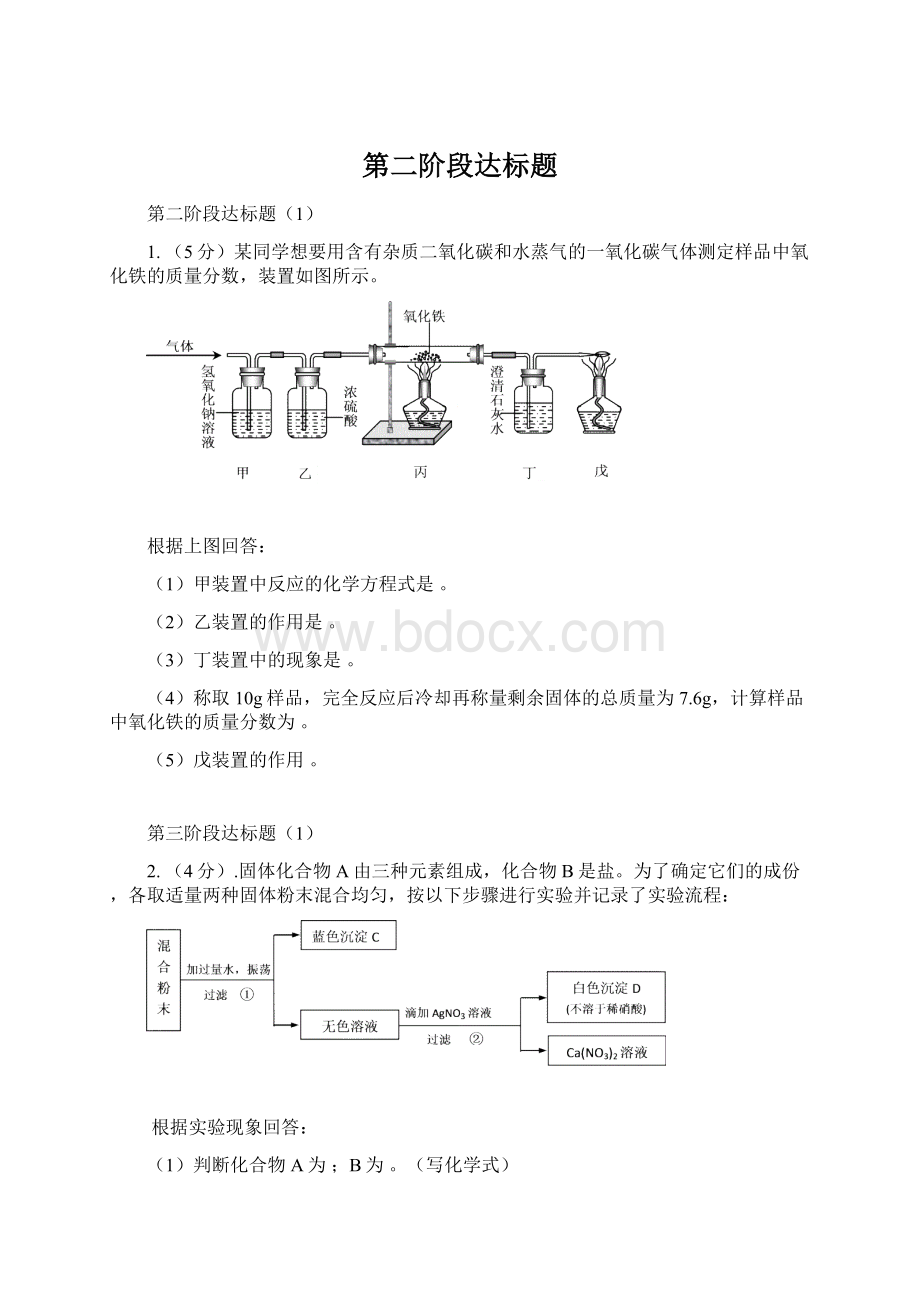
1.(5分)某同学想要用含有杂质二氧化碳和水蒸气的一氧化碳气体测定样品中氧化铁的质量分数,装置如图所示。
根据上图回答:
(1)甲装置中反应的化学方程式是。
(2)乙装置的作用是。
(3)丁装置中的现象是。
(4)称取10g样品,完全反应后冷却再称量剩余固体的总质量为7.6g,计算样品中氧化铁的质量分数为。
(5)戊装置的作用。
第三阶段达标题
(1)
2.(4分).固体化合物A由三种元素组成,化合物B是盐。
为了确定它们的成份,各取适量两种固体粉末混合均匀,按以下步骤进行实验并记录了实验流程:
根据实验现象回答:
(1)判断化合物A为;B为。
(写化学式)
(2)写出步骤②发生反应的化学方程式。
第二阶段达标题
(2)
1.(5分)现有一混合气体,其主要成分为CO,含有少量的水蒸气,可能含有少量CO2。
某化学课题组的同学欲用该混合气体进行系列实验:
①检验CO2气体是否存在,并除去CO2气体②用干燥纯净的CO气体还原氧化铁③实验CO气体还原氧化铁生成的气体生成物的性质。
试用下图所示的仪器组装一套实验装置,完成上述实验任务。
请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这几种仪器组件的连接顺序应是:
混合气体→()→()→()→()。
(2)判定原混合气体中含有CO2气体是否存在的根据是。
(3)仪器D的作用是。
(4)装置C中玻璃管内固体的颜色是由色变为色。
(5)反应进行完全后,若装置C中玻璃管内固体质量减少ag,则参加反应的一氧化碳的质量是(计算结果可为分数形式)。
第三阶段达标题
(2)
2.(4分)现有一固体混合物A的成分,已知其中可能含有NH4C1、(NH4)2SO4、NaOH、Ba(OH)2、MgCl2、CuCl2,六种物质中的两种或多种。
按下图所示进行实验,出现的现象如下图中所述(设过程中所有可能发生的反应均恰好完全反应)。
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)。
(2)混合物A中,肯定存在的物质是(写化学式)。
(3)溶液C中,一定存在的溶质是(写化学式)。
(4)写出实验过程④中发生的化学反应的化学方程式:
。
第二阶段达标题(3)
1.(5分)氢气具有还原性,可在加热条件下还原氧化铜。
小明同学利用氢气的还原性设计下图实验装置测定氧化铜样品(其中的杂质不参与反应)中氧化铜的质量分数。
试回答下列问题:
(1)写出仪器A中发生反应的化学方程式:
。
(2)检验仪器A气密性的方法是:
。
(3)仪器D中的实验现象是:
。
(4)小明同学通过称量反应前、后E部分的质量增加,来计算试样中氧化铜的质量分数,若按这一方案进行实验并记录数据,则计算出的结果和实际值相比将(填“偏大”、“偏小”或“相同”)。
(5)针对该实验装置,你的改进意见是:
。
第三阶段达标题(3)
2.(4分)现欲探究一固体混合物A的成分,已知其中可能含有Mg、CuO、Na2SO4、Na2CO3和NaCl五种物质中的两种或多种。
按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)。
(2)滤渣C是(写化学式)。
(3)混合物A中,肯定存在的物质是(写化学式)。
(4)写出实验过程②中发生化学反应的化学方程式:
。
第二阶段达标题(4)
1.(5分)某气体可能由H2、CO、CO2、H2O、HCl中的一种或几种组成,为确定其成分,进行如下实验:
气体通过有关装置时观察到的现象如下:
装置编号
A
B
C
D
E
试剂
硝酸银溶液
澄清石灰水
氧化铜粉末
澄清石灰水
无水硫酸铜
现象
无明显变化
变浑浊
变红色
无明显变化
变蓝色
试推断:
(1)该气体中一定含有。
(2)该气体中一定没有,理由是。
第三阶段达标题(4)
2.(3分)甲、乙、丙是三种单质,A、B、C是三种化合物,它们之间有下图所示关系:
据此推断乙、B、C的化学式:
乙.,B.,C.。
(每空填一种物质)
第二阶段达标题(5)
1.(5分)用下图所示的仪器组装一套实验装置,并完成下列实验任务:
①用干燥
的CO气体还原CuO②检验CO还原CuO的气体生成物
请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这套装置的连接顺序应是(填仪器接口字
母):
()接(),()接(),()接()。
(2)实验开始时,先通入CO气体,后加热氧化铜的理由是
。
(3)A中澄清石灰水的作用是。
(4)该套实验装置从环境保护的角度考虑可能存在的不足是,
你提出的合理处理建议是。
第三阶段达标题(5)
2.(3分)A、B、C、D分别是NaCl溶液、NaOH溶液、稀硝酸、BaCl2溶液四种溶液中的各一种,现用另一种试剂X(X是MgSO4溶液、Ca(OH)2溶液、稀盐酸、CuSO4溶液四种溶液中的某一种),按如图所示的方法进行实验。
通过实验现象确定:
(1)A是溶液,C是溶液。
(2)X是溶液。
第二阶段达标题(6)
2.(4分)某化学探究活动小组的小峰同学为了测定某不纯氧化铁试样(其中的杂质不参与反应)中氧化铁的质量分数,设计了如下图所示的实验装置。
试回答下列问题:
(1)写出A中发生反应的化学方程式:
。
(2)小峰同学通过称量反应前、后D部分的质量,来计算试样中氧化铁的质量分数,若
按这一方案进行实验并记录数据,则计算出的结果和实际值相比将
(填“偏大”、“偏小”或“相同”)。
(3)对于小峰同学设计的这个实验方案,谈谈你的评价意见和建议:
。
第三阶段达标题(6)
1.(4分)实验室中现有一种固体混合物,其中可能含有Cu(OH)2、CuO、Cu、NaOH、
Na2CO3、CaCl2六种物质中的两种或多种。
按下图所示进行实验,出现的现象如图中所述。
试根据实验过程和发生的现象判断:
(1)产生的气体D是(写化学式)。
(2)混合物A中,一定存在的物质是(写化学式)。
(3)滤液F中,一定存在的溶质是(写化学式)。
(4)写出过程
中可能发生的化学反应中的一个化学方程式:
。
第二阶段达标题(7)
2.(5分)某研究性学习小组学习了工业“侯氏制碱法”的原理后,知道:
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
【提出问题】能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
【实验验证】如图16是该学习小组进行模拟实验时所用到的部分主要装置。
已知浓氨水遇生石灰会产生大量的NH3。
请回答下列问题:
⑴检验A装置气密性的方法是:
塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若,说明装置不漏气。
⑵D是连接在装置A与装置C之间的气体净化装置,进气口是(填a或b),D的作用是除去__________气体。
⑶实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2,其原因是___________。
(填写序号)
①使CO2更易被吸收②NH3比CO2更易制取③CO2的密度比NH3大
⑷用____________的方法将生成的NaHCO3晶体从混合物中分离出来。
【得出结论】利用“侯氏制碱法”在实验室可以制取NaHCO3。
第三阶段达标题(7)
2.(4分)海水的综合利用可以制备金属镁,其流程如图17所示(图中A、B、C均表示主要成分):
请填写下列空白:
⑴C的化学式为____________________。
⑵写出A→B的化学反应方程式_______________________________________。
⑶整个过程中没有涉及到的基本反应类型是________________________________。
⑷若在实验室进行粗盐提纯,溶解、过滤、蒸发(结晶)三步操作中都要用到的玻璃仪器是_________________。
第二阶段达标题(8)
1.(5分)现有一混合气体,其主要成分为CO,含有少量水蒸气,还可能含有少量HCl气体。
某化学课题组的同学欲用该混合气体进行实验:
①检验HCl气体是否存在,并除去HCl气体②用干燥纯净的CO气体还原不纯的氧化铜试样(其中的杂质不发生变化)③实验CO气体还原氧化铜生成的气体生成物的性质
试用如图所示的仪器组装一套实验装置,完成上述实验任务。
请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这几种仪器组件的连接顺序应是(填写仪器导管接口处字母):
()接(),()接(),()接()。
(2)判定HCl气体是否存在的根据是
。
(3)仪器B的作用是。
(4)仪器D中的现象是。
(5)反应进行完全后,若仪器D中物质增重ag,则仪器C中的试样质量减少g.
(计算结果可为分数形式)
第三阶段达标题(8)
2.现有一固体混合物A的成分,已知其中可能含有NH4Cl、KNO3、Na2CO3、(NH4)2SO4、Fe2O3五种物质中的两种或多种。
按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)
(2)混合物A中,肯定存在的物质是(写化学式)
(3)溶液E中,一定存在的溶质是(写化学式)
(4)写出实验过程④中发生的化学反应的化学方程式
第二阶段达标题(9)
1.(5分)由于大量使用一次性塑料方便袋造成的“白色污染”,已成为一个严重的社会问题。
某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H两种元素),他们设计了如图所示的实验装置,使该塑料试样在纯氧气中充分燃烧,观察实验现象,分析有关数据,推算元素含量。
试回答下列问题:
(1)仪器A中所发生反应的化学方程式为。
(2)仪器B的作用是。
(3)仪器E中的现象是。
(4)若仪器C的玻璃管中放入的塑料试样质量为Wg,塑料试样充分燃烧后,若仪器D增重ag,则Wg该塑料试样中含氢元素的质量为g(计算结果可为分数形式)
(5)若装置中没有连接仪器B,将该塑料试样中氢元素的质量测算结果(填“偏小”、“偏大”、“无影响”中之一)。
第三阶段达标题(9)
2.(4分)现欲探究一固体混合物A的成分,已知其中可能含有Mg(OH)2、CuCl2、NH4NO3、(NH4)2SO4、CuO五种物质中的两种或多种。
按下图所示进行实验,出现的现象如下图中所述(设过程中所有可能发生的反应都恰好完全反应)。
试根据实验过程和发生的现象,填写以下空白:
(1)产生的气体B的气味为。
(2)溶液G中一定存在的物质是(写化学式)。
(3)混合物A中,肯定存在的物质是(写化学式)。
(4)写出实验过程④中可能发生的化学反应中的1个化学方程式(只能写1个,多写该空不得分)。
。
第二阶段达标题(10)
1.(5分)现有一定量的含ZnO的锌粒,请从图中选择适当的实验装置,设计一实验测定锌粒的纯度,可供选择的试剂有:
①稀硫酸②稀硝酸③浓硫酸④硫酸铜溶液⑤浓硝酸。
请回答下列问题:
(1)测定纯度可以设计两种方法,一种是最简单的,则选择仪器是(填装置编号)。
戊中选择的药品是(填编号);若气体从左向右流,则接口的顺序为(填接口字母代号);
(2)仪器组装好后,在开始实验时,要先,操作方法是。
(3)若实验样品质量是10g,实验中测定氢气的体积是2.22L(氢气密度为0.09g/L)则样品的纯度为。
第三阶段达标题(10)
2.(4分)有一固体混合物,可能由Na2CO3、CuSO4、BaC12、K2SO4、KCl中的一种或几种混合而成,实验过程及现象如图所示。
试推断:
A是_________,C是__________,
白色固体混合物中一定含有______________,可能含有_____________,一定不含有___________________.
第二阶段达标题(11)
1.用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如下图所示:
根据上图回答:
(1)甲装置的作用是_______________________________;
(2)实验过程中丁装置中没有明显的变化,而戊装置中出现了白色沉淀,则该还原性气体是_________________。
(3)上述实验中,如果没有甲装置,将使测定结果中铁元素与氧元素的质量比_____________(填“偏大”、“偏小”或“无影响”);
(4)如果没有乙装置,测定结果中铁元素与氧元素的质量比_____________(填“偏大”、“偏小”或“无影响”);
第三阶段达标题(11)
2.下图是一定条件下相关物质的转化关系,其中A是只含两种元素的纯净物,B、C、E、F均是初中常见的无色、无味的单一气体。
G溶液显浅绿色.
(1)写出下列物质的化学式
CEFH。
(2)写出符合反应①的一个化学反应方程式:
第二阶段达标题(12)
1.(5分)现有混入少量CO2的一氧化碳气体,某同学欲用纯净、干燥的CO还原氧化铁,并验证反应的一种产物。
根据下图所示实验装置回答(其中A处框图表示盛有CO2和CO混合气体的贮气瓶):
⑴请用字母标号表示装置连接的正确顺序(每种装置只能用一次):
A
⑵B装置中反应的化学方程式为
⑶C装置中可以观察到的实验现象是
⑷D装置的作用是
⑸对于上述实验方案,谈谈你的评价意见和建议:
第三阶段达标题(12)
2.(4分)实验室中现有一种固体混合物,其中可能含有Mg、Na2SO4、Na2CO3、BaCl2、BaSO4五种物质中的两种或多种。
按下图所示进行实验,出现的现象如图中所述。
(设所有可能发生的反应均已发生)
试根据实验过程和发生的现象判断:
⑴产生的气体B是(写化学式)。
⑵混合物A中,一定存在的物质是(写化学式)。
⑶滤渣D中含有的物质是(写化学式)。
⑷写出步骤③中一定发生的一个化学反应的方程式:
。
第二阶段达标题(13)
1.(5分)己知乙醇(C2H5OH)完全燃烧时生成C02和H2O。
如果氧气不充足,乙醇燃烧还可能生成C0。
现用以下装置进行实验,确证乙醇燃烧产物中有C0、C02和H2O。
请回答下列问题;
(1)能确证产物中有H2O的现象是无水CuSO4变蓝;能确证产物中有CO的现象是:
(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化。
B装置的作用;
C装置的作用是;D装置的作用是。
(3)若乙醇燃烧产物中C0和C02的总质量为25.2g,其中碳元素与氧元素的质里比为
2:
5,则参加化学反应的乙醇的质量为,反应产物中H2O的质量为。
第三阶段达标题(13)
2.(4分)现欲通过实验确定一固体混合物A的成分,已知其中可能含有NaCl、CuO、Na2CO3、Cu四种物质中的两种或多种。
按下图所示进行实验,出现的现象如图中所述。
(假设有关化学反应均恰好完全反应)。
试根据以上实验过程和现象填写以下空白:
(1)混合物A中,一定存在的物质是(写化学式)。
(2)混合物A中一定不存在的物质是(写化学式)。
(3)滤液D中,一定存在的溶质是(写化学式)。
(4)写出实验过程④中所发生的化学反应的化学方程式:
。
第二阶段达标题(14)
1(4分)用下列装置验证某混合气体一定含有H2O、CO2、H2三种气体并验证氢气的性质,某同学组装了下列仪器装置,请回答问题:
(已知:
H2具有和CO相似的还原性H2+CuO=Cu+H2O;碱石灰既可以吸水也可吸收二氧化碳)
碱石灰
ABCDEFG
⑴证明CO2存在的现象是;
⑵证明H2O存在的现象是;
⑶E装置的现象;
⑷如果通过F装置反应前后质量变化来计算参加反应的氧化铜的质量,没有G装置会使计算数值(填“偏大”、“偏小”“不受影响”)
第三阶段达标题(14)
2(4分)实验室中现有一种固体混合物,其中可能含有Ba(OH)2、Fe2O3、Cu、Na2CO3、四种物质中的两种或多种。
按下图所示进行实验,出现的现象如图中所述。
②加适量氯化铵
恰好完全反应
气体D
滤液B
滤液F(无色)
气体E
③加过量稀盐酸,微热
充分反应后过滤
①加足量水
充分溶解后过滤
固体混合物
A
沉淀C
沉淀G
试根据实验过程和发生的现象判断:
⑴产生的气体E是(写化学式)。
沉淀G是(写化学式)。
⑵混合物A中,一定不存在的物质是(写化学式)。
⑶写出过程
中发生的化学反应的化学方程式:
。
第二阶段达标题(15)
1.下图为常见的实验装置(各具用途),根据下列要求回答问题。
装置可重复使用。
提示:
H2+CuO
Cu+H2O
ABCDE
⑴将含水蒸气的氢气干燥后还原氧化铜,则该气体先要通过装置_____。
(填序号,下同)
⑵如果验证混合体中有H2和H2O,需连接的仪器顺序是_______________。
⑶如果验证混合气体中有H2、CO和H2O,则需连接的仪器顺序为__________。
⑷如果验证混合气体中有CO2、CO、H2,则需连接的仪器顺序是。
第三阶段达标题(15)
2、A是一种白色难溶于水的钙盐,由三种元素组成,其式量为100。
(1)用化学式表示:
A___________________,B___________________
(2)写出A与盐酸反应的化学方程式:
______________________________________
(3)D中含有的溶质可能有哪几种情况?
____________________________________________________________________
第二阶段达标题(16)
1.(6分)某实验小组利用下面装置制取二氧化碳气体,请根据装置回答:
①欲制取一瓶二氧化碳气体,应选用装置是_______,有关化学方程式为____________________;
②一同学利用装置C验证制得的气体时未看到浑浊现象,可能的原因是____________________,___________________________;
③要得到干燥的二氧化碳气体,还应用到装置______________________________;
④要吸收反应多余的二氧化碳最好使用装置D而不用装置C,是因为______________________________。
第三阶段达标题(16)
2.(5分)A是绿色粉末,G是蓝色溶液,X为常见的稀酸,B、C、D、E、F、H和Y中初中化学常见的物质。
它们之间转化关系如下图所示,反应①、②、③、④和⑤是初中化学常见的反应。
请回答下列问题。
(1)写出化学式:
D,E,X。
(2)写出化学方程式:
反应②;
反应④。
第二阶段达标题(17)
1、某课外小组的同学们收集了含一氧化碳和二氧化碳的废气,为了确认这种废气的组成,他们在实验室按如下装置进行了实验。
(l)B装置中盛放足量浓氢氧化钠溶液,其作用是_______________。
(2)C装置中发生反应的化学方程式是_____________________。
(3)A装置和D装置完全相同,其作用的不同之处是_____________________
____________________________________。
(4)对设计的这个实验方案,谈谈你的评价意见和建议。
第三阶段达标题(17)
2.(4分)现有一固体混合物A的成分,已知其中可能含有CuO、Na2CO3、(NH4)2SO4、Ba(OH)2四种物质中的两种或多种。
按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均完全反应)。
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)
(2)混合物A中,肯定不存在的物质是(写化学式)
(3)溶液C中,一定存在的溶质是(写化学式)
(4)写出实验过程③中发生的化学反应的化学方程式
第二阶段达标题(18)
1.(8分)已知某纯碱试样中含有杂质氯化钠,为测定试样中纯碱的质量分数,可用下图装置进行实验。
主要步骤如下,请填空:
①按图组装仪器,并检查__________________;②将10g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;③称量盛有碱石灰的U形管的质量为300g;④从分液漏斗中滴入20%的稀硫酸,直到________________为止,写出反应的化学方程式__________________________;⑤从导管A处缓缓鼓入一定量的空气;⑥再次称量盛有碱石灰的U形管的质量;⑦重复⑤和⑥的操作,直到U形管的质量基本不变,测得质量为303.3g。
回答下列问题:
(1)装置中浓硫酸的作用是___________________________________。
(2)步骤⑤的目的是_________________________________________。
(3)试样中纯碱的质量分数为_________________________________。
(4)分液漏斗中的稀H2SO4不能换成浓盐酸,理由是______________________________。
(5)若用生成沉淀的方法来测定试样中纯碱的质量分数,应选用的试剂是____________。
第三阶段达标题(18)
2、纯碱在日常生活和化学工业中用途很广,如用于硬水软化、洗涤剂生产、食品加工、石油精炼、粗盐精制、玻璃制造等领域。
工业上以食盐、氨气(主要由合成氨厂提供)和二氧化碳为主要原料生产纯碱。
其流程如下:
已知有关物质重要反应的化学方程式如下:
△
①NaCl+NH3+H2O+CO2====NaHCO3↓+NH4Cl
△
②2NaHCO3====Na2CO3+H2O+CO2↑
△
③2NH4Cl+X====2NH3↑+CaCl2+2H2O
④NH4Cl====NH3↑+HCl↑
根据以上信息回答下列问题。
(1)盐水精制的过程是除去溶液中各种杂质的过程。
为将盐水中含有的Ca2+、Mg2+等沉积,可以向其一和加入过量纯碱.此时将混合