人教版九年级上学期期末化学试题II卷新编.docx
《人教版九年级上学期期末化学试题II卷新编.docx》由会员分享,可在线阅读,更多相关《人教版九年级上学期期末化学试题II卷新编.docx(11页珍藏版)》请在冰豆网上搜索。
人教版九年级上学期期末化学试题II卷新编
人教版2020年九年级上学期期末化学试题(II)卷
姓名:
________班级:
________成绩:
________
一、单选题
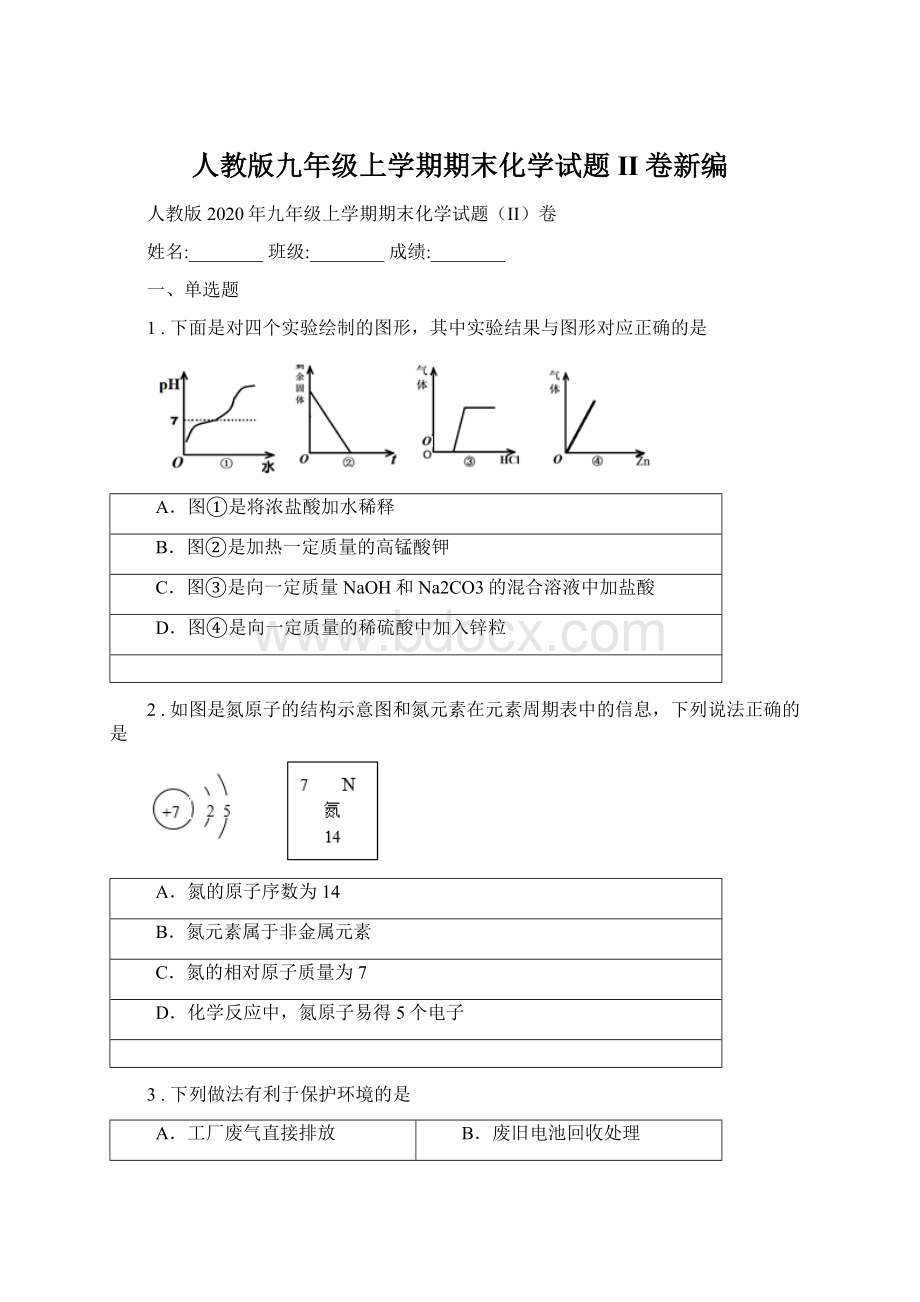
1.下面是对四个实验绘制的图形,其中实验结果与图形对应正确的是
A.图①是将浓盐酸加水稀释
B.图②是加热一定质量的高锰酸钾
C.图③是向一定质量NaOH和Na2CO3的混合溶液中加盐酸
D.图④是向一定质量的稀硫酸中加入锌粒
2.如图是氮原子的结构示意图和氮元素在元素周期表中的信息,下列说法正确的是
A.氮的原子序数为14
B.氮元素属于非金属元素
C.氮的相对原子质量为7
D.化学反应中,氮原子易得5个电子
3.下列做法有利于保护环境的是
A.工厂废气直接排放
B.废旧电池回收处理
C.生活污水任意排放
D.随意丢弃塑料袋
4.物质的性质决定物质的用途。
下列各物质用途利用到物质化学性质的是()
A.金属铜用来做导线
B.金刚石用来裁玻璃
C.用氦气填充探空气球
D.酒精用作酒精灯燃料
5.下列说法中不正确的是()
A.可以用水鉴别NaCl、NH4NO3、NaOH三种白色固体
B.少量浓硫酸溅到皮肤,可用大量水清洗,再涂上3%-5%的氢氧化钠溶液
C.红磷在氧气中燃烧时产生大量白色烟
D.实验室中,不慎将燃着的酒精灯碰倒,酒精在桌面上燃烧,应立即用湿抹布盖灭
6.能闻到花香,说明分子的性质是
A.分子的体积很小
B.分子的质量很小
C.分子在不断运动
D.分子之间有间隔
7.为落实主体责任、完善监管制度等,2017年将修订《安徽省环境保护条例》。
下列说法不符合该条例的是()
A.增加植树绿化面积
B.城市道路使用节能灯
C.加强长江流域污水排放监控
D.为方便生活多使用塑料袋
8.现代社会对能源的需求量越来越大.下列图示中,不是利用环保新能源发电的是()
A.太阳能发电
B.风力发电
C.潮汐和海风发电
D.火力发电
9.铁路列车实行大提速的有效措施是将原有铁路短轨或长轨焊接为超长轨,常用:
2Al+Fe2O3
Al2O3+2Fe,这一反应原理来焊接钢轨。
对该反应说法错误的是()
A.该反应是置换反应
B.根据反应,54g铝完全反应可以得到112g铁
C.反应前后元素的化合价都发生改变
D.在金属活动性顺序中:
铝>铁
10.下列关于溶液的说法中,正确的是
A.溶液是由溶质和溶剂组成的
B.溶液是一种纯净物
C.溶液都是无色的
D.溶液中只能含有一种溶质
11.下列有关水的说法正确的是()
A.地球上可利用的淡水资源取之不尽,用之不竭
B.湘江的水经过沉淀、过滤、吸附后,可以得到纯水
C.为了保护水资源,禁止使用化肥和农药
D.用肥皂水可以区分软水和硬水
12.下列工、农业生产中,没有涉及化学变化的是
A.高粱生产食醋
B.利用空气制氧气
C.铁矿石炼铁
D.焚烧垃圾发电
13.今年夏天南京青奥会前,青奥火炬载着中国人民对世界人民的友谊,进行了全球传递。
它采用的燃料是丙烷(分子结构模型如图),下列关于丙烷分子的说法不正确的是
A.丙烷由碳元素和氢元素组成
B.丙烷分子中碳原子和氢原子的个数比为3:
8
C.丙烷的化学式为C3H8
D.一个丙烷分子中含有11个质子
14.建立模型是学习化学的重要方法,下列有关模型正确的是()
A.
空气组成
B.
原子结构
C.
微粒与元素关系
D.
地壳中元素含量
15.病人输液时常用的葡萄糖的化学式是C6H12O6,下列有关叙述正确的是()
A.葡萄糖由6个碳原子和6个水分子构成
B.葡萄糖分子由碳、氢、氧元素组成
C.葡萄糖是一种氧化物
D.葡萄糖分子中碳、氢、氧原子个数比是1:
2:
1
16.化学方程式正确的是()
A.4P+5O2
2P2O5
B.4Fe+3O2
2Fe2O3
C.Cu+2AgCl→CuCl2+2Ag
D.2Fe+6HCl→2FeCl3+3H2↑
17.2011年4月11日央视《消费主张》:
超市馒头这样出炉;生产日期随便改;防腐剂、甜蜜素齐上阵(甜蜜素的化学式——C6H12NNaO3S)。
下列有关甜蜜素的说法正确的是
A.该物质是由五种元素组成的
B.该化合物中C、N两种元素的质量比为6︰1
C.甜蜜素完全燃烧的产物中可能含有NO2气体
D.每个甜蜜素分子是由23个原子构成的
18.下列有关仪器使用或用途的叙述中正确的是()
A.试管:
加热时所盛液体的体积不能超过试管容积的2/3
B.胶头滴管:
向试管中滴加液体时应将胶头滴管伸入试管内
C.酒精灯:
熄灭酒精灯可用嘴吹灭
D.玻璃棒:
常用于搅拌、过滤、转移液体
19.下列关于铁丝在氧气中燃烧和铁丝生锈的说法不正确的是()
A.铁丝在氧气中燃烧,火星四射,生成黑色固体
B.铁丝生锈是缓慢氧化
C.铁丝燃烧的产物是四氧化三铁
D.铁丝生锈是物理变化
20.下列能正确反映相关变化关系的是()
A向一定质量的二氧化锰中加入过氧化氢溶液
B一定量的硫粉与过量的氧气在密闭容器内点燃并充分反应
C加热一定质量的高锰酸钾固体
D等质量CaCO3分别与等体积等浓度的稀盐酸(足量)反应
A.A
B.B
C.C
D.D
二、实验题
21.实验室用高锰酸钾制取氧气,并验证氧气的化学性质。
(1)实验1中反应的化学方程式为_____;
(2)实验2中,证明木炭发生反应依据是_____。
写出木炭充分燃烧的化学方程式为_____。
三、流程题
22.某金属冶炼厂在生产过程中产生了一定量的含铜废料
化学兴趣小组利用稀硫酸和铁粉分离回收铜,并获得硫酸亚铁晶体
其设计方案如图所示.
查阅资料得知:
在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜,反应的化学方程式:
。
(1)步骤Ⅰ中分离得到固体A和蓝色溶液B,操作的名称是_____.
(2)蓝色溶液B中的溶质是_____
填化学式
.
(3)写出步骤Ⅲ中发生反应的化学方程式_____.
(4)铜制品在空气中会发生锈蚀[铜锈的主要成分是Cu2(OH)2CO3],根据铜锈的主要成分,可以推断出铜生锈除了需要氧气外,还需要空气中的_____和 _____(填名称或化学式).
四、科学探究题
23.金属是现代生活和工业生产中应用极为普遍的一类材料。
(一)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快。
Al、Cu、Fe三种金属在稀盐酸里的反应现象如图1所示。
(1)图1中Y所代表的金属是_____(填“Cu”或“Fe”);
(2)Al、Cu、Fe三种金属的活动性由强到弱的顺序为_____;
(3)铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是_____;(用方程式表示化学原理)
(二)防止金属腐蚀,特别是钢铁的锈蚀是世界科学研究和技术领域中的重大问题。
铁生锈的条件为铁与_____、_____ 同时接触,_____(举一例物质)可加速铁的锈蚀。
为了防止铁制品生锈,应采取的措施是_____(写出一种)。
(查阅资料)铁锈成分复杂,化学式可简单表示为Fe2O3•nH2O.浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
(提出问题)铁锈(Fe2O3•nH2O)中n的值等于多少呢?
(问题探究)小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3•nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。
(4)实验前应先______。
(5)为了保证实验安全,实验开始时应先_____,目的是_____。
(6)A中的现象是_____,请指出该装置中有一处明显不足_____。
(数据处理)图3是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。
反应前(g)
反应后(g)
B
100
105.4
C
150
163.2
(7)写出T3﹣T4时间段发生反应的化学方程式________。
(8)计算原样品中单质铁的质量分数是______。
(计算结果保留1位小数)
(9)n的值是_____。
五、计算题
24.有一种石灰石样品(主要成分是CaCO3和SiO2)。
课外小组同学将100g盐酸加入到30g石灰石样品中(已知SiO2不与盐酸反应,也不溶于水。
实验过程中溶液损失忽略不计),完全反应后测得烧杯中剩余物质质量是121.2g。
请计算。
(1)反应后生成的二氧化碳的质量是___________。
(2)该石灰石样品中CaCO3的质量分数________________?
(写出计算过程)
参考答案
一、单选题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
16、
17、
18、
19、
20、
二、实验题
1、
三、流程题
1、
四、科学探究题
1、
五、计算题
1、