中考化学备考之流程图压轴突破训练培优篇附答案.docx
《中考化学备考之流程图压轴突破训练培优篇附答案.docx》由会员分享,可在线阅读,更多相关《中考化学备考之流程图压轴突破训练培优篇附答案.docx(16页珍藏版)》请在冰豆网上搜索。
中考化学备考之流程图压轴突破训练培优篇附答案
一、中考初中化学流程图
1.化学是认识、改造和应用物质的科学。
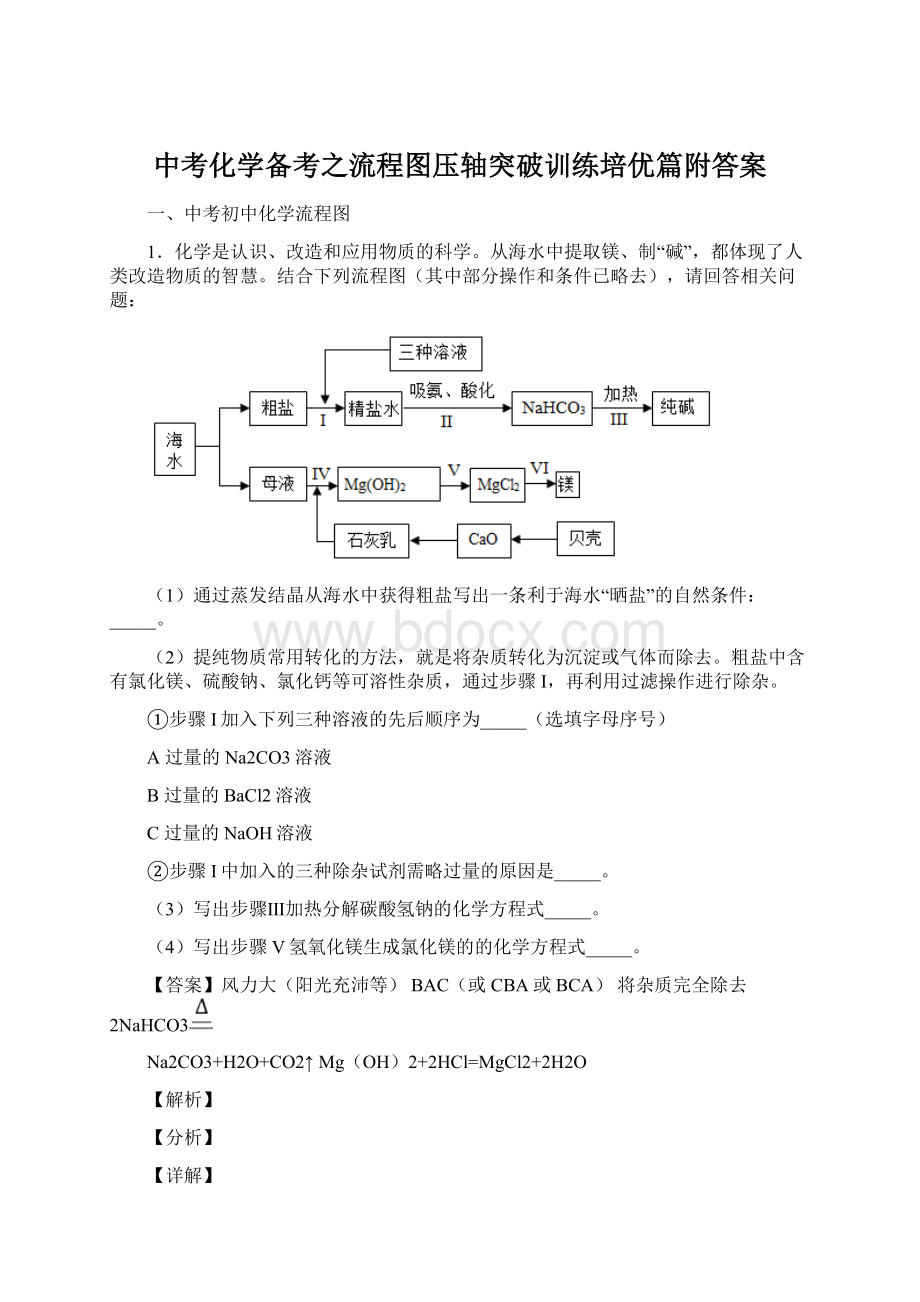
从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。
结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
(1)通过蒸发结晶从海水中获得粗盐写出一条利于海水“晒盐”的自然条件:
_____。
(2)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。
粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤I,再利用过滤操作进行除杂。
①步骤I加入下列三种溶液的先后顺序为_____(选填字母序号)
A过量的Na2CO3溶液
B过量的BaCl2溶液
C过量的NaOH溶液
②步骤I中加入的三种除杂试剂需略过量的原因是_____。
(3)写出步骤Ⅲ加热分解碳酸氢钠的化学方程式_____。
(4)写出步骤V氢氧化镁生成氯化镁的的化学方程式_____。
【答案】风力大(阳光充沛等)BAC(或CBA或BCA)将杂质完全除去2NaHCO3
Na2CO3+H2O+CO2↑Mg(OH)2+2HCl=MgCl2+2H2O
【解析】
【分析】
【详解】
(1)风力大、阳光充沛等都利于水分的蒸发,有利于“晒盐”;
(2)①粗盐水中主要含有MgCl2、Na2SO4和CaCl2等可溶性杂质,所加试剂的顺序是加入稍过量的BaCl2溶液除去Na2SO4,再加稍过量的Na2CO3溶液,除去CaCl2和过量的BaCl2,加稍过量的NaOH溶液,除去MgCl2,顺序不唯一,只要把稍过量的BaCl2溶液放在稍过量的Na2CO3溶液前面加入就行;故顺序为BAC(或CBA或BCA);
②该实验过程中,除杂试剂都要过量,原因是将杂质完全除去。
(3)碳酸氢钠在加热的条件下分解为碳酸钠、二氧化碳和水;化学方程式2NaHCO3
Na2CO3+H2O+CO2↑;
(4)氢氧化镁和盐酸反应生成氯化镁和水;化学方程式:
Mg(OH)2+2HCl=MgCl2+2H2O。
2.某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计如图所示实验。
依据实验流程回答相关问题。
(1)向溶液a中加入紫色石蕊试液,现象是__________________。
(2)白色固体b一定是_______________(填化学式)。
(3)加入过量稀HNO3的目的是_______________。
(4)现象c:
①若无白色沉淀,干燥剂成分为_______________。
②若有白色沉淀,写出产生此现象的化学方程式_______________。
【答案】溶液变蓝CaCO3完全除去NaOH、Na2CO3,以免干扰检验CaCl2CaO和NaOH
【解析】
【分析】
【详解】
(1)某干燥剂含有CaO、NaOH和CaCl2中的两种物质,氧化钙遇水会反应生成氢氧化钙,加水后形成的溶液a(至少含有氢氧化钙或氢氧化钠中的一种)一定呈碱性,所以溶液a中加入紫色石蕊试液,溶液一定会是蓝色。
故填:
溶液变蓝。
(2)溶液a中加入过量碳酸钠后形成白色固体b,而干燥剂中含有CaO、NaOH和CaCl2中的两种物质,氧化钙遇水反应生成氢氧化钙,所以白色固体b一定是碳酸钠与氢氧化钙或氯化钙反应生成的碳酸钙沉淀。
故填:
CaCO3。
(3)溶液a中加入过量碳酸钠后,碳酸钠与氢氧化钙反应生成碳酸钙沉淀与氢氧化钠,或是碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠溶液,溶液中一定会有碳酸钠,可能含有氢氧化钠或氯化钠,向溶液中加入过量稀HNO3,再滴加硝酸银,硝酸银与氯化钠反应会生成氯化银白色沉淀,目的是想检验溶液中是否含有氯化钠,从而确定干燥剂中是否含有氯化钙,但是氢氧化钠和碳酸钠会对氯化钠的检验造成干扰,它们遇到硝酸银也会产生白色沉淀,为排除他们的干扰,所以加入过量稀硝酸,将氢氧化钠和碳酸钠都转化为硝酸钠和水及二氧化碳(逸散到空气中),所以加入过量稀HNO3的目的是完全除去NaOH、Na2CO3,以免干扰检验CaCl2。
故填:
完全除去NaOH、Na2CO3,以免干扰检验CaCl2。
(4)根据以上分析,加入过量稀硝酸,稀硝酸与氢氧化钠和碳酸钠分别反应后会生成硝酸钠、水和二氧化碳(跑走),若溶液中有氯化钠,硝酸银与氯化钠反应会生成氯化银白色沉淀,现象c:
①若无白色沉淀,干燥剂中不含氯化钙,所以干燥剂的成分为CaO和NaOH。
故填:
CaO和NaOH。
②若有白色沉淀,硝酸银与氯化钠反应生成氯化银沉淀和硝酸钠,产生此现象的化学方程式
。
【点睛】
根据氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠等知识进行分析解答。
3.某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石。
下图是利用该镁矿石制备七水硫酸镁(MgSO4·7H2O)的工艺流程。
已知CaSO4和MgSO4的溶解度曲线如图所示。
根据以上信息回答下列问题:
(1)反应前将镁矿石粉碎的目的是________________
(2)写出步骤①中碳酸镁与硫酸发生反应的化学方程________________
(3)沉淀A的成分是SiO2和部分硫酸钙,过滤1后得到的滤液中的溶质除了MgSO4还有____________。
(4)步骤⑥中的操作a名称是____________。
【答案】增大反应物的接触面积,加快反应速率,使反应进行得更充分MgCO3+H2SO4=MgSO4+H2O+CO2↑CaSO4降温结晶
【解析】
【分析】
【详解】
(1)因为自然界中开采出来的镁矿石是块状的,如果不将其粉碎,稀硫酸只能和块状镁矿石的表面接触,接触面积较小,反应速率较慢。
因此反应前将镁矿石粉碎的目的是:
增大反应物的接触面积,加快反应速率,使反应进行得更充分;
(2)步骤①中碳酸镁与硫酸反应产生硫酸钠、水和二氧化碳,其化学方程式是:
:
MgCO3+H2SO4=MgSO4+H2O+CO2↑
(3)沉淀A的成分是SiO2和部分硫酸钙,过滤1后得到的滤液中的溶质除了MgSO4还有硫酸钙(CaSO4)。
因为硫酸钙微溶于水,大部分变为沉淀,但有少部分溶解在水中。
(4)从题中提供的溶解度曲线可知,硫酸镁的溶解度受温度影响加大,故步骤⑥中将溶液浓缩蒸发,然后降温结晶,就会有七水硫酸镁晶体析出。
因此操作a的名称是:
降温结晶。
4.用金属铁制备自来水新型消毒、净水剂Na2FeO4的流程如下,请回答下列问题:
(1)固体B中的物质是_______;Na2FeO4属于______(填“酸”、“碱”、“盐”、“氧化物”).
(2)操作Ⅰ的名称是________;该操作能使A、B分离的原因是_________.
(3)反应②的基本反应类型为:
_______;反应③的化学方程式为:
________.
(4)溶液C中的溶质组成存在_________种可能性.
【答案】Fe和Cu盐过滤A是液体,B是固体(合理皆可)复分解反应2Fe(OH)2+H2O2=2Fe(OH)3三
【解析】
【分析】
【详解】
(1)由反应的流程可知,过量的铁粉与硫酸铜反应,生成了硫酸亚铁和铜,由于铁是过量的,在过滤后得到的固体B是Cu,Fe的混合物;Na2FeO4是金属离子和酸根离子构成的化合物,属于盐。
故填:
Fe和Cu;盐;
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤。
故填:
过滤;A是液体,B是固体(合理皆可);
(3)反应②是硫酸亚铁与氢氧化钠反应生成氢氧化亚铁和硫酸钠,反应的方程式是:
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,该反应是两种化合物交换成分生成另外两种化合物,属于复分解反应;反应③是氢氧化亚铁被过氧化氢氧化为氢氧化铁,方程式是:
2Fe(OH)2+H2O2=2Fe(OH)3。
故填:
复分解反应;2Fe(OH)2+H2O2=2Fe(OH)3;
(4)若氢氧化钠溶液与硫酸亚铁溶液恰好完全反应,所得溶液中只有一种溶质——硫酸钠;若氢氧化钠过量,则有两种溶质﹣﹣硫酸钠和氢氧化钠;若硫酸亚铁过量,则有两种溶质﹣﹣硫酸钠和硫酸亚铁。
故填:
三。
【点睛】
本题给出了制取物质的反应流程图,对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理.再结合有关的知识分析解答有关的问题。
5.四氧化三铁可用于医疗器械、电子等工业。
某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
(阅读资料)
(1)25℃时,氢氧化物沉淀的pH范围如表
Zn(OH)2
Fe(OH)2
Mg(OH)2
开始沉淀的pH
5.7
7.6
10.4
沉淀完全的pH
8.0
9.6
12.4
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
(3)制备Fe3O4的实验流程如下:
(回答问题)
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为______________(写一个即可)。
(2)操作a的名称为___。
该操作需要的玻璃仪器有烧杯、玻璃棒、__________等。
玻璃棒在此操作中的主要作用是___。
(3)溶液1所含溶质有_______(至少写两种);溶液3所含溶质的主要成分为___。
【答案】2NaOH+ZnSO4═Zn(OH)2↓+Na2SO或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4过滤漏斗引流硫酸镁、硫酸钠、氢氧化钠(两种即可)硫酸亚铁
【解析】
【分析】
【详解】
(1)加入氢氧化钠溶液后,调节PH至9.6,可以判断能形成得到氢氧化锌和氢氧化亚铁沉淀,,反应的化学方程式为:
2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4;
(2)经过操作a后得到了固体和溶液,所以可以判断操作a的名称为过滤,过滤需要漏斗,玻璃棒在该过程中的作用为引流;
(3)加入氢氧化钠后,硫酸锌和氢氧化钠反应生成了硫酸钠,氢氧化镁只有在pH值等于10.4时,才会沉淀,所以溶液中还含有硫酸镁,向固体1中加入氢氧化钠溶液,根据题给信息可以知道25℃时,Zn(OH)2可溶于pH>10.5的碱溶液,所以氢氧化锌要溶解,剩余的固体2为氢氧化亚铁,所以加入稀硫酸后溶液3的溶质为硫酸亚铁;
故答案为:
(1)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4;
(2)过滤;漏斗;引流;(3)硫酸镁、硫酸钠、氢氧化钠(两种即可);硫酸亚铁。
6.碱性锌锰干电池(内部填充物为锌粉、碳粉、KOH、MnO2等)是目前应用广泛的家用电池,在使用过程中会转化为氢氧化氧锰(MnOOH)和ZnO。
化学兴趣小组取出旧碱性锌锰干电池中的固体填充物,在常温下做如图过程处理:
[资料在线]
(1)MnO2不溶于水,且常温下不与稀盐酸反应。
(2)氢氧化氧锰与盐酸反应的化学方程式为:
2MnOOH+2HCl=MnCl2+MnO2+2H2O。
请回答:
(1)步骤①发生了中和反应,溶液的pH下降至9并生成一种盐,该盐的化学式为____。
(2)步骤②中稀盐酸与三种物质反应,其中可产生无色无味的可燃性气体的反应化学方程式为____;其中与氧化锌的反应,属于_____(填基本反应类型)。
(3)滤渣B中除含氧元素以外,一定还含有_____元素。
(4)若MnO2全部转化为MnOOH时,则电池电量耗尽。
借助仪器测得滤液乙中的锰元素质量占旧电池中锰元素总质量的22%,该旧电池电量理论上已使用____%。
【答案】KClZn+2HCl=ZnCl2+H2↑复分解反应C、Mn44%
【解析】
【详解】
(1)步骤1发生酸碱中和反应,为电池中的碱KOH和稀盐酸反应,生成盐为KCl。
(2)生成无色无味可燃性气体,推测为氢气,反应方程式:
Zn+2HCl=ZnCl2+H2↑。
盐酸与氧化锌的反应生成氯化锌和水,是两种化合物相互交换成分生成另外两种化合物,属于复分解反应。
(3)滤渣B中有不参与反应的碳粉和反应后剩余MnO2,因此,滤渣B中除含氧元素以外,一定还含有C、Mn元素
(4)滤液乙中的锰离子来自于氢氧化氧锰(MnOOH)与盐酸反应,测得滤液乙中的锰元素质量占旧电池中锰元素总质量的22%,根据方程式2MnOOH+2HCl=MnCl2+MnO2+2H2O,计算可知氢氧化氧锰(MnOOH)的锰元素质量是滤液中锰离子质量的2倍,占44%。
所以该旧电池电量理论上已使用44%。
7.化工厂用废硫酸制备K2SO4的流程如下:
(1)生产上将CaCO3研成粉末的目的是_______欲达此目的,还可采用的方法是__________(任写一条)
(2)上述流程中,还可循环使用的物质是___(填写化学式).
(3)写出反应①中主要的化学方程式_______
(4)反应③中相关物质的溶解度如下表所示,反应③在常温下可实现的原因是______
物质
KCl
K2SO4
NH4Cl
(NH4)2SO4
溶解度/g(20℃)
34.2
11.1
37.2
75.4
(5)洗涤反应③所得晶体最适宜的试剂是___________(填序号)
AH2OB饱和K2SO4溶液C二者均可
(6)检验K2SO4晶体是否洗涤干净的方法是____________
【答案】加快反应速率搅拌CO2和CaCO3H2SO4+CaCO3=CaSO4+CO2↑+H2O常温下K2SO4的溶解度小B取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净。
【解析】
【详解】
(1)将CaCO3研成粉末,可以增大反应物的接触面积,其目的是加快反应速率,欲达此目的,还可采用的方法是将反应物混合后充分搅拌;(或其他合理答案)
(2)观察上述流程,发现二氧化碳和碳酸钙既是反应物也是生成物,故可循环使用的物质有CO2和CaCO3;
(3)①中主要的化学方程式:
H2SO4+CaCO3=CaSO4+CO2↑+H2O;
(4)根据复分解反应发生的条件,反应Ⅲ中虽然没有不溶物,但常温下K2SO4的溶解度小,在生成物中会以沉淀的形式出现,故反应可以进行;
(5)洗涤反应③所得晶体最适宜的试剂是饱和硫酸钾溶液,不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;
(6)银离子和氯离子结合生成氯化银沉淀,为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根离子,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净。
8.氯化亚铜(CuCl)是一种白色粉末,不溶于水、乙醇(标准状况下沸点是78.2℃)及稀硫酸,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用于有机合成工业中的催
化剂。
以粗盐水(含氯化钙、硫酸镁等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下(其中①②③为依次加入):
⑴A溶液中溶质的化学式是______________;
⑵写出反应III的化学方程式_____________________________________________;
⑶反应VI的化学方程式是:
2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4,反应中化合价升高的元素是____________________;
⑷本工艺中可循环利用的物质是________________________________________;
⑸反应VI后,过滤得到的CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却密封包装即得产品。
70℃真空干燥的目的是___________________。
【答案】
S(或硫)
与
防止
被氧化,加快乙醇与水的蒸发(答不全不给分)
【解析】
(1)加入氯化钡溶液可以除去硫酸根离子,加入碳酸钠溶液可以除去钙离子和过量的钡离子,加入氢氧化钠溶液可以除去镁离子,因此A溶液是碳酸钠溶液,碳酸钠的化学式是Na2CO3;
(2)反应III中,电解饱和食盐水时,氯化钠和水反应生成氢氧化钠、氢气和氯气,反应的化学方程式为:
;(3)反应2NaCl+2CuSO4+SO2+2H2O=2CuCl↓+2H2SO4+Na2SO4中,氯化钠中钠元素的化合价是+1,氯元素的化合价都是−1,硫酸铜中铜元素的化合价是+2,硫元素的化合价是+6,氧元素的化合价是−2,二氧化硫中硫元素化合价是-4,氧元素化合价是−2,水中氢元素化合价是+1,氧元素化合价是−2,氯化亚铜中铜元素的化合价是+1,氯元素化合价是−1,硫酸中氢元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是−2,硫酸钠中钠元素化合价是+1,硫元素的化合价是+6,氧元素的化合价是−2,因此反应中化合价升高的元素是硫元素,由+4变成+6,故反应中化合价升高的元素是S;(4)本工艺中可循环利用的物质是NaOH、H2SO4,电解生成的氢氧化钠可应用于反应Ⅰ,反应VI中生成的硫酸可应用于反应Ⅴ;(5)70℃真空干燥的目的是加快乙醇和水的蒸发,防止CuCl被空气氧化。
9.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。
其生产工艺流程示意图如下:
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸等除杂、精制。
则加入试剂合理的顺序为_____________(填字母序号)。
A.①②③B.③②①C.①③②
(2)加盐酸的作用是(用方程式表示)________________、______________。
(3)制碱原理可看作是由①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3+NH4Cl两个反应加合而成。
反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?
_______________。
表1相关物质的溶解度(20℃)(单位:
g)
NaCl
NH4HCO3
NaHCO3
NH4Cl
36.0
21.7
9.6
37.2
(4)操作2为洗涤、煅烧。
晶体应在以下装置______________中(填字母序号)进行“洗涤”操作。
在上述操作中,如何判断晶体已经洗涤干净______________。
(5)X的化学式为_____________,若X直接排放到空气中会造成的后果是_______________。
(6)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为______________,Y的化学式为______________,写出Y的一种用途_____________。
【答案】BCNaOH+HCl==NaCl+H2ONa2CO3+2HCl==2NaCl+H2O+CO2↑NaHCO3的溶解度较低,析出晶体B取最后一次洗涤液,滴加硝酸银溶液,若没有沉淀则已洗涤干净CO2温室效应氨气NH4Cl作氮肥
【解析】
(1)加入碳酸钠的作用有两个:
一个是除去溶液中的Ca2+、另一个是除去过量的氯化钡,所以加入的碳酸钠必须排在氯化钡的后面,所以顺序是NaOH、BaCl2、Na2CO3;
(2)加入盐酸的目的是除去过量的氢氧化钠和过量的碳酸钠,(3)由NaCl+NH4HCO3=NaHCO3+NH4Cl可知,碳酸氢钠和氯化铵的质量比为84:
53.5,碳酸氢钠生成的多,但是溶解度很小,20℃时的溶解度为9.6g,所以生成的碳酸氢钠大都以晶体存在,类似于沉淀,符合复分解反应的条件,所以反应能顺利进行;(4)为了能将洗涤的液体与固体及时分离,所以洗涤时应用装置B,如果洗涤干净则洗涤所得溶液中没有氯化铵,所以判断晶体已经洗涤干净的方法是:
取最后一次洗涤液,滴加硝酸银溶液,若没有沉淀则已洗涤干净;(5)碳酸氢钠在加热条件下分解生成碳酸钠和二氧化碳、水,所以X的化学式为CO2,直接排放会导致温室效应。
(6)滤液中最主要成分是氯化铵,氯化铵与Ca(OH)2反应的产物是氨气、氯化钙、水,氨气可用于循环使用,氯化铵的化学式为NH4Cl,因含氮元素,可做氮肥。
点睛:
本题容易出错的地方是对于循环物质的判断,在后面的生成物中的物质,如果在前面的反应物中用到过该物质就可以循环使用.
10.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
资料:
+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:
(1)发电厂是利用垃圾焚烧产生的___________转变为电能。
(2)垃圾焚烧产生的烟气中含有SO2、HCl等有害气体。
吸收步骤中,石灰浆的作用就是吸收这些有害气体,请你写出石灰浆吸收HCl的化学方程式_____
(3)溶解步骤中,产生的H2的化学方程式为①____________________除此外,溶解步骤还能发生两个反应:
②Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;③Fe+Fe2(SO4)3=3FeSO4,这三条化学方程式中反应前后铁元素的化合价不变的是______________(填序号)。
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、_____(填操作名称),过滤,得到硫酸亚铁晶体,其中氮气的作用是_________
(5)请你就城市生活垃圾处理提一条建议_____
【答案】化学能2HCl+Ca(OH)2=CaCl2+2H2OFe+H2SO4=FeSO4+H2↑②降温结晶保护气,防止+2价的铁元素被空气中的氧气氧化生活垃圾分类回收等
【解析】
(1)
(1)发电厂是利用垃圾焚烧产生的化学能转变为电能;
(2)石灰浆显碱性,能够吸收酸性气体,所以吸收步骤中,石灰浆的作用是除去烟气中含有的SO2、HCl等有害气体,氢氧化钙与盐酸反应生成氯化钙和水,化学反应方程式为:
2HCl+Ca(OH)2=CaCl2+2H2O;(3)溶解步骤中,硫酸与铁反应生成硫酸亚铁和氢气,铁锈与硫酸反应生成硫酸铁和水,所以产生的H2的化学方程式①为:
Fe+H2SO4═FeSO4+H2↑;②Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,反应前后铁元素的花合价不变;Fe+Fe2(SO4)3═3FeSO4,反应前后铁元素的化合价改变;(4)将所得硫酸亚铁溶液在氮气环境中得到硫酸亚铁铵晶体,基本操作步骤:
加热浓缩,然后冷却结晶;再过滤;最后洗涤干燥,得到硫酸亚铁晶体,其中氮气的作用是作保护气,避免+2价的铁元素被空气中的氧气氧化;(5)生活垃圾分类回收等是为生活垃圾处理提出的一条很好的建议。
11.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。
以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业。
从硼镁泥中提取MgSO4·7H2O的简要工业流程如下:
根据题意回答下列问题:
(1)实验中需要用98%的浓硫酸(p=1.84g/mL)来配制一定浓度的稀硫酸。
下列所给的仪器中,属于配制过程中必须使用的有_____________(填