硫酸钙+硫酸钙的硫酸钙+硫酸密度.docx
《硫酸钙+硫酸钙的硫酸钙+硫酸密度.docx》由会员分享,可在线阅读,更多相关《硫酸钙+硫酸钙的硫酸钙+硫酸密度.docx(11页珍藏版)》请在冰豆网上搜索。
硫酸钙+硫酸钙的硫酸钙+硫酸密度
氯化钙固体与稀硫酸反应时,可能因为氯化钙固体表面生成不溶于
水的硫酸钙而阻止了氯化钙与硫酸的继续作用,使反应不能继续进
行到底。
氯化钙与硫酸的反应式为:
CaCl2(固体)+H2SO4(稀硫酸)→CaSO4↓+2HCl
碳酸钠溶液与稀硫酸的反应可以进行到底:
Na2CO3(在溶液中)+H2SO4(稀硫酸)→Na2SO4+H2CO3
H2CO3(在稀硫酸溶液中)→H2O+CO2↑
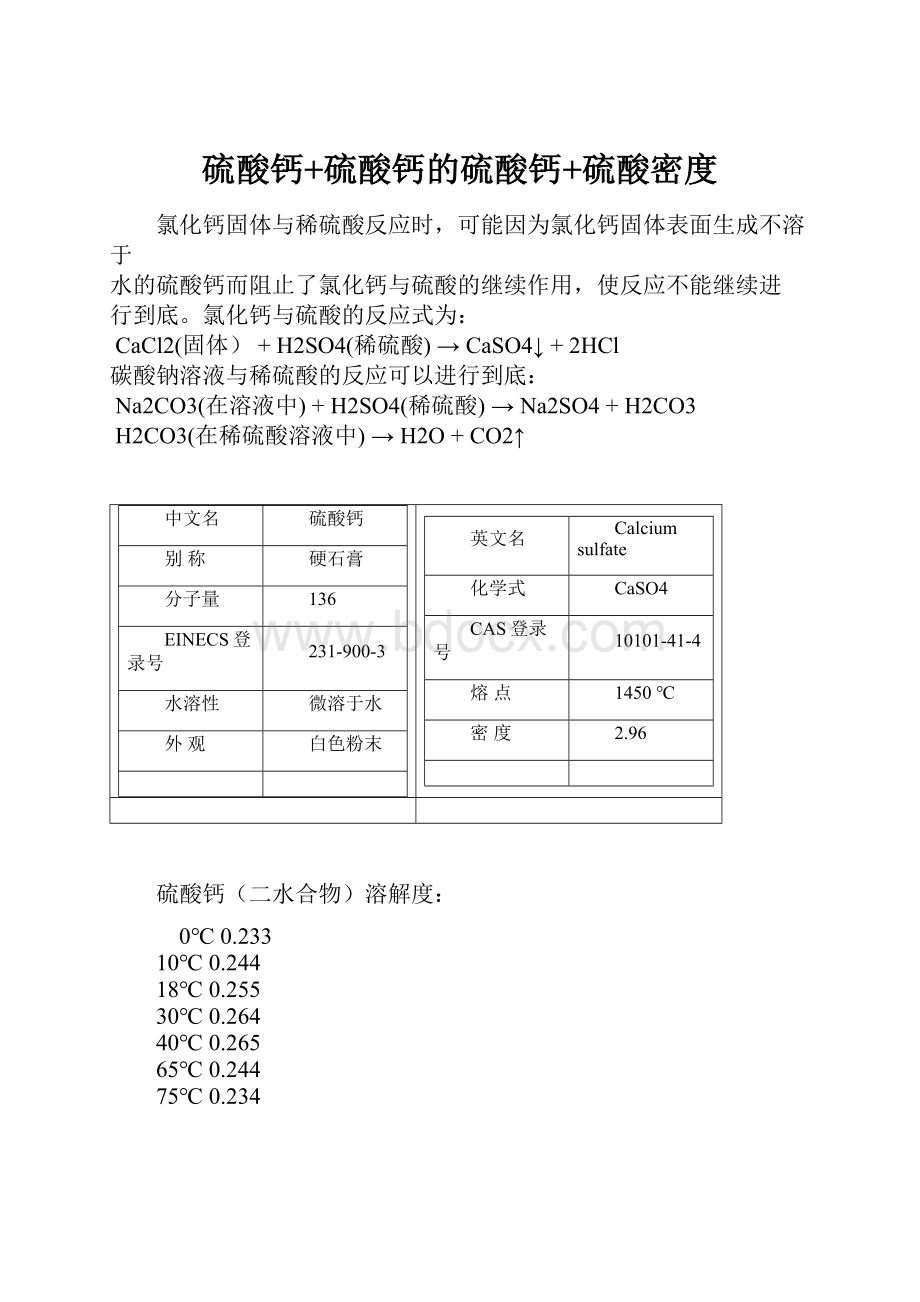
中文名
硫酸钙
别称
硬石膏
分子量
136
EINECS登录号
231-900-3
水溶性
微溶于水
外观
白色粉末
英文名
Calciumsulfate
化学式
CaSO4
CAS登录号
10101-41-4
熔点
1450℃
密度
2.96
硫酸钙(二水合物)溶解度:
0℃0.233
10℃0.244
18℃0.255
30℃0.264
40℃0.265
65℃0.244
75℃0.234
硫酸钙(CaSO4)无色正交或单斜晶体,单斜晶体熔点1450℃,1193℃正交转单斜晶体。
密度2.61克/立方厘米,微溶于水。
1200℃以上可以分解:
2CaSO4==1200℃==2CaO+2SO2↑+O2↑
一般由天然产出。
也是磷酸盐工业和某些其他工业的副产品。
2化学性质
高温下跟碳作用可生成硫化钙和二氧化碳。
生石膏CaS 硫酸钙O4·2H2O是 天然矿物,为白、浅黄、浅粉红至灰色的透明或半透明的板状或纤维状晶体。
性脆,128℃失1.5H2O,163℃失2H2O。
工业上将生石膏加热到150℃脱水成熟石膏CaSO4·0.5H2O(或烧石膏),加水又转化为CaSO4·2H2O。
据此可用于石膏绷带、制作石膏模型、粉笔、工艺品、建筑材料。
石膏还用为水泥调速剂以控制其硬化速度。
油漆腻子、纸张填料也用到石膏,日常点豆腐可用它为凝结剂。
农业上施用石膏以降低土壤的碱性。
石膏矿与煤炭于高温可制得SO2用于生产硫酸。
CaSO4溶解度不大,其溶解度呈特殊的先升高后降低状况。
如10℃溶解度为0.1928g/100g水(下同),40℃为0.2097,100℃降至0.1619,使溶解硫酸钙的硬水在高压锅炉(可达400℃)中结垢,造成危害,应于事前用Na2CO3使CaSO4转化为更难溶的CaCO3沉淀(其溶解度:
0.0015g)而除去(使 硬水软化)。
在大理石遇稀H2SO4时因生成微溶CaSO4包于大理石表面阻碍与酸的接触,使反应停止,故不能用稀H2SO4与大理石制取CO2。
化学方程式:
CaCO3+H2SO4===CaSO4(微溶于水)+H2O+CO2↑
初中化学:
由于其形式为某酸某,所以涉及到原子团,其根为硫酸根,所以为SO4其他常见的有硫酸根的还有硫酸亚铁,硫酸铜,硫酸钠等等
作用用途
氮肥生产分析微量一氧化碳和二氧化碳作吸湿剂、涂料、人造象牙、油漆、造纸、染料、印花、冶金、处理水。
作为食品添加剂和加工助剂,药物。
用作水泥原料;用作水泥阻滞剂;石膏
除大量用作建筑材料和水泥原料外,广泛用于橡胶、塑料、肥料、农药、油漆、纺织、食品、医药、造纸、日用化工、工艺美术、文教等部门。
在缺乏硫资源的地区,可用以制造硫酸和硫酸铵。
无色透明的石膏可作光学材料。
是制造水泥、半水硫酸钙及硫酸的原料。
油漆和造纸工业中用作填充剂。
农业上用作化肥,能降低土壤碱度、改善土壤性能。
还用作番茄、土豆罐头中的组织强化剂、酿造用水的硬化剂、酒的风味增强剂等。
建材、水泥生产用 [1] 可制作各种模型,医疗上用作石膏绷带。
此外,还可用于调节水泥的凝结时间,作油漆用的白色颜料、纸张的填料和抛光粉,也是一种常用的 干燥剂。
也用于冶金和农业等方面。
也有用作 面包改良剂。
检验
氯化物
取硫酸钙0.50g,加硝酸溶液(1→2)5ml与水40ml,振摇使溶解,依法检查(附录ⅧA),与标准氯化钠溶液9.0ml制成的对照溶液比较,不得更浓(0.018%)。
碳酸盐
取硫酸钙1.0g,加水5ml,混匀,滴加稀盐酸,不得发生暴沸。
炽灼失重取硫酸钙1.0g,炽灼至恒重,减失重量应为18.0%-23.0%。
铁盐
取硫酸钙0.20g,加 过硫酸按50mg与稀盐酸10ml,振摇溶解后,加水稀释使成50ml,加 硫氰酸铵试液5.0ml,摇匀,依法检查(附录ⅧG),与标准铁溶液3.0ml用同一方法制成的对照液比较,不得更深(0.015%)。
重金属
取硫酸钙1.0g,加稀盐酸5ml与水15ml,加热溶解,放冷,加酚酞指示液1滴,滴加浓氨溶液至溶液显淡红色,加醋酸盐缓冲液(pH3.5)2ml,滤过,滤液加水至25ml,加维生素C0.5g,溶解后,依法检查(附录ⅧH第一法),含重金属不得过百万分之十五。
测定含量
方法名称:
硫酸钙---硫酸钙的测定---络合滴定法
应用范围:
本方法采用滴定法测定硫酸钙的含量。
本方法适用于硫酸钙。
方法原理:
供试品加稀盐酸10mL与水100mL,振摇使溶解,在搅拌下精密加乙二胺四醋酸二钠滴定液(0.05mol/L)20mL,摇匀,加氢氧化钠溶液(1→5)15mL与紫脲酸铵指示剂0.2~0.3g,继以乙二胺四醋酸二钠滴定液(0.05mol/L)滴定至溶液由桃红色变为紫色,计算硫酸钙的含量。
试剂:
1.稀盐酸
2.紫脲酸铵指示剂
3.乙二胺四醋酸二钠滴定液(0.05mol/L)
4.基准氧化锌
5.水
6.氢氧化钠溶液(1→5)
7.锌滴定液(0.05mol/L)
试样制备:
1.稀盐酸
取盐酸234mL加水稀释至1000mL。
2.紫脲酸铵指示剂
取紫脲酸铵0.1g,加氯化钠使成20g,研细。
3.乙二胺四乙酸二钠滴定液(0.05mol/L)
取乙二胺四醋酸二钠19g,加适量的水使溶解成1000mL,摇匀。
标定:
取于约800℃灼烧至恒重的基准氧化锌0.12g,精密称定,加稀盐酸3mL使溶解,加水25mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL与氨-氯化铵缓冲液(pH10.0)10mL,再加铬黑T指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
每1mL乙二胺四乙酸二钠滴定液(0.05mol/L)相当于4.069mg的氧化锌。
根据本液的消耗量与氧化锌的取用量,算出本液的浓度。
贮藏:
置玻璃塞瓶中,避免与橡皮塞、橡皮管等接触。
4.锌滴定液(0.05mol/L)
配制:
取硫酸锌15g(相当于锌约3.3g)加稀盐酸10mL与水适量是溶解成1000mL,摇匀。
标定:
精密量取本液25mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL,氨-氯化铵缓冲液(pH10.0)与铬黑T指示剂少量,用乙二胺四乙酸二钠滴定液(0.05mol/L)滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
根据乙二胺四乙酸二钠滴定液的消耗量,计算出本液的浓度,即得。
操作步骤:
取本品0.2g,精密称定,加稀盐酸10mL与水100mL,振摇使溶解,在搅拌下精密加乙二胺四乙酸二钠滴定液每1mL乙二胺四乙酸二钠滴定液(0.05mol/L)相当于6.807mg的CaSO4。
注:
“精密称取”系指称取重量应准确至所称取重量的千分之一。
[2]
质检指标值
铵(NH4),%≤0.005
澄清度试验/号≤4
碱金属及镁(MgO),%≤0.2
盐酸不溶物,%≤0.025
重金属(以Pb计),%≤0.001
铁(Fe),%≤0.0005
碳酸盐(CO3),%≤0.05
氯化物(Cl),%≤0.002
硝酸盐(NO3),%≤0.002
含量(CaSO4·2H2O),%≥99.0
鉴别
加稀盐酸使溶解,溶液是钙盐与硫酸盐(附录Ⅲ)的鉴别反应。
配伍禁忌
有水分存在时,钠盐可能与有机胺、氨基酸、多肽和蛋白质有配伍禁忌,并可能形成复合物。
钙盐将影响四环素类抗生素的生物利用度,据推测,硫酸钙可能与 吲哚美辛、阿司匹林、门冬酰胺、 头孢氨苄、 红霉素有配伍禁忌,因为这些物质与其他钙盐有配伍禁忌。
高温状态下,硫酸钙可与磷或铝粉末发生剧烈反应,也能与 重氮甲烷发生剧烈反应。
[3]
化学实验
在使用碳酸钙制取二氧化碳的实验中,不能用稀硫酸代替稀盐酸是因为反应会生成微溶的硫酸钙,没有溶解的硫酸钙包裹在石灰石表面,使反应停止。
参考资料:
1.
硫酸钙的用途
2.
中华人民共和国药典,国家药典委员会编,化学工业出版社,2005年版,二部,p913。
3.
硫酸钙(二水合物)溶解度:
0℃0.233
10℃0.244
18℃0.255
30℃0.264
40℃0.265
65℃0.244
75℃0.234
硫酸钙本来就是微溶于水的.
硫酸特性:
产生一部分硫酸合氢离子H3SO4+,正是这一部分硫酸合质子,导致纯硫酸具有非常强的酸性,虽然少,但是酸性却要比水合质子强得多,所以纯硫酸的哈米特酸度函数高达-12.0。
在硫酸溶剂体系中,H3SO4+经常起酸的作用,能质子化很多物质产生离子型化合物:
NaCl+H2SO4==NaHSO4+HCl(不加热都能很快反应)
KNO3+H2SO4→K++HSO4-+HNO3
HNO3+H2SO4→NO2++H3O++2HSO4-
CH3COOH+H2SO4→CH3C(OH)2++HSO4-
HSO3F+H2SO4→H3SO4++SO3F-( 氟磺酸酸性更强)
上述与HNO3的反应所产生的NO2+,有助于 芳香烃的硝化反应。
浓硫酸特性
1.脱水性
脱水指浓硫酸脱去非游离态水分子或按照水的氢氧原子组成比脱去有机物中氢氧元素的过程。
就硫酸而言,脱水性是浓硫酸的性质,而非稀硫酸的性质,浓硫酸有脱水性且脱水性很强,脱水时按水的组成比脱去。
物质被浓硫酸脱水的过程是化学变化,反应时,浓硫酸按水分子中氢氧原数的比(2:
1)夺取被脱水物中的氢原子和氧原子或脱去非游离态的结晶水,如 五水硫酸铜(CuSO4·5H2O)。
硫酸可被浓硫酸脱水的物质一般为含氢、氧元素的有机物,其中蔗糖、木屑、纸屑和棉花等物质中的有机物,被脱水后生成了黑色的炭,这种过程称作炭化。
一个典型的炭化现象是蔗糖的黑面包反应。
在200mL烧杯中放入20g蔗糖,加入几滴水,水加适量,搅拌均匀。
然后再加入15mL质量分数为98%的浓硫酸,迅速搅拌。
观察实验现象。
可以看到蔗糖逐渐变黑,体积膨胀,形成疏松多孔的海绵状的炭,反应放热,还能闻到刺激性气体。
C12H22O11==浓硫酸==12C+11H2O
同时进行碳与浓硫酸反应:
C+2H2SO4(浓)==加热==CO2↑+2SO2↑+2H2O
2.强氧化性
(1)与金属反应
①常温下浓硫酸能使铁、铝等金属钝化。
②加热时,浓硫酸可以与除金、铂之外的所有金属反应,生成高价金属硫酸盐,本身一般被还原成二氧化硫。
Cu+2H2SO4(浓)==加热==CuSO4+SO2↑+2H2O
2Fe+6H2SO4(浓)==加热==Fe2(SO4)3+3SO2↑+6H2O
在上述反应中,硫酸表现出了强氧化性和酸性。
(2)与非金属反应
热的浓硫酸可将碳、硫、磷等非金属单质氧化到其高价态的氧化物或 含氧酸,本身被还原为二氧化硫。
在这类反应中,浓硫酸只表现出氧化性。
C+2H2SO4(浓)=加热=CO2↑+2SO2↑+2H2O
S+H2SO4(浓)==加热==3SO2↑+2H2O硫酸
2P+5H2SO4(浓)==加热==2H3PO4+5SO2↑+2H2O
(3)与其他还原性物质反应
浓硫酸具有强氧化性,实验室制取 硫化氢、 溴化氢、 碘化氢等还原性气体不能选用浓硫酸。
H2S+H2SO4(浓)==S↓+SO2↑+2H2O
2HBr+H2SO4(浓)==Br2↑+SO2↑+2H2O
2HI+H2SO4(浓)==I2↓+SO2↑+2H2O
稀硫酸特性
性质
1.可与多数金属(比铜活泼)和绝大多数金属氧化物反应,生成相应的硫酸盐和水;
2.可与所含酸根离子对应酸酸性比硫酸根离子弱的盐反应,生成相应的硫酸盐和弱酸;
3.可与碱反应生成相应的硫酸盐和水;
4.可与氢前金属在一定条件下反应,生成相应的硫酸盐和氢气;
5.加热条件下可催化蛋白质、二糖和多糖的水解;
6.能与指示剂作用,使紫色石蕊试液变红,使无色酚酞试液不变色。
检验
所需药品:
经过盐酸酸化的 氯化钡溶液,镁粉。
检验方法:
使用经过盐酸(HCl)酸化的的氯化钡(BaCl2)。
向待测物溶液滴入几滴经过盐酸酸化的氯化钡溶液,震荡,如果产生白色沉淀;向溶液中加入镁粉后生成可燃性气体,则待测溶液中含有硫酸。
但此方法仅限中学阶段。
常见误区
稀硫酸在中学阶段,一般当成H2SO4=2H++SO42-,两次完全电离,其实不是这样的。
根据硫酸酸度系数p K a1=-3.00,p K a2=1.99,其二级电离不够充分,在稀硫酸中HSO4-=可逆=H++SO42-,并未完全电离,1mol/L的硫酸一级电离完全,二级电离约电离10%,也就是溶液中仍存在大量的HSO4-。
而即使是NaHSO4溶液0.1mol/L时,硫酸氢根也只电离了约30%。
硫酸密度:
10%的硫酸密度1.066g/cm3
20%的硫酸密度1.139g/cm3
30%的硫酸密度1.218g/cm3
40%的硫酸密度1.303g/cm3
50%de硫酸密度1.395g/cm3
60%的硫酸密度1.498g/cm3
70%的硫酸密度1.611g/cm3
80%的硫酸密度1.727g/cm3
90%的硫酸密度1.814g/cm3
98%的硫酸密度1.836g/cm3
密度 H2SO4 密度H2SO4 密度 H2SO4 密度 H2SO4
g/cm3 % g/cm3 % g/cm3 % g/cm3 %
1.000 0.3 1.115 16.7 1.230 31.4 1.345 44.7
1.005 1.0 1.120 17.4 1.235 32.0 1.350 45.3
1.010 1.7 1.125 18.1 1.240 32.6 1.355 45.8
1.015 2.5 1.130 18.8 1.245 33.2 1.360 46.3
1.020 3.2 1.135 19.4 1.250 33.8 1.365 46.9
1.025 4.0 1.140 20.1 1.255 34.4 1.370 47.4
1.030 4.7 1.145 20.7 1.260 35.0 1.375 47.9
1.035 5.5 1.150 21.4 1.265 35.6 1.380 48.4
1.040 6.2 1.155 22.0 1.270 36.2 1.385 49.0
1.045 7.0 1.160 22.7 1.275 36.8 1.390 49.5
1.050 7.7 1.165 23.3 1.280 37.4 1.395 50.0
1.055 8.4 1.170 23.9 1.285 37.9 1.400 50.5
1.060 9.1 1.175 24.6 1.290 38.5 1.405 51.0
1.065 9.8 1.180 25.2 1.295 39.1 1.410 51.5
1.070 10.6 1.185 25.8 1.300 39.7 1.415 52.0
1.075 11.3 1.190 26.5 1.305 40.2 1.420 52.5
1.080 12.0 1.195 27.1 1.310 40.8 1.425 53.0
1.085 12.7 1.200 27.7 1.315 41.4 1.430 53.5
1.090 13.4 1.205 28.3 1.320 41.9 1.435 54.0
1.095 14.0 1.210 28.9 1.325 42.5 1.440 54.5
1.100 14.7 1.215 29.6 1.330 43.1 1.445 55.0
1.105 15.4 1.220 30.2 1.335 43.6 1.450 55.4
1.110 16.1 1.225 30.8 1.340 44.2 1.455 55.9
1.460 56.4 1.585 67.8 1.710 78.5 1.835 95.7
1.465 56.9 1.590 68.2 1.715 78.9 1.836 97.0
1.470 57.4 1.595 68.7 1.720 79.4
1.475 57.8 1.600 69.1 1.725 79.8
密度 H2SO4 密度H2SO4 密度 H2SO4
g/cm3 % g/cm3 % g/cm3 %
1.480 58.3 1.605 69.5 1.730 80.2
1.485 58.8 1.610 70.0 1.735 80.7
1.490 59.2 1.615 70.4 1.740 81.2
1.495 59.7 1.620 70.8 1.745 81.6
1.500 60.2 1.625 71.2 1.750 82.1
1.505 60.6 1.630 71.7 1.755 82.6
1.510 61.1 1.635 72.1 1.760 83.1
1.515 61.5 1.640 72.5 1.765 83.6
1.520 62.0 1.645 72.9 1.770 84.1
1.525 62.4 1.650 73.4 1.775 84.6
1.530 62.9 1.655 73.8 1.780 85.2
1.535 63.4 1.660 74.2 1.785 85.7
1.540 63.8 1.665 74.6 1.790 86.3
1.545 64.3 1.670 75.1 1.795 87.0
1.550 64.7 1.675 75.5 1.800 87.7
1.555 65.1 1.680 75.9 1.805 88.4
1.560 65.6 1.685 76.3 1.810 89.2
1.565 66.0 1.690 76.8 1.815 90.1
1.570 66.5 1.695 77.2 1.820 91.1
1.575 66.9 1.700 77.6 1.825 92.2
阅读(4436)| 评论
(2)