八下科学易错题.docx
《八下科学易错题.docx》由会员分享,可在线阅读,更多相关《八下科学易错题.docx(18页珍藏版)》请在冰豆网上搜索。
八下科学易错题
取稀硫酸质量(g)60.090.0120.0150.0180.0
1.由于大量使用一次性塑料袋而造成的“白色污染”已成为严重的社会问
产生气体质量(g)00.10.3m0.6
题。
某化学研究小组同学对某种塑料袋的组成进行分析研究(资料显示
该塑料只含C、H两种元素)。
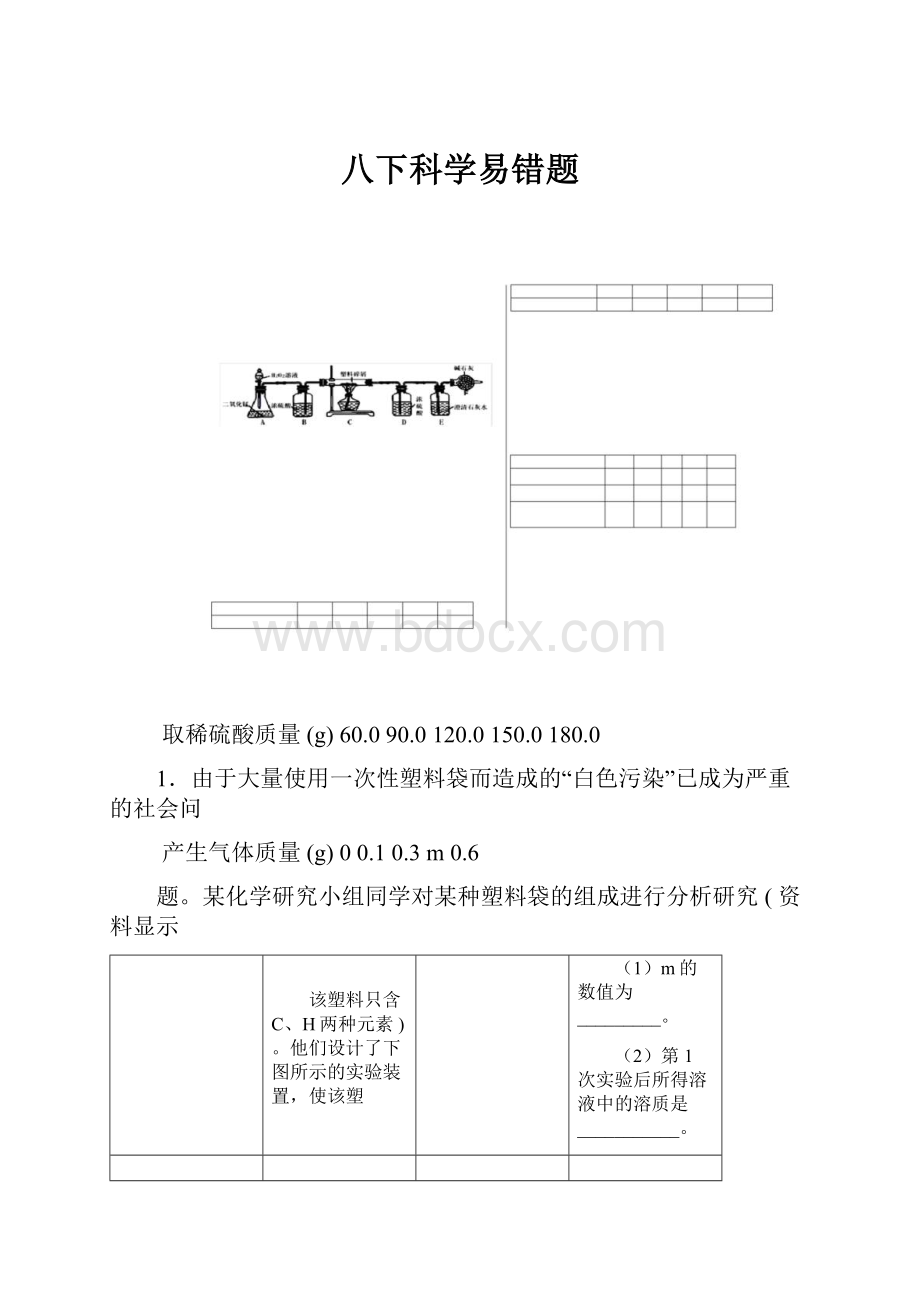
他们设计了下图所示的实验装置,使该塑
(1)m的数值为_________。
(2)第1次实验后所得溶液中的溶质是___________。
料样品在纯氧中完全燃烧,观察实验现象、分析有关数据、推算元素含
(3)列式计算该样品中变质铁的质量分数是多少?
(保留至0.1%)
量。
(4)硫酸溶液的质量分数是多少?
3、珍珠是绍兴地区的特产之一。
珍珠的主要成分是什么呢?
某探究小组为
此展开了研究。
查阅资料发现,珍珠的主要成分是碳酸钙。
为了测定珍珠
中碳酸钙的含量,他们从市场上购买了100克珍珠并将其磨成粉,分成五
等份后,分别放入5只烧杯中。
然后向烧杯中分别加入不同质量的同种盐
(1)实验装置中有一处明显错误,请指出错误处,并写出改正方法。
酸,测得实验数据如下表所示(假设珍珠粉中其他成分既不溶于水,也不
参与反应)。
(2)装置B的作用是。
烧杯编号12345
(3)若装置C的玻璃管中放入的塑料试样质量为5.6g,塑料试样充分
加入样品的质量/克2020202020
燃烧后,装置D增重7.2g,则该塑料试样中碳元素与氢元素的原子
加入稀盐酸的质量/克1020304050
个数比为(假设该塑料只含C、H两种元素)。
充分反应后生成气体1.763.52X7.047.92
(4)若装置中没有连接装置E,将使该塑料试样中碳元素的质量测算
结果(填“偏小”、“偏大”或“无影响”)。
2.铁的锈蚀对社会生产造成较大损害,但也有有利的一面,如某些食品包
装袋内常放入还原性铁粉作“双吸剂”以防止食品腐败。
某课外兴趣小组
在实验室发现了一包破损的还原性铁粉(含少量杂质,杂质既不溶于水也
的质量/克
(1)表中X的值为。
(2)加入的稀盐酸的溶质质量分数是多少?
(3)珍珠粉样品中碳酸钙的质量分数是多少?
(4)第5号烧杯中溶液的质量分数是多少?
不溶于酸),他们取六份样品,分别加稀硫酸反应,测得部分数据如下,
请根据有关信息回答问题。
(相对原子质量Fe-56H-1S-32O-16)
4、为测定石灰石样品的纯度(样品中的杂质既不溶于水也不与盐酸反应,
实验次数12345
且耐高温).取10g该石灰石样品,再把100g盐酸平均分4次加入样品取样品质量(g)31.031.031.031.031.0
-1-
中,充分反应后剩余固体的质量见下表:
(1)①由Ⅰ可知原混合气体中肯定不含_______;②由Ⅱ可以得出的结论
是_____;
(2)最终收集到的气体是________;
(3)为了确定该混合气体的最终组成,还需补充的实验或改进的操作是___。
求:
(1)石灰石样品的纯度;
7.为了准确测定校舍建筑工地上石料中碳酸钙的质量分数,该校某化学兴
(2)所用盐酸的质量分数;
(3)100g这种纯度的石灰石跟一定量的盐酸恰好完全反应后,溶液中溶
趣小组先将石料粉碎,然后称取4份,分别逐渐加入到4份稀盐酸中(石
质的质量分数.
料中的杂质不参与反应),待反应停止后,所测数据记录如下表:
高温
5.碳酸钙在高温条件下发生如下反应:
CaCO3CaO+CO2
。
将100g
分析表中数据,回答下列问题:
(1)先将石料粉碎的目的:
含CaCO3质量分数为80%的石灰石样品(杂质不发生反应,也不含钙元
(2)表中有一次测定的数据有明显的错误,这次数据的编号是______.
素),高温煅烧一段时间后,冷却,测得剩余固体中含钙元素的质量
(3)25.0g石料恰好完全反应时,消耗稀盐酸的质量是______g.
分数为41%,则生成的CaO质量约为g。
(4)计算该石料中碳酸钙的质量分数.
6.某无色气体中可能含有一氧化碳、二氧化碳、氢气、氮气中的一种或几
编号项目1234
种,现将该气体依次通过如图所示装置,观察到:
Ⅰ:
A装置内未见浑浊
出现;Ⅱ:
D装置内无水硫酸铜变蓝;Ⅲ:
E装置未出现明显现象;最终收
石料质量/g25.025.050.050.0
稀盐酸质量/g120.0150.0250.0100.0
集到一定量干燥气体(假设每步反应都是完全)
CO2气体质量/g8.88.818.88.8
8.取4.4g部分被氧化的镁带样品,加入到147g溶质的质量分数为10%的
H2SO4溶液中,镁带和H2SO4均恰好完成反应。
(镁和硫酸生成硫酸镁和氢气,
氧化镁和硫酸反应生成硫酸镁和水)
(1)写出上述镁带在H2SO4溶液中发生反应的化学方程式:
(2)反应完成后生成MgSO4的质量为g。
请回答下列问题:
9.镁易被空气中的氧气氧化成氧化镁。
现有一卷标签上标明120克的镁带,
-2-
称其质量为136克(假设镁除被氧化外,没有发生其他任何变化,且氧
学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正
化是均匀的)。
试计算:
确的是()【来源:
21·世纪·教育·网】
物质MNQP
(1)被氧化的镁的质量是多少克?
反应前质量(g)181232
(2)称取上述变质的镁带6.8克加入到足量的盐酸中,反应产生氢气的质
量是多少克?
反应后质量(g)X26212
A.该变化的基本反应类型是化合反应B.反应后物质M的质量为l3g
10.环形导线(可看作通电螺线管的一匝)能产生
磁场,其磁感线分布如右图所示,则点(选填“A”
或“B”)的磁场较弱。
若将一小磁针放在环形导
线的右侧,小磁针的极将向导线靠近。
C.反应中N、P的质量比为13:
6D.物质Q可能是该反应的催化剂
12.一定条件下,3.9g苯(C6H6)与9.6gO2恰好完全反应,生成6.6gCO2、
2.7gH2O和物质X,则X的质量为,X的化学式为;O2与X
的化学计量数之比为。
13.如图是水位自动报警器示意图:
3.习小组欲测定石灰石中碳酸钙
的质量分数,采用的方法如下:
取
该石灰石样品20g,把80g稀盐酸
实验次数
加入稀盐酸
的质量/g
剩余固体
的质量/g
(1)A、B都是碳棒,在水位由
甲位置升到乙位置的过程中,
碳棒B受的浮力将(填“变大”、
分四次加入,实验过程所得数据如12015
“变小”或“不变”)。
右表(已知石灰石样品中含有的二22010
(2)水库中的水是导体,当水位
氧化硅等杂质不溶于水,不与稀盐3206.8
到达(填“甲”或“乙”)位置时,
酸反应)。
根据实验数据计算:
420n
“控制电路”接通,此时“工作电路”中的红灯会发光报警。
而当“控制电路”
(1)表中n的数值为。
断开时,只有绿灯会发光。
请用笔划代替导线将“工作电路”连接起来。
(2)样品中碳酸钙的质量分数是。
(3)如图所示三种设备,工作原理有一个与水位自动报警器明显不同,这个
(3)求盐酸中溶质的质量分数。
设备是。
(3)求第4次反应后溶液中生成溶质的质量分数和剩余物的质量分数。
14.按
11.在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化
-3-
下图所示置做实验时,可看到的现象是:
B瓶中的试液变红色;F瓶的溶液若B的质量增加2.2g,则A的质量增加g.
变浑浊;E管的粉末变红色;G处放出的气体可燃烧,据此,请写出A、B、17.超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在
C、D、E、F、G各处发生反应的化学方程式.
潜水艇中用它作制氧剂,供人们呼吸之用,它与二氧化碳反应的化学方程
式为:
4KO2+2CO2═2K2CO3+3O2,某学生为了验证这一实验,以大理石,足量
A处;B处;
的盐酸和超氧化钾为原料制取O2,设计如下实验装置:
C处;D处;
E处;F处;
G处.
(1)A是制取CO2的装置,应从图1~3中选择.C装置内可能出现
的现象是.为了检验E中收集到的气体,可以在取出集气瓶后,
15.下图是测定植物某一生命活动过程的
用,现象是.
装置.A瓶中的氢氧化钠溶液的作用
(2)若E中的石灰水出现少量的白色沉淀,这是因为.
是,B瓶中的石灰水的作用(3)表明D中的超氧化钾样品接近反应完毕时的现象是.
是,D瓶中出现的现象18.有一乡村中学由于条件限制,仅有一大一小两种试管和稀硫酸。
甲、
是.此实验说明植物具有.乙两个学生找来铝制废牙膏皮,各自设计了一种装置,制取并收集一试管
16.为了确定CH4、H2和CO(简称试验
氢气。
气)三种可燃性气体,可分别让他们在氧气中燃烧,
(1)哪个学生设计的装置比较合理?
(填“甲”或
(1)装置A中的液体是,装置B中的液体是.
“乙”)。
另一设计的装置不合理的原因是:
。
(2)若装置A的质量增加,B的质量不变,则试验气是;燃烧的
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的
化学方程式为.试管,应该采取的措施是:
。
(3)若装置A的质量不变,B的质量增加,则试验气(3)日常生活中还可以用哪些物品来代替牙膏皮和稀硫酸
是,B瓶中的反应方程式是.
完成实验?
。
(4)若装置A、B的质量都增加,则试验气是,19.“化学多米诺实验”是
-4-
利用化学反应中气体产生的压力,使多个化学反应依次发生.(整个反应滴加入溶液至过量
只需要第一个反应发生,就好像多米诺骨牌游戏一样.)以下就是一个“化
学多米诺实验”,已知H2O2在MnO2的催化作用下可分解产生O2和H2O.所示
装置图中各仪器内盛放的物质分别为:
A.稀硫酸;B.锌粒;C.3%H2O2溶液;
D.MnO2;E.某溶液;F.某块状固体;G.滴有紫色石蕊试液的蒸馏水;H.足
量澄清石灰水.请回答以下各题:
(1)实验开始前必须进行的操作是;
(2)反应开始后,若G中出现红色,H中有白色沉淀生成,判断E、F中
的物质可能分别是;;
(3)按基本反应类型写出该实验中有关反应的化学方程式:
(用字母表示)
化合反应,发生在装置中;
分解反应,发生在装置中;
置换反应,发生在装置中;
复分解反应,发生在装置
9.小强同学用氢氧化钙和盐酸进行酸碱中和反应的实验时,向烧杯中的
氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂,因此,
他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究.请
你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【猜想】猜想一:
溶质只有氯化钙.猜想二:
溶质中有CaCl2和Ca(OH)2.
猜想三:
溶液中有.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
方案方法步骤实验现象实验结论
方案一
取少量烧杯内的溶液于试管中,滴
入几滴无色酚酞溶液
酚酞不变色猜想一正确
酚酞变红色猜想二正确
方案二取少量烧杯内的溶液于试管中,逐猜想三正确
【方案反思】方案一不能证明猜想一正确的理由是.
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯
化钙,你认为应该进行的实验步骤是.
【结论】在分析化学反应后所得物质的成分时,除考虑生成物外还需考
虑.
10.化学兴趣小组利用如装置
验证CO2能与NaOH反应。
(装
置气密性良好)
(1)关闭K2,打开K1、K3,当
D中出现的现象时,可确
定C中充满CO2。
(2)C中充满CO2后,关闭K1,打开K2,将注射器中5mL浓NaOH溶液推入
C中,观察到D中液体流入C中,说明CO2与NaOH发生反应,C中反应
的化学方程式是。
此过程中,C中压强的变化过程是。
(3)小组同
学发现此实验有不足,请你指出一处,写出改进方案。
11.化学兴趣小组的同学取10g某锌样品(含少量杂质,且杂质不溶于水,
也不与酸反应)于烧杯中,向其中加入一定量的稀硫酸,当加入稀硫酸
的质量为93.7g时,恰好完全反应,生成气体的质量与反应时间的关系
如下图所示,试回答下列问题:
稀硫酸的质量分数为多
少?
反应后,所得溶液中硫酸锌的质量分数为多少?
12.某同学对一瓶没有塞橡皮塞的氢氧化钠溶液开展了以
下探究:
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
-5-
(2)与CuCl2反应所消耗NaOH溶液的质量为克;实验操作实验现象实验结论
(3)计算氢氧化钠溶液中溶质的质量分数。
取少量该溶液于试管中,向溶液氢氧化钠溶液一定
25.某同学用一定质量分数的稀硫酸做“氧化铜+硫酸→硫酸铜+水”的实
中滴加溶液,并不断振荡。
变质了。
验,其五次实验结果如下表所示:
根据实验结果填写下列空格:
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
实验次数氧化铜/克硫酸溶液/克硫酸铜/克
[猜想]猜想1:
氢氧化钠溶液部分变质.猜想2:
氢氧化钠溶液全部变质。
12.01204.0
[查阅资料]
(1)氯化钙溶液呈中性。
24.01208.0
(2)氯化钙溶液能与碳酸钠溶液反应:
CaCl2+Na2CO3=CaCO3↓+2NaCl
36.01209.6
48.020016.0
510.0200X
[实验探究2]
实验步骤实验现象实验结论
(1)取少量该溶液于试管中,
有生成。
说明原溶液中一定有碳
(1)哪几次反应氧化铜有剩余?
。
向溶液中滴加过量的氯化钙溶酸钠。
液,并不断振荡。
(2)哪几次反应硫酸有剩余?
。
(2)取步骤
(1)试管中的少量
溶液变红
说明原溶液中一定有。
上层清液,滴加酚酞溶液。
色。
[实验结论]该氢氧化钠溶液(填“部分”或“全部”)变质。
[反思与评价]
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式。
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,
(3)表中X的值是。
(4)硫酸溶液中溶质的质量分数为。
26.如图所示,两根平行放置的长直导线a和b通有大小相同、方向相同
的电流,a受到的磁场力大小是F1,当加入一与导线所在平面垂直的匀强
磁场后,a受到的磁场力大小变为F2,则此时b受到的磁场力大小可能变
为。
你认为该方案填“可行”或“不可行”)。
说明理由。
[理解与应用]氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保
存的药品还有很多,试另举一例:
。
【
24.将NaOH溶液逐滴滴入HCl和CuCl2的混合溶液中,并根据观察到的现
象绘制了如图曲线,根据图示回答问题:
(1)氢氧化钠先与混合溶液中的反应(写化
学式);
-6-
()
-7-