九年级化学计算题练习题汇总.docx
《九年级化学计算题练习题汇总.docx》由会员分享,可在线阅读,更多相关《九年级化学计算题练习题汇总.docx(19页珍藏版)》请在冰豆网上搜索。
九年级化学计算题练习题汇总
焦岱初中
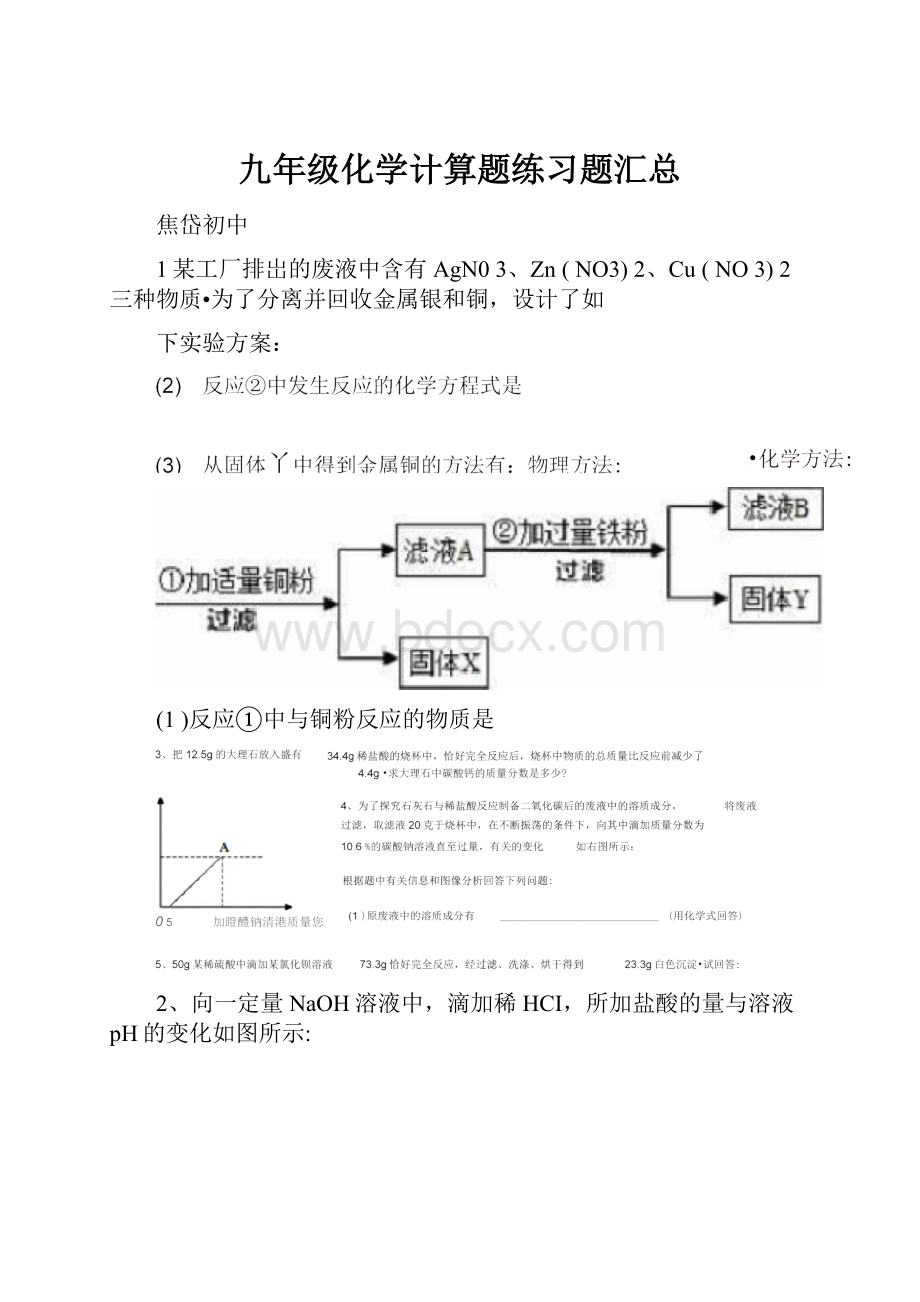
1某工厂排岀的废液中含有AgN03、Zn(NO3)2、Cu(NO3)2三种物质•为了分离并回收金属银和铜,设计了如
下实验方案:
(1)反应①中与铜粉反应的物质是
2、向一定量NaOH溶液中,滴加稀HCI,所加盐酸的量与溶液pH的变化如图所示:
⑴当加入稀HCI的体积为ml时,稀HCI与NaOH溶液恰好完全反应;
⑵向上述加了12ml稀盐酸后的NaOH溶液滴加紫色石蕊试液,溶液显色;
⑶当加入8mL稀盐酸后,溶液中的溶质有
(2)A点处溶液中溶质的质量?
(通过计算回答)
(1)在过滤操作中需要的玻璃仪器有;
(2)反应后所得溶液中溶质的质量分数.
6、现有氯酸钾和二氧化锰的混合物共26.5g,待反应不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g
求:
⑴制取氧气的质量;⑵剩余固体中含有的物质各为多少g?
(1)完全反应后生成H2的质量为
駅■*
/
■
(
1
反应时间S
g;
7、将一定质量的金属锌投入到100g稀硫酸中恰好完全反应,放岀气体的质量与反应时间的关系如图所示•试求:
(2)所用硫酸溶液中溶质的质量分数.
8、10g氯酸钾与二氧化锰的混合物加热,完全反应后,质量减少3.2g,则原混合物中二氧化锰的质量是多少?
9、实验用2.45g的氯酸钾和0.2g的二氧化锰最多可制取多少克的氧气?
10、实验室用含杂质的锌与稀盐酸反应制取氢气,取8g含杂质的锌粒于烧杯中(所含杂质不溶于水,也不与酸反应),
向其中加入74.2g稀硫酸,恰好完全反应后烧杯内剩余物质的质量为82g。
计算:
⑴杂质的质量g。
(2)反应后所得溶液的溶质质量分数(请写岀计算过程)。
11、实验室有一瓶久置且瓶盖破损的氢氧化钠固体,现取该固体10g,加入50g一定质量分数的盐酸至完全反应后,
称得剩余溶液质量为58.9g,求变质后生成物质的质量分数.
12、硫酸铜溶液可以作过氧化氢分解的催化剂•现取一定溶质质量分数的过氧化氢溶液68g倒入锥形瓶中,向其中
加入11.6g硫酸铜溶液,使过氧化氢完全分解,得到78g硫酸铜溶液.
求:
(1)产生氧气的质量.
(2)所用过氧化氢溶液的溶质质量分数.
13、向盛有26.4g硫酸钠和碳酸钠混合物的烧杯中加入218g稀硫酸,恰好完全反应,固体全部消失,烧杯内物质总
质量减少了4.4g.(化学反应方程式为NaCO+fSQ—NmSO+fO+COf),请计算:
(1)原混合物中碳酸钠的质量.
(2)反应后所得溶液中溶质的质量分数.
14、某补钙剂说明书的部分信息如右下图所示。
现将有20片该药剂制成的粉末与40g盐酸混合(其他成分不与盐酸
反应),恰好完全反应后称得剩余物的质量为55.6g。
(1)
"XX"牌钙片有效成分:
CaCO3
#-S:
I00g
ioo
青少年缺钙出现的疾病是。
(2)该品牌补钙剂每片含的CaCQ质量为多少?
(3)该盐酸中溶质的质量分数是多少?
(精确到0.1%)。
15、某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如
图所示,A点时,过滤,得到滤液242g,计算:
(1)反应生成沉淀的质量m为g.
(2)滤液中溶质的质量分数.
16、实验室常用石灰石和稀盐酸制取二氧化碳,现取含碳酸钙80%勺石灰石12.5g和94.4g稀盐酸恰好完全反应(石灰石中的杂质不溶于水,也不与稀盐酸反应)。
求:
(1)生成二氧化碳的质量;
(2)恰好完全反应后所得溶液中溶质的质量分数。
17、称取5.8g某生铁样品放入94.6g稀盐酸中,恰好完全反应(生铁样品中的杂质不溶于水也不
与盐酸发生反应),产生0.2g氢气。
试计算反应后所得溶液中溶质的质量分数。
18、某纯碱样品中含有少量氯化钠。
现称取该样品12g,完全溶于60g水中,加入63.4g稀盐酸,恰好完全反应,
最后称得烧杯中溶液的质量为131g。
九年级化学计算题练习题汇总
计算:
(1)完全反应后生成CO的质量;
(2)反应后所得溶液的溶质质量分数。
19、某氢氧化钙粉末中含有碳酸钙杂质•现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加
稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示.
(1)生成二氧化碳的质量是g;
(2)加入60g稀盐酸后所得溶液中含有的溶质是、(填化学式);
(3)计算样品中碳酸钙的质量分数(写岀计算过程,结果精确到0.1%).
20、某同学测定一瓶标签残缺的硫酸镁溶液的溶质质量分数,取30g该溶液,向其中逐滴加入溶质质量分数为10%勺
氢氧化钠溶液.生成沉淀的质量与所用氢氧化钠溶液的质量关系如图所示.反应方程式为:
MgSO+2NaOH=NSQ+Mg(OH
2J
(1)配制100g溶质质量分数为10%勺NaQH溶液,需NaQH的质量为g.
(2)计算MgSQ溶液中溶质的质量分数(列式计算).
沉淀质里/eI
21、某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验.
MOOOt渤I
请根据以上信息计算(结果保留到小数点后两位):
(1)反应生成沉淀的质量为
(2)样品中氯化钠的质量.
(3)滤液中溶质的质量分数.
参考答案
一、综合题
1、【考点】金属的化学性质;书写化学方程式.
【专题】金属与金属材料.
【分析】根据在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属
从其盐溶液中置换出来进行分析.
【解答】解:
(1)银的活动性排在铜之后,所以反应①中与铜粉反应的物质是硝酸银;
(2)反应②中发生的反应是硝酸铜和铁反应生成硝酸亚铁和铜,化学方程式是:
Fe+Cu(NG)2=Fe(NO)2+Cu;
(3)通过推导可知,固体丫中含有铁、铜,所以从固体丫中得到金属铜的方法有:
用磁铁吸弓I;在混合物中加入足
量的稀硫酸,然后过滤、洗涤、干燥.
故答案为:
(1)硝酸银;
(2)Fe+Cu(NQ)2=Fe(NQ)2+Cu;
(3)用磁铁吸引;
在混合物中加入足量的稀硫酸,然后过滤、洗涤、干燥.
【点评】本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.
二、计算题
2、.⑴10⑵红⑶NaQHNaCl3、【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】分析所发生的反应,可发现反应后总质量减轻是由于生成了气体二氧化碳,因此,可知恰好完全反应时放岀
二氧化碳的质量为4.4g;然后利用二氧化碳的质量,根据反应的化学方程式,分别计算恰好完全反应时碳酸钙的质量,最后使用质量分数的计算公式,求岀石灰石中碳酸钙的质量分数即可.
【解答】解:
由于该反应会生成二氧化碳气体,所以反应后减小的质量即为二氧化碳的质量;
设恰好完全反应时,消耗碳酸钙的质量为x,
CaCG+2HCI—CaCL+HO+COf
44
100
100
X
44
_4.4g
大理石中碳酸钙的质量分数:
解得:
x=10g
SHX100%=80%
4.4g
答:
大理石中碳酸钙的质量分数为80%
【点评】根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式
进行计算.
4、HCI和CaCI21.2g
5、【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【分析】
(1)根据过滤操作所用仪器分析解答;
(2)根据硫酸和氯化钡反应生成硫酸钡沉淀和氯化氢,利用沉淀的质量求岀生成氯化氢的质量及质量分数.
【解答】解:
(1)在过滤操作中需要的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)设生成氯化氢的质量为x
BaCW+HtSO—BaSQj+2HCI,
23373
23.3gx
233
x=7.3g
反应后所得溶液的溶质质量分数
X100%=7.3%
答案:
(1)烧杯、漏斗、玻璃棒;
(2)反应后所得溶液的溶质质量分数为7.3%.
6、(6分)
(1)4.4
(2)80%(3)10.5%
【解】生成二氧化碳的质量为:
100g+12.5g-108.1g=4.4g(1分)
设:
样品中碳酸钙的质量为x,生成氯化钙的质量为
CaCO+2HCI=CaCI2+H20+CO21
100111
x
解得:
x=10gy=11.1g
(2)样品中碳酸钙的质量分数为:
(3)烧杯中溶液质量为108.1g-(12.5g-10g)=105.6g
44
y4.4g
10g/12.5g=80%(3分)
(2分)
所得溶液的溶质质量分数为:
11.1g/105.6g=10.5%
答:
略
7、【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【专题】综合计算(图像型、表格型、情景型计算题).
【分析】根据图中数据可以判断生成氢气的质量;
根据氢气的质量可以计算稀硫酸中硫酸的质量,进一步可以计算所用硫酸溶液中溶质的质量分数.
【解答】解:
(1)由图中可知,完全反应后生成H2的质量为0.4g.
故填:
0.4.
(2)设所用硫酸溶液中溶质的质量为
Zn+H2SQ—ZnSO+Hd,
982
x0.4g
x=19.6g,
126g
所用硫酸溶液中溶质的质量分数为:
W弓X100%=19.6%,
答:
所用硫酸溶液中溶质的质量分数为19.6%.
【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.
8、【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】根据质量守恒定律,由反应前后固体减少的质量为反应放岀氧气的质量;再利用产生氧气的质量计算参加反
应的氯酸钾的质量,混合物质量与氯酸钾质量差即为二氧化锰的质量.
【解答】解:
根据质量守恒定律,反应放岀氧气的质量为3.2g
设氯酸钾的质量为x
Mn03
2KCIQ3△2KCI+3Q2f
24596
x3.2g
245二96
x3.2?
x=8.17g
原混合物中二氧化锰的质量=10g-8.17g=1.83g
答:
原混合物中二氧化锰的质量是1.83g.
【点评】由于二氧化锰在反应中为催化剂,反应前后质量不变,本题也可以由氧气质量计算反应生成氯化钾的质量,而由反应后固体求岀二氧化锰的质量.
9、【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
【分析】根据化学方程式计算所要计算的物质的量即可,注意0.2g的二氧化锰与计算无关•注意过程的完整性
【解答】解:
用2.45g氯酸钾最多可制取(指完全反应)氧气的质量设为x.
2KCIO3■2KCI+3O2f
245
96
2.45g
x
245
Z45呂
96
=X
x=0.96g
答:
2.45g氯酸钾最多可得到0.96g氧气.
其次过程中数据使用要正确,
【点评】根据方程式计算反应物或者生成物的质量时,一要注意方程式必须要正确,免无效的劳动.
10、解:
生成Hb的质量为:
8g+74.2g—82g=0.2g
设锌的质量为x,生成ZnSO的质量为y
Zn+fSQ===ZnSQ+Hbf
651612
xy0.2g
65:
2=x:
0.2gx=6.5g
杂质的质量二8g—6.5g=1.5g
161:
2=y:
0.2gy=16.1g
16上
反应后溶液的溶质质量分数=「匕x100%=20%
答:
(1)杂质的质量为1.5g;
(2)反应后所得溶液的溶质质量分数为20%。
11、【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算.
然后计算变质
【分析】根据质量守恒定律计算生成二氧化碳的质量,依据化学方程式计算参加反应的碳酸钠的质量,
后生成物质的质量分数.
【解答】解:
生成二氧化碳的质量为:
10g+50g-58.9g=1.1g
设参加反应的碳酸钠的质量为x
N3CG+2HCI—2NaCI+H2O+COf
106
44
I.ig
106
44
x=2.65g
=
所以变质后生成物质的质量分数为:
^X100%=26.5%.
故答案为:
26.5%.
【点评】本题主要考查含杂物质的计算,注意质量守恒定律的应用和有关化学方程式的计算,计算要细心、准确.
12、【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【分析】
(1)根据质量守恒定律求岀氧气的质量即可;
(2)根据氧气的质量求岀过氧化氢的质量,然后利用溶质质量分数公式求岀即可;
【解答】解:
(1)根据质量守恒定律,氧气的质量=(68g+11.6g)-78g=1.6g;
(1)设34g过氧化氢溶液中所含H2O2的质量为x
所用过氧化氢溶液的溶质质量分数=X100%=5%
答案:
(1)产生氧气的质量1.6g;
(2)原过氧化氢溶液中溶质的质量分数为5%
13、【考点】根据化学反应方程式的计算;有关溶质质量分数的简单计算.
【专题】溶质质量分数与化学方程式相结合的计算.
【分析】
(1)根据质量守恒定律,物质的总质量减少的质量就是生成的二氧化碳的质量;根据碳酸钠与硫酸的反应,由二氧化碳的质量可求岀反应的碳酸钠的质量、生成的硫酸钠的质量;
(2)根据碳酸钠的质量可求岀原混合物中硫酸钠的质量,即可求岀反应后溶液中溶质硫酸钠的质量.
【解答】解:
(1)设固体混合物中碳酸钠的质量为x,生成的硫酸钠的质量为y
NQCO+”SQ=Na2SQ+H2O+COf
10614244
xy4.4g
106二」42二44
/一y一第4g
解得:
x=10.6gy=14.2g
答:
固体混合物中碳酸钠的质量为10.6g;
(2)反应后所得溶液中溶质的质量分数:
=12.5%.
要求学生有较强的识图能力和数据分析能
【点评】本题利用图表及反应方程式来分析和解决化学计算中的有关问题,力.
14、
(1)佝偻病(1分)解:
设20片该药剂中含CaCO的质量为x,40g盐酸中含HCI的质量为y
CaCO+2HCI=CaCI2+H2O+CO2?
100
73
44
x
分)
y
IJ
(20g+40g-55.6g)
(1
10073
44
Xy4
(2分)
(1分)
10gy=7.3g
(2)10g-20=0.5g
(3)7.3g-40gX100%=18.3%(1分)
答:
该品牌补钙药剂每片含CaCO的质量为0.5g,该盐酸中溶质的质量分数为18.3%。
15、解:
(1)反应生成沉淀的质量为:
11g+100g+141g-242g=10g,
故填:
10.
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
NazCO+CaCb—CaCOJ+2NaCI,
106100117
x10gy
W_100117
:
=11=打,
X100%=5%
x=10.6g,y=11.7g,
滤液中溶质的质量分数为:
1理-10.6計11.尢
答:
滤液中溶质的质量分数为:
•‘Jyx100%=5%
29,[4廿J
鞘;石灰石申真IR钙的昭f为熄/沁则二伽
设反葩后生碇氛代钙的號萤为*生戍二氯化碳的洗旺为y
CaCO;+2HC1=CflCh1-H:
O+CO"
300HI441
心JTyJ
空•強e】i*堆
HI厲
竺■啦y=<4g
Jij
施后淄港中繹融质U甘数二H熔劇00輒Mil仇
峯门)生成二氧化礙的就豪为“彰3)超启所團雷找中擀舷量分數为订」“(緘设.番不金扣g分,三段不男设分數J
16、
17、解:
设5.8g生铁样品中铁的质量为x,反应生成的FeCl2的质量为y。
也应JG所郡FeClj解蔽中的沁威前就秋甘養为i
5.fig+9xKW*=12,A
答:
反应后所得FeCl2溶液中的溶质的质量分数为12.7%。
18、解:
(1)4.4g(1分)
(2)10%
设和化学方程式,以及化学方程式下方的相对分子质量和已知量未知量(1分)
比例式(1分),列式(1分)结果(1分)答(1分)
氧化碳的
19、解:
(1)由题目中图可以看岀:
当加入稀盐酸的质量为45g时,石灰石中的碳酸钙完全反应且生成.质量为2.2g;故答案为:
2.2;
CaCl2;HCl;
(2)由图示可知,加入60g稀盐酸后盐酸过量,故溶液中含有的溶质是氯化钙和氯化氢;故答案为:
(3)设样品中碳酸钙的质量分数为
CaCG+2HCI—CaCb+fO+COf
100
44
15gxx
2.2g
100
44
『5釘
2.2g
解之得:
x=33.3%
答:
样品中碳酸钙的质量分数为33.3%.
20、解:
(1配制100g溶质质量分数为10%的NaOH溶液,需NaOH的质量为:
100gx10%=10g.
(2)由反应的曲线可知,当加入40g氢氧化钠溶液时恰好完全反应;
设MgSO溶液中溶质的质量为x
MgSO+2NaO—Mg(OH2;+N@SQ
12080
MgSQ溶液中溶质的质量分数为:
=20%
x40gx10%
20%.
故答为:
(1)10.
(2)MgSQ溶液中溶质的质量分数为
21、解:
(1)反应生成沉淀的质量为:
10.00g+87.00g+54.65g-140.00g=11.65g,
(2)设硫酸钠的质量为x,生成氯化钠的质量为y,
BaCh+NaSO—BaSO;+2NaCl,
142233117
11.65gy
x=7.1g,y=5.85g,
样品中氯化钠的质量为:
10.00g-7.1g=2.9g,
答:
样品中氯化钠的质量是2.9g.
2.g吕ggg
X100%=6.25%
(3)滤液中溶质的质量分数为:
14600g
答:
滤液中溶质的质量分数为6.25%.